Clear Sky Science · pt
Câncer gástrico 18F-FDG-PET/CT-negativo usa gluconeogênese baseada em glutamina e oxidação de ácidos graxos para sustentar o crescimento tumoral
Por que alguns tumores do estômago se escondem à vista de todos
Exames modernos de câncer muitas vezes dependem de tumores ávidos por açúcar brilhando nas imagens de PET/CT. Ainda assim, muitos cânceres gástricos perigosos mal aparecem, deixando os médicos com uma visão fraca sobre onde a doença se encontra e quão rápido ela cresce. Este estudo faz uma pergunta aparentemente simples: se esses tumores não estão se empanturrando de açúcar, em que eles estão se sustentando? A resposta revela um artifício metabólico que não só explica por que as imagens ficam escuras, mas também aponta para novas maneiras de privar esses cânceres de alimento.
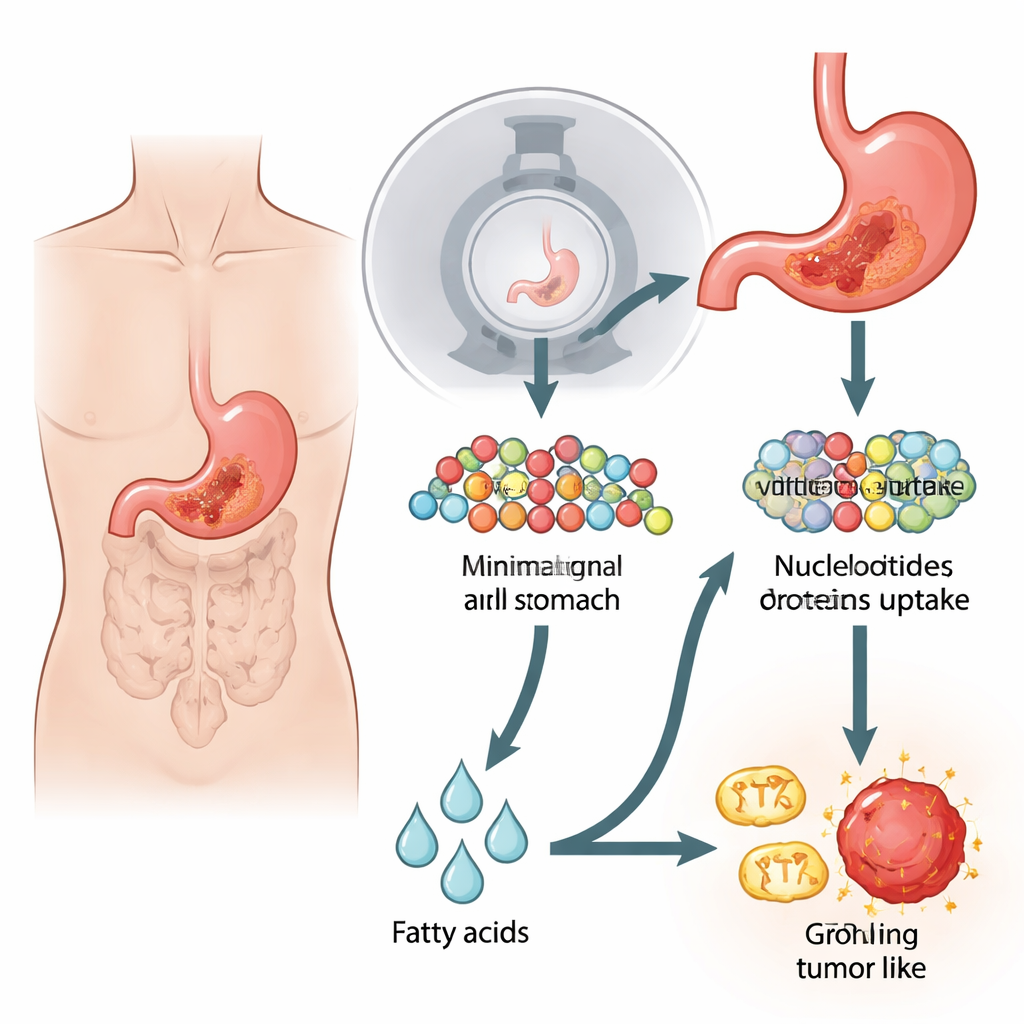
Quando o sinal habitual do açúcar desaparece
A maioria dos cânceres reprograma seu metabolismo para queimar glicose, um açúcar simples, mesmo quando há oxigênio suficiente. Esse “efeito Warburg” é a base dos exames padrão 18F-FDG PET/CT, que rastreiam um análogo radioativo do açúcar enquanto se acumula nos tumores. Mas certas formas de câncer gástrico, especialmente os tipos difuso e de anel de sinete, frequentemente aparecem negativas ou com sinal fraco nesses exames. Os autores recriaram essa situação intrigante no laboratório, estudando linhagens de células de câncer gástrico e tumores em camundongos que absorviam muito menos glicose e mostravam sinais fracos em PET/CT. Surpreendentemente, apesar do baixo uso de açúcar, essas células se dividiam tão rapidamente quanto células tumorais ávidas por glicose e permaneceram em grande parte indiferentes quando a glicólise — a via clássica de queima de açúcar — foi bloqueada.
Uma fábrica secreta de açúcar alimentada por glutamina
Aprofundando-se, os pesquisadores analisaram como esses tumores com pouco consumo de glicose estavam construindo os blocos necessários para copiar seu DNA e crescer. Descobriram que as células absorviam avidamente o aminoácido glutamina, muito mais do que outros aminoácidos. Usando experimentos de rastreamento com glutamina marcada, seguiram os átomos de carbono através do centro metabólico da célula até uma via reversa que se assemelha a executar a glicólise ao contrário. Esse processo, chamado gluconeogênese, permitiu que as células refizessem intermediários semelhantes a açúcares a partir da glutamina, que então alimentavam a produção de blocos de construção do DNA. Uma enzima-chave nesse desvio, PCK2, foi encontrada em níveis elevados em células e tumores PET-negativos. Quando a equipe bloqueou enzimas PCK com drogas ou ferramentas genéticas, os níveis de intermediários essenciais caíram, a síntese de DNA diminuiu e o crescimento das células tumorais foi fortemente reduzido.
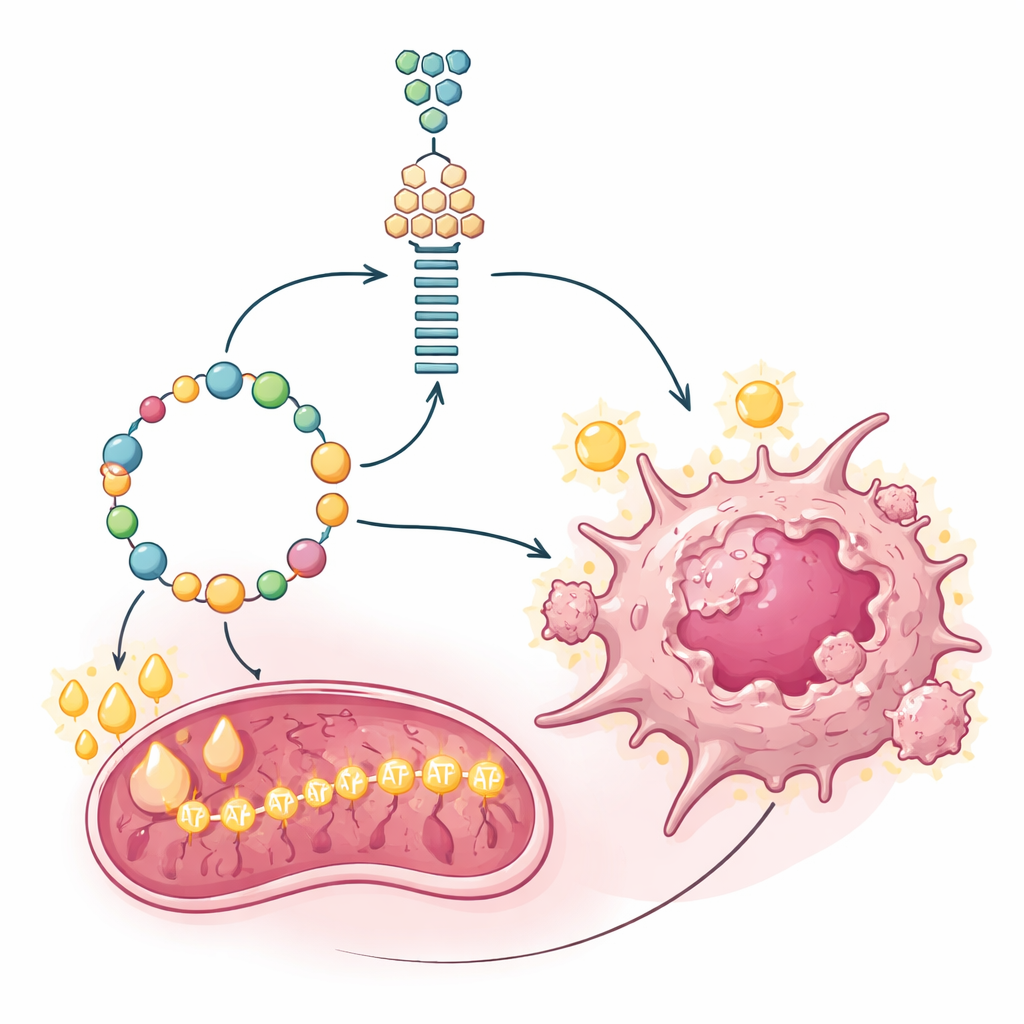
Gordura como combustível para a usina do câncer
Construir moléculas é apenas metade da batalha; tumores de rápido crescimento também precisam de grandes quantidades de energia. A própria gluconeogênese é custosa, consumindo energia em vez de gerá‑la. Os pesquisadores mediram como as células tumorais suspeitas produziam ATP, a moeda energética da célula, e descobriram que suas mitocôndrias estavam incomumente ativas. Em vez de dependerem principalmente de glicose ou glutamina para abastecer essas usinas, as células se apoiavam fortemente na oxidação de ácidos graxos — a quebra de gorduras. Uma enzima porteira para a importação de gorduras nas mitocôndrias, CPT1A, estava fortemente elevada em células e tumores PET-negativos. Bloquear CPT1A com um inibidor específico esvaziou os níveis de ATP e retardou a proliferação celular, revelando que a queima de gordura era o principal motor que sustentava tanto a produção de energia quanto o custoso atalho gluconeogênico.
Um interruptor mestre e uma impressão digital molecular
Para entender o que liga esse programa metabólico, os autores buscaram fatores de transcrição — interruptores mestres que controlam a expressão gênica — que poderiam estar impulsionando tanto a gluconeogênese quanto a oxidação de gorduras. Eles se concentraram no PPARγ, que estava marcadamente aumentado em cânceres gástricos PET-negativos. Esse fator ligou-se diretamente às regiões de controle dos genes PCK2 e CPT1A, aumentando sua atividade enquanto deixava o principal transportador de glicose, GLUT1, amplamente inalterado. Em amostras de pacientes e conjuntos de dados de célula única, tumores com baixo GLUT1 (baixo consumo de açúcar) mostraram consistentemente altos níveis de PCK2 e CPT1A. Clinicamente, esse padrão foi mais pronunciado em subtipos agressivos de câncer gástrico que frequentemente escapam à imagem por PET e estão ligados a pior sobrevida, sugerindo que essa impressão digital metabólica marca tumores particularmente perigosos e silenciosos em relação ao açúcar.
Transformando uma fraqueza metabólica em uma janela terapêutica
Por fim, a equipe testou se essa escolha incomum de combustíveis poderia ser usada contra o câncer. Em modelos de camundongo derivados de linhagens celulares e em modelos feitos diretamente a partir de tumores de pacientes, drogas que inibiam a gluconeogênese conduzida por PCK ou a queima de gordura dependente de CPT1A retardaram, cada uma, o crescimento de tumores gástricos PET-negativos. Quando combinados, os dois tratamentos tiveram efeito ainda mais forte, encolhendo tumores e reduzindo marcadores de divisão celular, enquanto tumores PET-positivos e ávidos por açúcar foram muito menos afetados. Em termos práticos, o estudo mostra que alguns cânceres do estômago sobrevivem não queimando o açúcar que procuramos nas imagens, mas convertendo glutamina em intermediários semelhantes a açúcar e mantendo suas “motores” funcionando com gordura. Cortando esses suprimentos de reserva, pode ser possível expor e tratar de forma eficaz tumores que hoje se escondem nas sombras da imagiologia padrão.
Citação: Liu, J., Xia, M., Zhao, Z. et al. 18F-FDG-PET/CT-negative gastric cancer employs glutamine-based gluconeogenesis and fatty acid oxidation to support tumor growth. Cell Death Dis 17, 365 (2026). https://doi.org/10.1038/s41419-026-08662-9
Palavras-chave: metabolismo do câncer gástrico, tumores negativos em FDG-PET, gluconeogênese a partir de glutamina, oxidação de ácidos graxos, PPARgamma PCK2 CPT1A