Clear Sky Science · ja
18F-FDG-PET/CT陰性胃がんは腫瘍増殖を支えるためにグルタミン由来の糖新生と脂肪酸酸化を利用する
なぜ一部の胃腫瘍は見つかりにくいのか
現代のがん画像診断は、多くの場合、糖を大量に取り込む腫瘍がPET/CT画像で明るく映ることに依存しています。しかし、危険な胃がんの中にはほとんど画像に写らないものがあり、医師は病変の位置や増殖速度を把握しにくくなります。本研究は一見単純な疑問を投げかけます:もしこれらの腫瘍が糖を大量に消費していないなら、何を栄養源にしているのか?その答えは、画像が暗くなる理由を説明するだけでなく、こうしたがんを飢えさせる新たな方法を示唆する代謝の“トリック”を明らかにします。
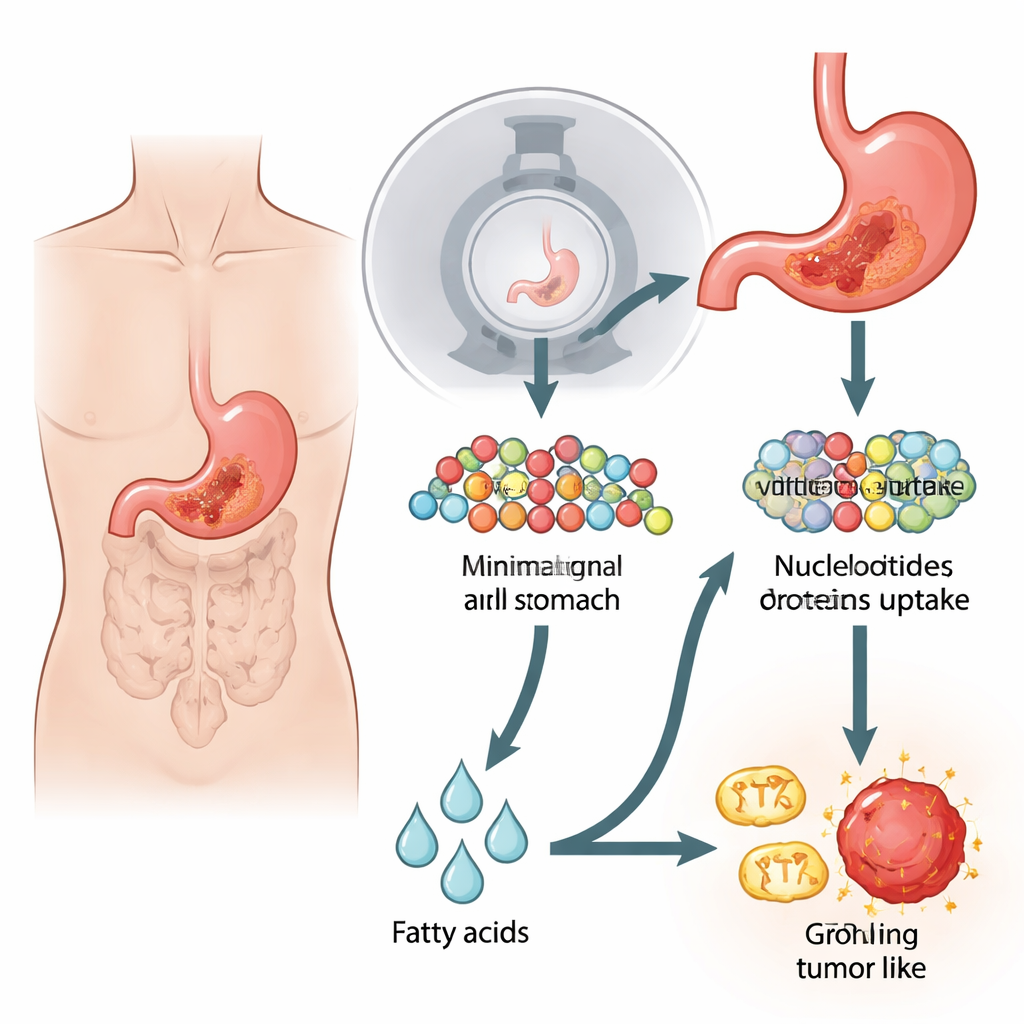
通常の糖シグナルが消えるとき
ほとんどのがんは、酸素が十分にある状況でもブドウ糖を燃やすよう代謝を書き換えます。この「ワールブルグ効果」が、放射性糖類似体の蓄積を追跡する標準的な18F-FDG PET/CT検査の基盤です。しかし、特にびまん性や印環(リング)型の攻撃的な胃がんは、これらの検査で陰性または薄くしか映らないことが多い。著者らは、がん細胞株やマウス腫瘍を用いて、これらの興味深い状況を再現しました。これらのモデルはブドウ糖の取り込みが大幅に少なく、PET/CT信号も弱かったのです。驚くべきことに、糖の利用が乏しいにもかかわらず、これらの細胞は糖を好むがん細胞と同じように速く分裂し、従来の糖分解(解糖)経路を遮断しても大きな影響を受けませんでした。
グルタミンで駆動される秘密の糖合成工場
さらに解析を進めると、これらの低グルコース腫瘍がDNA合成や増殖に必要な原料をどのように作り出しているかが明らかになりました。細胞は他のアミノ酸よりもはるかに多く、アミノ酸グルタミンを積極的に取り込んでいました。標識したグルタミンを用いたトレーシング実験で、グルタミン由来の炭素が細胞の中心的代謝経路を経て解糖を逆行するような経路に流れ込むことが追跡されました。この過程は糖新生と呼ばれ、グルタミンから糖様の中間体を再合成して、それがDNAの材料合成に供給されます。この迂回路の鍵となる酵素PCK2は、PET陰性の細胞や患者腫瘍で高発現していました。PCK酵素を薬剤や遺伝学的手法で阻害すると、重要な糖中間体の量が低下し、DNA合成が遅延し、腫瘍細胞の増殖が著しく抑制されました。
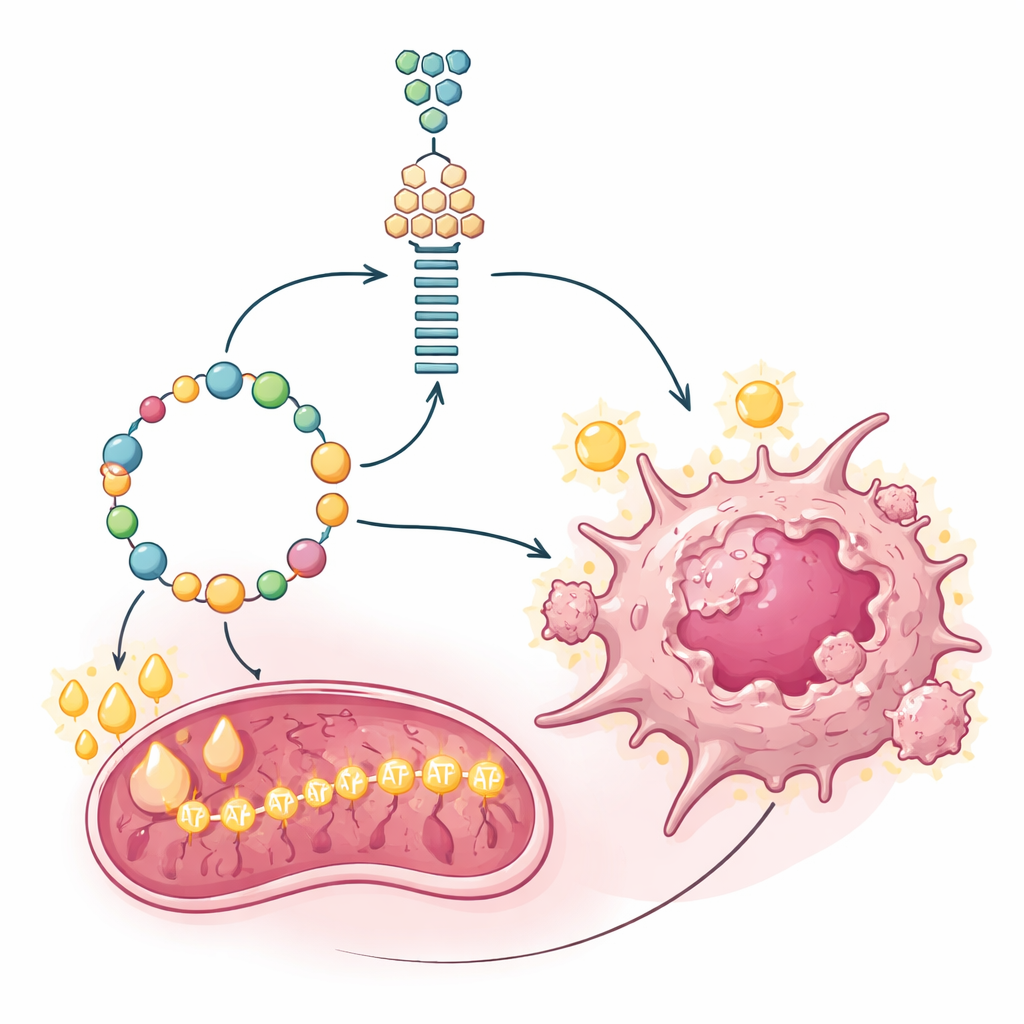
がんの発電所を動かす燃料としての脂肪
分子合成は半分の戦いに過ぎません。急速に増殖する腫瘍は大量のエネルギーも必要とします。糖新生自体はエネルギーを消費する反応です。研究者らは問題のがん細胞がどのようにATP(細胞のエネルギー通貨)を産生しているかを測定し、これらの細胞のミトコンドリアが異常に活発であることを見出しました。糖やグルタミンに頼るのではなく、これらの細胞は脂肪酸の酸化、すなわち脂肪の分解に大きく依存していました。脂肪をミトコンドリアに輸送する門番酵素であるCPT1Aは、PET陰性の細胞や腫瘍で強く上昇していました。CPT1Aを特異的阻害剤で遮断するとATPレベルが低下し、細胞増殖が遅くなり、脂肪燃焼がエネルギー産生と高コストの糖新生を支える主要なエンジンであることが示されました。
マスター・スイッチと分子の指紋
この代謝プログラムをオンにする因子を理解するために、著者らは糖新生と脂肪酸酸化の両方を駆動している可能性のある転写因子—遺伝子発現を制御するマスター・スイッチ—を探索しました。彼らはPPARγに注目し、PET陰性胃がんで顕著に増加していることを突き止めました。PPARγはPCK2およびCPT1A遺伝子の制御領域に直接結合し、これらの活性を高める一方で、主要なグルコース輸送体GLUT1にはほとんど影響を与えていませんでした。患者サンプルと単一細胞データセット全体で、GLUT1が低く(糖取り込みが乏しい)PCK2とCPT1Aが高い腫瘍は一貫して観察されました。臨床的には、このパターンはPET画像を回避しやすく予後不良と関連する攻撃的な胃がん亜型で最も顕著であり、この代謝的指紋が特に危険な糖に反応しない腫瘍を示す可能性があることを示唆しています。
代謝的弱点を治療の窓口に変える
最後に、研究チームはこの異常な燃料選択をがんに対して利用できるかを試しました。細胞株由来モデルと患者腫瘍由来のモデルの両方で、PCK駆動の糖新生やCPT1A依存の脂肪燃焼を阻害する薬剤はいずれもPET陰性胃腫瘍の増殖を遅らせました。両者を併用すると、腫瘍はさらに縮小し、細胞分裂の指標も低下しました。一方で、糖を好むPET陽性腫瘍は影響がはるかに小さかった。平たく言えば、本研究は一部の胃がんが検査で探す糖を燃やすのではなく、グルタミンを糖様の前駆体に変換し、エンジンを脂肪で回して生き延びていることを示しています。これらの代替供給を断てば、標準的な画像診断の陰に隠れている腫瘍を露出させ、有効に治療できる可能性があるのです。
引用: Liu, J., Xia, M., Zhao, Z. et al. 18F-FDG-PET/CT-negative gastric cancer employs glutamine-based gluconeogenesis and fatty acid oxidation to support tumor growth. Cell Death Dis 17, 365 (2026). https://doi.org/10.1038/s41419-026-08662-9
キーワード: 胃がんの代謝, FDG-PET陰性腫瘍, グルタミン由来糖新生, 脂肪酸酸化, PPARgamma PCK2 CPT1A