Clear Sky Science · ar
سرطان المعدة السلبي في فحص 18F‑FDG‑PET/CT يعتمد على تكوين السكر من الغلوتامين وتأكسد الأحماض الدهنية لدعم نمو الورم
لماذا تختبئ بعض أورام المعدة في العلن
تعتمد الفحوص الحديثة للسرطان غالبًا على ظهور الأورام الجائعة للسكر عند تصوير PET/CT. ومع ذلك، فإن العديد من سرطانات المعدة الخطيرة بالكاد تظهر على هذه الصور، ما يترك الأطباء بصورة باهتة عن مكان المرض وسرعة نموه. تطرح هذه الدراسة سؤالاً بسيطًا تخفيه بساطته: إذا لم تكن هذه الأورام تلتهم السكر، فبماذا تتغذى بدلًا من ذلك؟ تكشف الإجابة عن حيلة أيضية لا تفسر فقط سبب ظلمة الصور، بل تشير أيضًا إلى طرق جديدة لتجويع هذه السرطانات.
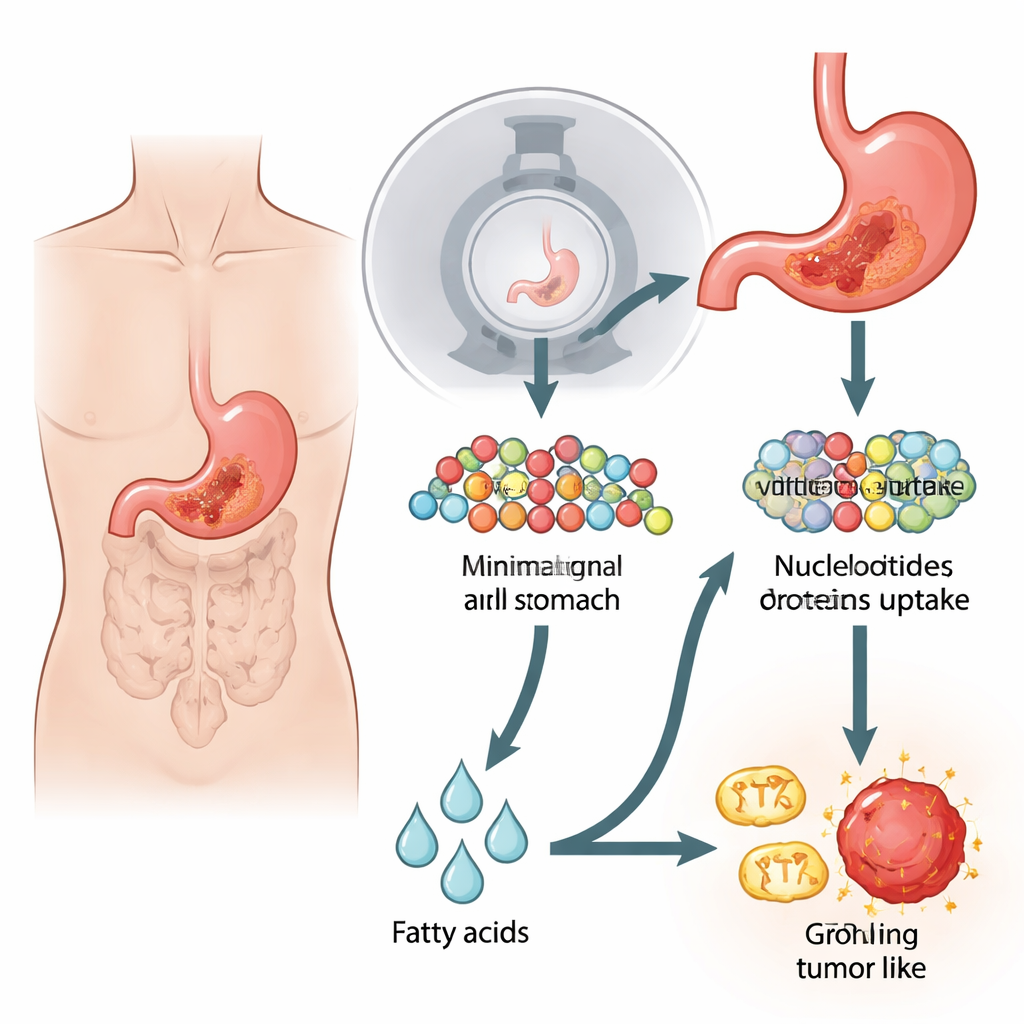
عندما يختفي إشارة السكر الاعتيادية
تعيد معظم السرطانات برمجة أيضها لحرق الجلوكوز، وهو سكر بسيط، حتى في وجود الأكسجين. هذا «تأثير واربورغ» هو أساس فحوص 18F‑FDG PET/CT الاعتيادية، التي تتعقب مماثل سكر مشع وهو يتراكم في الأورام. لكن أشكالًا معينة من سرطان المعدة، لا سيما النماذج الغازية والحوَلية (signet‑ring)، غالبًا ما تبدو سلبية أو خافتة في هذه الفحوص. أعاد المؤلفون خلق هذا الموقف المحير في المختبر بدراسة خطوط خلايا سرطان المعدة وأورام الفئران التي امتصت كميات أقل بكثير من الجلوكوز وأظهرت إشارات PET/CT ضعيفة. وبشكل مفاجئ، وعلى الرغم من استخدام هذه الخلايا الضعيف للسكر، كانت تنقسم بسرعة مماثلة لخلايا السرطان المحبة للسكر وبقيت إلى حد كبير غير متأثرة عندما تم حجب التحلل السكري — الطريق الكلاسيكي لحرق السكر.
مصنع سري للسكر مدفوع بالغلوتامين
عميقًا في التفاصيل، نظر الباحثون إلى كيفية بناء هذه الأورام منخفضة السكر للمواد الخام اللازمة لنسخ الحمض النووي والنمو. اكتشفوا أن الخلايا تمتص حمض الأمينو الغلوتامين بنهم، أكثر بكثير من الأحماض الأمينية الأخرى. ومن خلال تجارب تتبع باستخدام غلوتامين معنّن، تتبعوا ذرات الكربون عبر المحور الأيضي المركزي للخلايا وإلى مسار عكسي يشبه تشغيل تحلل السكر بالعكس. تسمح هذه العملية، المسماة تكوين السكر (gluconeogenesis)، للخلايا بإعادة صنع وسطيات شبيهة بالسكر من الغلوتامين، والتي تغذي بعد ذلك إنتاج لبنات بناء الحمض النووي. وُجد إنزيم رئيسي في هذا التحويل، PCK2، بمستويات عالية في الخلايا والأورام السلبية في فحص PET. عندما أعاق الفريق إنزيمات PCK بالأدوية أو بالطرق الجينية، انخفضت مستويات وسطيات السكر الحرجة، تباطأ تصنيع الحمض النووي، وتقلص نمو خلايا الورم بشدة.
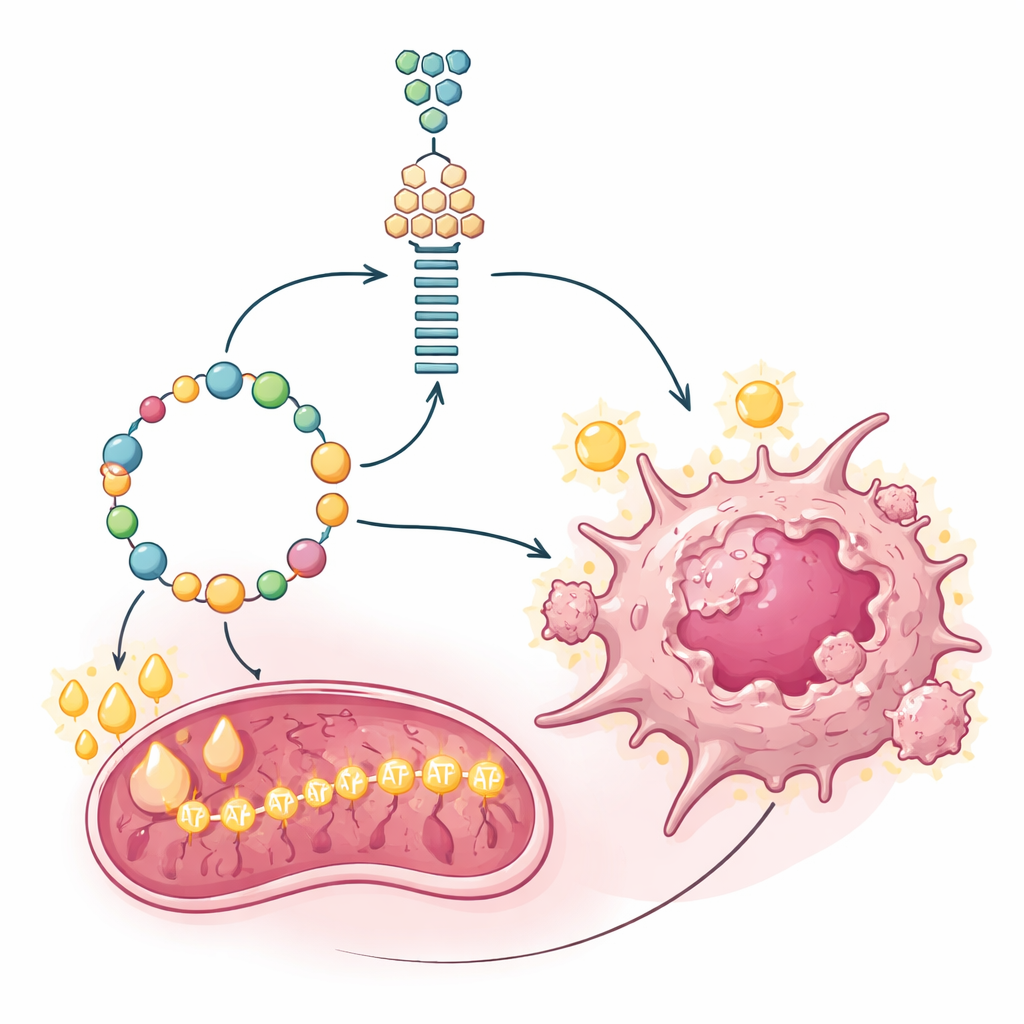
الدهون كوقود لمحطة طاقة السرطان
بناء الجزيئات هو نصف المعركة فقط؛ تحتاج الأورام سريعة النمو أيضًا إلى كميات كبيرة من الطاقة. تكوين السكر نفسه مكلف، يستهلك الطاقة بدلًا من توليدها. قيَّم الباحثون كيف تولد الخلايا المشتبه بها ATP، عملة الطاقة الخلوية، ووجدوا أن ميتوكوندريا هذه الخلايا كانت نشطة بشكل غير عادي. بدلًا من الاعتماد أساسًا على السكر أو الغلوتامين لتغذية هذه المحطات، اعتمدت الخلايا بشكل كبير على تأكسد الأحماض الدهنية — تكسير الدهون. كان إنزيم بوَّاب لاستيراد الدهون إلى الميتوكوندريا، CPT1A، مرتفعًا بقوة في الخلايا والأورام السلبية في PET. إيقاف CPT1A بمثبط محدد استنزف مستويات ATP وأبطأ تكاثر الخلايا، كاشفًا أن حرق الدهون كان المحرك الرئيسي الداعم لكل من إنتاج الطاقة وامتداد اختصار تكوين السكر المكلف.
مفتاح تحكم وبصمة جزيئية
لفهم ما يشغل هذا البرنامج الأيضي، بحث المؤلفون عن عوامل نسخ — مفاتيح رئيسية تتحكم في التعبير الجيني — قد تقود كلًا من تكوين السكر وتأكسد الدهون. ركزوا على PPARγ، الذي ارتفع بدرجة ملحوظة في سرطانات المعدة السلبية في PET. ربط هذا العامل مباشرة بمناطق التحكم في جينات PCK2 وCPT1A، معززًا نشاطهما بينما ترك الناقل الغلوزي الرئيسي GLUT1 إلى حد بعيد دون تغيير. عبر عينات المرضى وبيانات الخلية المفردة، أظهرت الأورام ذات GLUT1 المنخفض (ضعف امتصاص السكر) مستويات مرتفعة ثابتة من PCK2 وCPT1A. سريريًا، كان هذا النمط أكثر وضوحًا في الأنواع الغازية من سرطان المعدة التي غالبًا ما تهرب من تصوير PET وترتبط ببقاء أسوأ، مما يشير إلى أن هذه البصمة الأيضية تميّز أورامًا خطيرة خاصة صامتة بالنسبة للسكر.
تحويل الضعف الأيضي إلى نافذة علاجية
أخيرًا، اختبر الفريق ما إذا كان يمكن استغلال اختيار الوقود غير العادي هذا ضد السرطان. في نماذج فئران مبنية من خطوط خلوية ونماذج مُشتقة مباشرة من أورام مرضى، أبطأت الأدوية التي تثبط تكوين السكر المدفوع بواسطة PCK أو حرق الدهون المعتمد على CPT1A نمو أورام المعدة السلبية في فحص PET. عند الجمع بين العلاجين، كان للأثر تأثير أقوى، حيث تقلصت الأورام وانخفضت علامات الانقسام الخلوي، بينما كانت الأورام الإيجابية في PET والشرهة للسكر أقل تأثرًا بكثير. بعبارات بسيطة، تُظهر الدراسة أن بعض سرطانات المعدة لا تبقى على قيد الحياة بحرق السكر الذي نبحث عنه في الصور، بل بتحويل الغلوتامين إلى وسطيات شبيهة بالسكر وتشغيل محركاتها بالدهون. بقطع هذه الإمدادات الاحتياطية، قد يكون من الممكن كشف هذه الأورام ومعالجتها بفاعلية التي تختبئ حاليًا في ظلال التصوير القياسي.
الاستشهاد: Liu, J., Xia, M., Zhao, Z. et al. 18F-FDG-PET/CT-negative gastric cancer employs glutamine-based gluconeogenesis and fatty acid oxidation to support tumor growth. Cell Death Dis 17, 365 (2026). https://doi.org/10.1038/s41419-026-08662-9
الكلمات المفتاحية: أيض سرطان المعدة, أورام سلبية في فحص FDG‑PET, تكوين السكر من الغلوتامين, تأكسد الأحماض الدهنية, PPARgamma PCK2 CPT1A