Clear Sky Science · pl
Przeznaczenie kaspofunginy jako inhibitora małocząsteczkowego toksyny α Clostridium perfringens w leczeniu zgorzeli gazowej
Groźna infekcja potrzebująca lepszych metod leczenia
Zgorzel gazowa to szybko postępująca, często śmiertelna infekcja, która może wystąpić po poważnych urazach lub czasem pojawić się bez wyraźnego ostrzeżenia. Wywołuje ją bakteria Clostridium perfringens, produkująca silne toksyny, które rozrywają mięśnie, przerywają przepływ krwi i w ciągu kilku godzin przytłaczają organizm. Obecne metody leczenia — pilna interwencja chirurgiczna, antybiotyki i czasem terapia tlenowa — mogą ratować życie, ale nie zawsze zatrzymują uszkodzenia na czas. W tym badaniu sprawdzono, czy istniejący lek przeciwgrzybiczy, kaspofungina, można przeznaczyć ponownie do bezpośredniego unieszkodliwienia głównej toksyny bakterii i zaoferowania nowej, szybszej metody ochrony pacjentów.
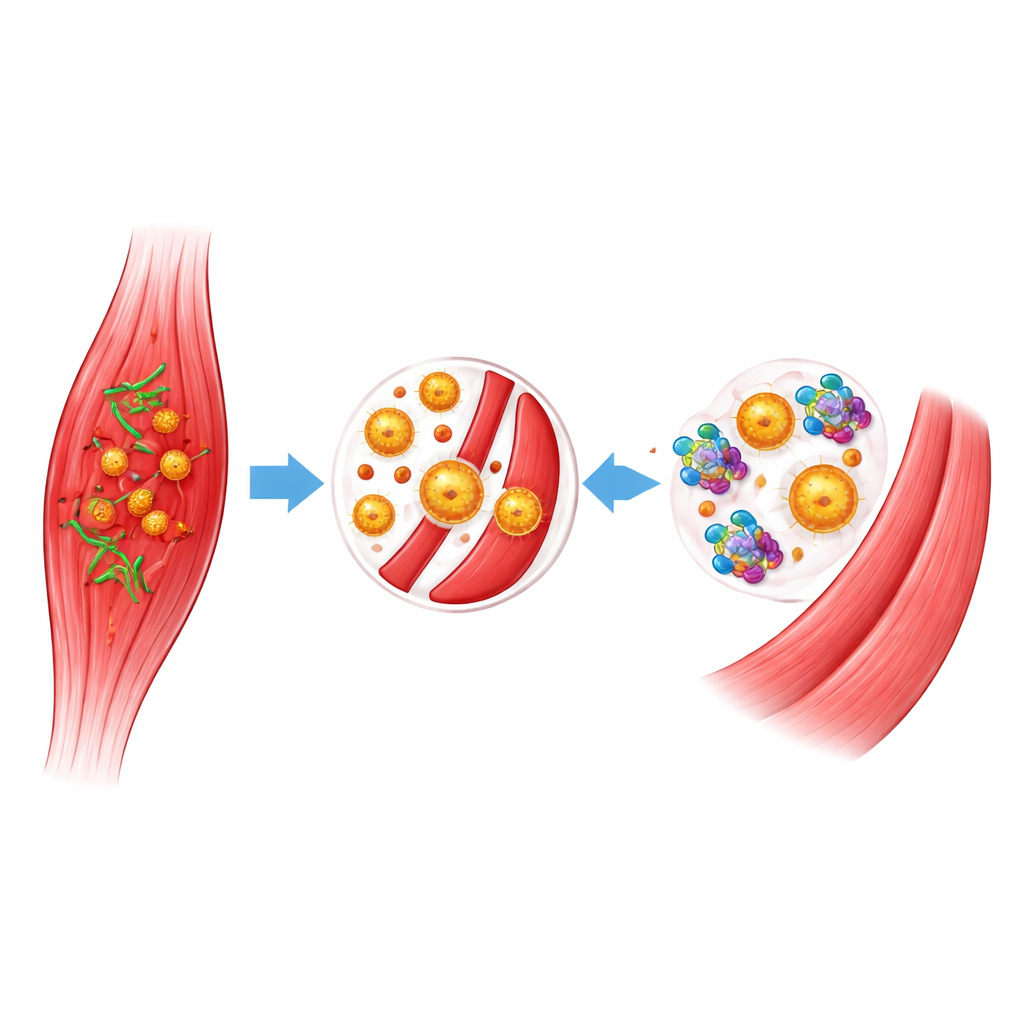
Toksyna bakteryjna niszcząca mięśnie i przepływ krwi
C. perfringens wytwarza kilka toksyn, ale kluczową rolę w zgorzeli gazowej odgrywa toksyna alfa. Toksyna alfa atakuje istotne lipidy w błonach komórkowych, zabijając komórki mięśni i naczyń krwionośnych oraz ułatwiając rozprzestrzenianie się bakterii. Zakłóca też działanie układu odpornościowego, powodując zlepianie się białych krwinek i płytek krwi, blokując drobne naczynia i uniemożliwiając komórkom zwalczającym infekcję dotarcie do ogniska. Z czasem to zaciśnięcie krążenia prowadzi do masywnego obumierania mięśni, wstrząsu i niewydolności narządów. Ponieważ toksyna alfa napędza tak dużą część tego zniszczenia, blokowanie jej aktywności jest atrakcyjną strategią spowolnienia lub zatrzymania choroby.
Poszukiwanie nowych zastosowań w starych lekach
Zamiast zaczynać od zera i opracowywać nowy lek, badacze przesiewali 764 leki już zatwierdzone do stosowania u ludzi. Testowali każdy z nich pod kątem zdolności do zablokowania aktywności enzymatycznej toksyny alfa, koncentrując się na tym, jak dobrze potrafi ona powstrzymać toksynę przed rozcinaniem kluczowego lipidu błonowego. Z tej obszernej biblioteki 21 związków istotnie zmniejszyło aktywność toksyny. Zespół przeprowadził następnie drugi, bardziej wymagający test przy użyciu hodowanych ludzkich komórek naczyń krwionośnych. Tylko jeden lek, mikafungina — środek przeciwgrzybiczy stosowany w szpitalach — ochronił te komórki przed śmiercią wywołaną toksyną. Do eksperymentów włączono potem pokrewną mikafunginie kaspofunginę, ze względu na podobną strukturę i profil kliniczny.
Jak dwa leki przeciwgrzybicze wiążą się z toksyną
Zarówno mikafungina, jak i kaspofungina okazały się zdolne zablokować zdolność toksyny alfa do zabijania ludzkich komórek naczyń oraz do indukowania wydzielania cząsteczek zapalnych. Modele komputerowe sugerowały dlaczego: leki wydają się osiadać w wnęce na toksynie, gdzie normalnie wiązałby się jej naturalny, lipidowy cel. Sztywne łańcuchy boczne mikafunginy sięgają głębiej w tę kieszeń i tworzą wiele ścisłych kontaktów, podczas gdy bardziej elastyczny łańcuch boczny kaspofunginy osadza się płycej i tworzy mniej silnych wiązań. Różnice te odpowiadają pomiarom laboratoryjnym pokazującym, że mikafungina jest silniejszym inhibitorem jednej z aktywności toksyny. Jednak kaspofungina zachowuje się inaczej w odniesieniu do innego aspektu funkcji enzymu, co sugeruje, że subtelne różnice w dokowaniu każdego leku do toksyny mogą zmieniać jej działanie.
Od komórek do myszy: testy ochrony in vivo
Zablokowanie toksyny w probówce jest ważne, ale prawdziwą próbą jest, czy ochrona utrzyma się w żywym organizmie. Gdy myszom podano oczyszczoną toksynę alfa, większość nieleczonych zwierząt zmarła w ciągu doby. Myszom, które otrzymały kaspofunginę wraz z toksyną, w dużej mierze udało się przeżyć, co pokazuje, że lek może stłumić śmiertelne działanie toksyny w organizmie. Co zaskakujące, mikafungina, mimo silniejszego blokowania w testach in vitro, przy tej samej dawce nie poprawiła przeżywalności. Autorzy sugerują, że drobne różnice w tym, jak mocno leki wiążą się z białkami krwi — a zatem ile wolnego leku jest dostępne do neutralizacji toksyny — mogą wyjaśniać tę rozbieżność. W drugim modelu, gdy myszy zakażono żywymi C. perfringens w mięśniu uda, kaspofungina znacząco opóźniła śmierć i zmniejszyła uszkodzenie mięśni. W połączeniu ze standardowym antybiotykiem klindamycyną zarówno przeżywalność, jak i ochrona mięśni poprawiły się jeszcze bardziej.
Co to może znaczyć dla leczenia zgorzeli gazowej
Badanie dochodzi do wniosku, że kaspofungina, lek już stosowany klinicznie w ciężkich zakażeniach grzybiczych, ma duży potencjał jako terapia ukierunkowana na toksynę w zgorzeli gazowej. Zamiast zabijać bakterie bezpośrednio, kaspofungina rozbraja ich główną broń, dając standardowym antybiotykom i zabiegom chirurgicznym więcej czasu na działanie oraz pomagając chronić mięśnie i naczynia krwionośne przed katastrofalnym uszkodzeniem. Ponieważ kaspofungina jest już zatwierdzona i szeroko dostępna, w zasadzie mogłaby zostać szybciej włączona do badań klinicznych pod kątem zgorzeli gazowej niż zupełnie nowy związek. Szerzej rzecz ujmując, praca pokazuje, że przeszukiwanie istniejących bibliotek leków może ujawnić małe cząsteczki neutralizujące toksyny bakteryjne, otwierając drzwi do nowej klasy terapii koncentrujących się na blokowaniu szkód, a nie tylko atakowaniu drobnoustrojów.
Cytowanie: Takehara, M., Homma, Y., Ishihara, T. et al. Repurposing caspofungin as a small-molecule inhibitor of Clostridium perfringens α-toxin for treatment of gas gangrene. Commun Med 6, 225 (2026). https://doi.org/10.1038/s43856-026-01503-y
Słowa kluczowe: zgorzel gazowa, Clostridium perfringens, toksyny bakteryjne, ponowne wykorzystanie leków, kaspofungina