Clear Sky Science · es
Reorientación de caspofungina como inhibidor de pequeña molécula de la α-toxina de Clostridium perfringens para el tratamiento de la gangrena gaseosa
Una infección peligrosa que necesita mejores tratamientos
La gangrena gaseosa es una infección de evolución rápida y a menudo mortal que puede seguir a heridas graves o, en ocasiones, aparecer sin aviso. Está causada por la bacteria Clostridium perfringens, que libera potentes toxinas que destripan el músculo, cortan el flujo sanguíneo y abruman al organismo en cuestión de horas. Los tratamientos actuales —cirugía urgente, antibióticos y a veces terapia con oxígeno— pueden salvar vidas, pero no siempre detienen el daño a tiempo. Este estudio explora si un fármaco antifúngico ya existente, la caspofungina, podría reutilizarse para desactivar directamente la principal toxina de la bacteria y ofrecer una forma nueva y más rápida de proteger a los pacientes.
La toxina bacteriana que destruye músculo y flujo sanguíneo
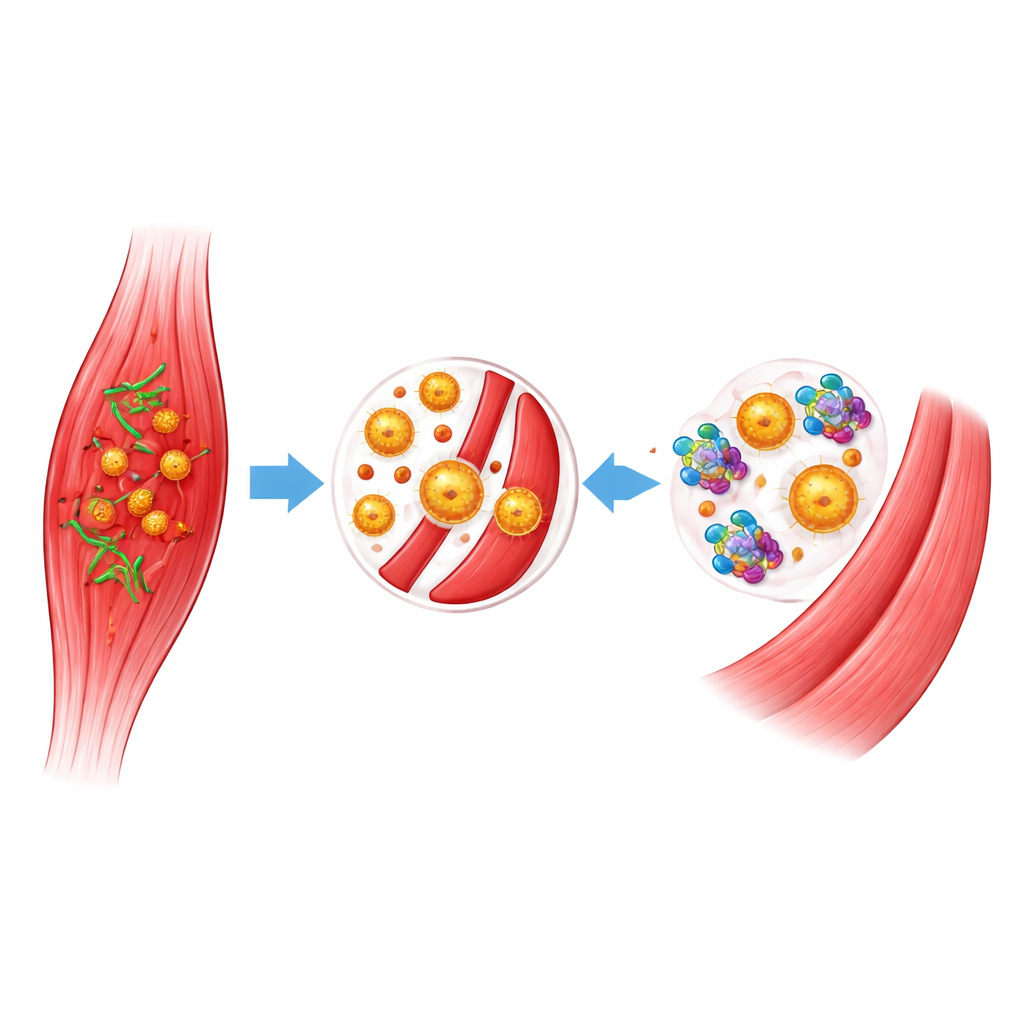
C. perfringens produce varias toxinas, pero una llamada α-toxina desempeña un papel central en la gangrena gaseosa. La α-toxina ataca lípidos clave en las membranas celulares, matando células musculares y de los vasos sanguíneos y facilitando la propagación bacteriana. También altera el sistema inmunitario al provocar que los glóbulos blancos y las plaquetas se agreguen, bloqueando los capilares y evitando que las células que combaten la infección lleguen al lugar afectado. Con el tiempo, este estrangulamiento de la circulación provoca una muerte muscular severa, shock y fallo orgánico. Dado que la α-toxina impulsa gran parte de esta devastación, bloquear su actividad es una estrategia atractiva para frenar o detener la enfermedad.
Buscando usos nuevos en medicamentos antiguos
En lugar de empezar de cero para inventar un fármaco nuevo, los investigadores examinaron 764 medicamentos ya aprobados para uso humano. Probaron cada uno por su capacidad para bloquear la actividad enzimática de la α-toxina, centrándose en cuánto podían impedir que la toxina cortara un lípido membrana clave. De esta amplia biblioteca, 21 compuestos redujeron sustancialmente la actividad de la toxina. El equipo realizó entonces una segunda prueba, más exigente, usando células de vasos sanguíneos humanos en cultivo. Solo un fármaco, micafungina —un antifúngico utilizado en hospitales— protegió a estas células de la muerte inducida por la toxina. Un antifúngico relacionado, la caspofungina, se incorporó después a los experimentos porque tiene una estructura y perfil clínico similares.
Cómo dos antifúngicos se adhieren a la toxina
Tanto la micafungina como la caspofungina demostraron ser capaces de bloquear la capacidad de la α-toxina para matar células de los vasos sanguíneos humanos y para impulsar la liberación de moléculas inflamatorias. El modelado por ordenador sugirió la razón: los fármacos parecen alojarse en una cavidad de la toxina donde normalmente se uniría su diana lipídica natural. La cadena lateral rígida de la micafungina encaja profundamente en este bolsillo, formando muchos contactos estrechos, mientras que la cadena lateral más flexible de la caspofungina se sitúa de forma más superficial y crea menos enlaces fuertes. Estas diferencias coinciden con medidas de laboratorio que muestran que la micafungina es el bloqueador más potente de una de las actividades de la toxina. No obstante, la caspofungina se comporta de manera distinta en otro aspecto de la función enzimática, lo que sugiere que sutiles variaciones en cómo se acoplan cada fármaco a la toxina pueden reshaper su comportamiento.
De las células a los ratones: probando la protección en animales vivos
Bloquear una toxina en una placa es importante, pero la verdadera prueba es si esa protección se mantiene en un animal vivo. Cuando a ratones se les administró α-toxina purificada, la mayoría de los animales no tratados murieron en menos de un día. Los ratones que recibieron caspofungina junto con la toxina, sin embargo, sobrevivieron en su mayoría, demostrando que el fármaco puede mitigar los efectos letales de la toxina en el organismo. Sorprendentemente, la micafungina, a pesar de ser un bloqueador más potente en tubos de ensayo, no mejoró la supervivencia a la misma dosis. Los autores sugieren que pequeñas diferencias en la afinidad de estos fármacos por las proteínas sanguíneas —y por tanto en la fracción de fármaco libre disponible para neutralizar la toxina— pueden explicar esta discrepancia. En un segundo modelo, en el que ratones fueron infectados en el músculo de la pierna con C. perfringens vivo, la caspofungina retrasó significativamente la muerte y redujo el daño muscular. Cuando se combinó con el antibiótico estándar clindamicina, tanto la supervivencia como la preservación del músculo mejoraron todavía más.
Qué podría significar esto para el tratamiento de la gangrena gaseosa
El estudio concluye que la caspofungina, un fármaco ya en uso clínico para infecciones fúngicas graves, tiene un fuerte potencial como terapia dirigida a la toxina para la gangrena gaseosa. En lugar de matar directamente a la bacteria, la caspofungina desarma su arma principal, dando más tiempo a los antibióticos y a la cirugía para actuar y ayudando a proteger el músculo y los vasos sanguíneos de una lesión catastrófica. Dado que la caspofungina ya está aprobada y es ampliamente accesible, en principio podría pasar a ensayos clínicos para la gangrena gaseosa con mayor rapidez que un compuesto totalmente nuevo. En un sentido más amplio, el trabajo muestra cómo el examen de bibliotecas de fármacos existentes puede descubrir pequeñas moléculas que neutralizan toxinas bacterianas, abriendo la puerta a una nueva clase de tratamientos que se centran en bloquear el daño en lugar de limitarse a atacar a los microbios.
Cita: Takehara, M., Homma, Y., Ishihara, T. et al. Repurposing caspofungin as a small-molecule inhibitor of Clostridium perfringens α-toxin for treatment of gas gangrene. Commun Med 6, 225 (2026). https://doi.org/10.1038/s43856-026-01503-y
Palabras clave: gangrena gaseosa, Clostridium perfringens, toxinas bacterianas, reposicionamiento de fármacos, caspofungina