Clear Sky Science · nl
Herbestemming van caspofungine als kleinmolecuulremmer van Clostridium perfringens α-toxine voor de behandeling van gasgangreen
Een gevaarlijke infectie die beter behandelbare opties nodig heeft
Gasgangreen is een snel voortschrijdende, vaak dodelijke infectie die kan volgen op ernstige verwondingen of soms plotseling verschijnt zonder duidelijke aanleiding. De ziekte wordt veroorzaakt door de bacterie Clostridium perfringens, die krachtige toxines uitscheidt die spierweefsel verscheuren, de bloedtoevoer afsnijden en het lichaam binnen enkele uren overweldigen. De huidige behandelingen — spoedchirurgie, antibiotica en soms zuurstoftherapie — kunnen levens redden, maar remmen niet altijd tijdig de schade. Deze studie onderzoekt of een bestaand antifungaal middel, caspofungine, kan worden herbestemd om het belangrijkste toxine van de bacterie direct uit te schakelen en zo een snellere manier te bieden om patiënten te beschermen.
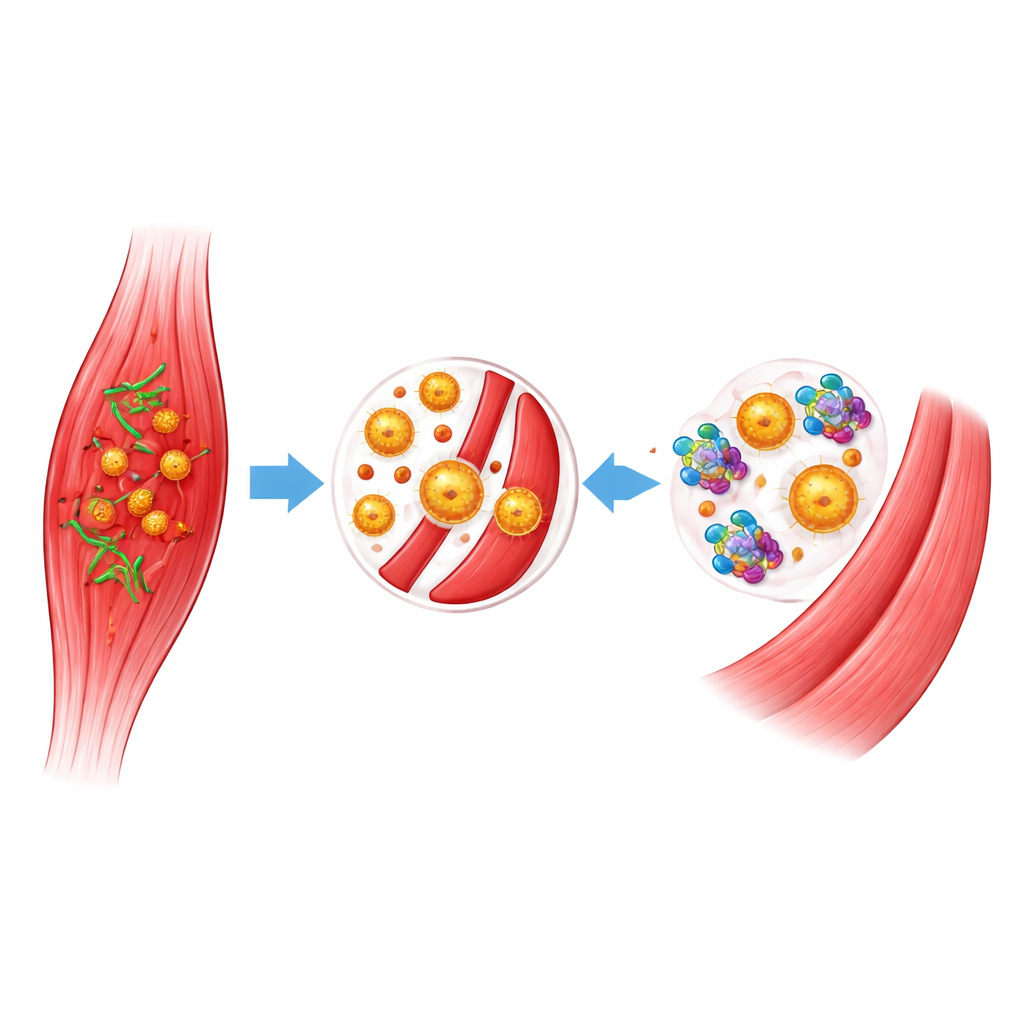
Het bacteriële toxine dat spieren en bloedtoevoer verwoest
C. perfringens produceert meerdere toxines, maar één ervan, het alpha-toxine, speelt een centrale rol bij gasgangreen. Het alpha-toxine valt belangrijke vetten in celmembranen aan, doodt spier- en bloedvatcellen en helpt de bacterie zich te verspreiden. Het verstoort ook het immuunsysteem door witte bloedcellen en bloedplaatjes te laten samenklonteren, waardoor kleine bloedvaten worden geblokkeerd en afweercellen de geïnfecteerde plek niet kunnen bereiken. In de loop van de tijd veroorzaakt deze verstoring van de circulatie ernstige spierverslapping, shock en orgaanfalen. Omdat alpha-toxine zo’n grote rol speelt in deze verwoesting, is het blokkeren van zijn activiteit een aantrekkelijke strategie om de ziekte te vertragen of te stoppen.
Op zoek naar nieuwe toepassingen voor oude medicijnen
In plaats van vanaf nul een nieuw geneesmiddel te ontwikkelen, selecteerden de onderzoekers 764 medicijnen die al voor menselijk gebruik zijn goedgekeurd. Ze testten elk middel op het vermogen om de enzymatische activiteit van het alpha-toxine te remmen, met focus op hoe goed het het toxine kon verhinderen een sleutelvetstof in membranen af te breken. Uit deze grote bibliotheek verminderden 21 verbindingen de activiteit van het toxine aanzienlijk. Het team voerde vervolgens een tweede, zwaardere test uit met menselijke bloedvatcellen in kweek. Slechts één geneesmiddel, micafungine — een in het ziekenhuis gebruikt antifungaal middel — beschermde deze cellen tegen door het toxine veroorzaakte celdood. Een verwant antifungaal middel, caspofungine, werd daarna aan de experimenten toegevoegd omdat het een vergelijkbare structuur en klinisch profiel heeft.
Hoe twee antifungale middelen zich aan het toxine binden
Zowel micafungine als caspofungine bleken het vermogen van alpha-toxine om menselijke bloedvatcellen te doden en de afgifte van ontstekingsmoleculen te stimuleren, te blokkeren. Computer‑modellering suggereerde waarom: de geneesmiddelen lijken zich in een holte van het toxine te nestelen waar normaal gesproken zijn natuurlijke vetachtige doelmolecuul zou binden. De stijve zijgroep van micafungine past diep in deze pocket en vormt veel nauwe contacten, terwijl de flexibelere zijgroep van caspofungine ondieper zit en minder sterke bindingen aangaat. Deze verschillen komen overeen met laboratoriummetingen die tonen dat micafungine de sterkere remmer is van één van de activiteiten van het toxine. Toch gedraagt caspofungine zich anders op een ander functioneel onderdeel van het enzym, wat erop wijst dat subtiele variaties in hoe elk geneesmiddel aan het toxine dockt, diens werking kunnen hervormen.
Van cellen naar muizen: bescherming testen in levende dieren
Een toxine blokkeren in een schaal is belangrijk, maar de echte toets is of die bescherming ook in een levend dier standhoudt. Wanneer muizen zuiver alpha-toxine kregen toegediend, stierven de meeste onbehandelde dieren binnen een dag. Muizen die caspofungine samen met het toxine ontvingen, overleefden daarentegen grotendeels, wat aantoont dat het middel de dodelijke effecten van het toxine in het lichaam kan dempen. Verrassend genoeg verbeterde micafungine, ondanks dat het in reageerbuizen een sterkere remmer is, de overleving bij dezelfde dosis niet. De auteurs suggereren dat kleine verschillen in hoe sterk deze geneesmiddelen aan bloedproteïnen binden — en daarmee hoeveel vrij middel beschikbaar is om het toxine te neutraliseren — deze kloof kunnen verklaren. In een tweede model, waarbij muizen in de beenspier werden geïnfecteerd met levende C. perfringens, vertraagde caspofungine de dood significant en verminderde het spierschade. In combinatie met de standaardantibioticum clindamycine verbeterden zowel overleving als spierbehoud verder.
Wat dit kan betekenen voor de behandeling van gasgangreen
De studie concludeert dat caspofungine, een middel dat al klinisch wordt gebruikt voor ernstige schimmelinfecties, veelbelovend is als een toxinegerichte therapie voor gasgangreen. In plaats van de bacterie direct te doden, ontwapent caspofungine hun belangrijkste wapen, waardoor standaardantibiotica en chirurgie meer tijd krijgen om te werken en spieren en bloedvaten worden beschermd tegen catastrofale schade. Omdat caspofungine al is goedgekeurd en breed beschikbaar is, zou het in principe sneller naar klinische proeven voor gasgangreen kunnen worden gebracht dan een volledig nieuw middel. Algemeen laat het werk zien hoe het screenen van bestaande geneesmiddelenbibliotheken kleinmoleculen kan aan het licht brengen die bacteriële toxines neutraliseren, en zo de deur opent naar een nieuwe klasse behandelingen die gericht zijn op het blokkeren van schade in plaats van alleen het aanvallen van microben.
Bronvermelding: Takehara, M., Homma, Y., Ishihara, T. et al. Repurposing caspofungin as a small-molecule inhibitor of Clostridium perfringens α-toxin for treatment of gas gangrene. Commun Med 6, 225 (2026). https://doi.org/10.1038/s43856-026-01503-y
Trefwoorden: gasgangreen, Clostridium perfringens, bacteriële toxines, herbestemming van geneesmiddelen, caspofungine