Clear Sky Science · fr
Réaffectation du caspofongine en tant qu’inhibiteur de petite molécule de l’α-toxine de Clostridium perfringens pour le traitement de la gangrène gazeuse
Une infection dangereuse qui réclame de meilleurs traitements
La gangrène gazeuse est une infection fulgurante et souvent mortelle qui peut suivre des blessures graves ou parfois survenir sans avertissement. Elle est causée par la bactérie Clostridium perfringens, qui libère des toxines puissantes qui déchirent le muscle, coupent l’apport sanguin et submergent l’organisme en quelques heures. Les traitements actuels — chirurgie d’urgence, antibiotiques et parfois oxygénothérapie — peuvent sauver des vies, mais n’empêchent pas toujours les dégâts à temps. Cette étude examine si un antifongique existant, la caspofongine, pourrait être réaffecté pour désarmer directement la principale toxine de la bactérie et offrir un moyen nouveau et plus rapide de protéger les patients.
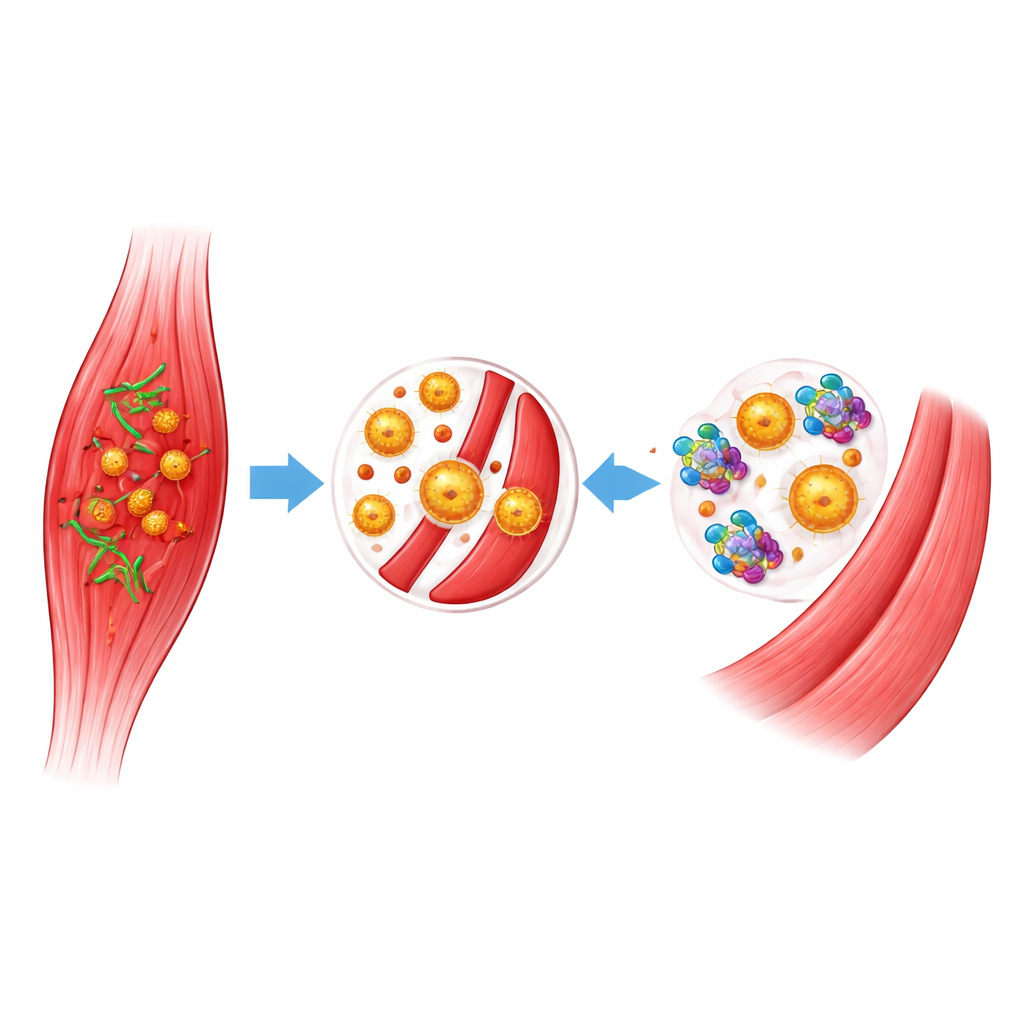
La toxine bactérienne qui détruit le muscle et la circulation
C. perfringens produit plusieurs toxines, mais l’alpha-toxine joue un rôle central dans la gangrène gazeuse. L’alpha-toxine attaque des lipides clés des membranes cellulaires, tuant les cellules musculaires et vasculaires et facilitant la propagation bactérienne. Elle perturbe aussi le système immunitaire en provoquant l’agrégation des globules blancs et des plaquettes, obstruant les petits vaisseaux et empêchant les cellules défensives d’atteindre le site infecté. Avec le temps, cette asphyxie de la circulation provoque une nécrose musculaire sévère, un état de choc et une défaillance d’organes. Parce que l’alpha-toxine est l’un des moteurs principaux de cette destruction, bloquer son activité est une stratégie prometteuse pour ralentir ou arrêter la maladie.
À la recherche d’anciens médicaments pour une nouvelle utilisation
Plutôt que de partir de zéro pour inventer un nouveau médicament, les chercheurs ont criblé 764 médicaments déjà approuvés pour l’usage humain. Ils ont testé chacun pour sa capacité à bloquer l’activité enzymatique de l’alpha-toxine, en se concentrant sur sa capacité à empêcher la toxine de cliver un lipide membranaire clé. De cette vaste bibliothèque, 21 composés ont considérablement réduit l’activité de la toxine. L’équipe a ensuite mené un second test plus exigeant utilisant des cellules de vaisseaux sanguins humaines en culture. Un seul médicament, la micafongine — un antifongique utilisé en milieu hospitalier — a protégé ces cellules de la mort induite par la toxine. Un antifongique apparenté, la caspofongine, a ensuite été intégré aux expériences en raison de sa structure et de son profil clinique semblables.
Comment deux antifongiques s’accrochent à la toxine
La micafongine et la caspofongine se sont avérées capables d’empêcher l’alpha-toxine de tuer les cellules de vaisseaux sanguins humaines et de provoquer la libération de médiateurs inflammatoires. La modélisation informatique suggère pourquoi : les médicaments semblent se loger dans une cavité de la toxine où sa cible lipidique naturelle se lie normalement. La chaîne latérale rigide de la micafongine s’insère profondément dans cette poche, formant de nombreux contacts serrés, tandis que la chaîne latérale plus flexible de la caspofongine siège plus superficiellement et forme moins de liaisons fortes. Ces différences correspondent aux mesures de laboratoire montrant que la micafongine est le bloqueur le plus puissant pour l’une des activités de la toxine. Pourtant la caspofongine se comporte différemment sur un autre volet de la fonction enzymatique, suggérant que de subtiles variations dans la façon dont chaque médicament s’ancre à la toxine peuvent modifier son comportement.
Des cellules aux souris : tester la protection chez des animaux vivants
Bloquer une toxine en culture est important, mais le véritable test est de savoir si cette protection résiste dans un organisme vivant. Lorsque des souris ont reçu de l’alpha-toxine purifiée, la plupart des animaux non traités sont morts en moins d’une journée. Les souris ayant reçu de la caspofongine en même temps que la toxine ont toutefois majoritairement survécu, montrant que le médicament peut atténuer les effets létaux de la toxine in vivo. De manière surprenante, la micafongine, bien qu’étant un bloqueur plus puissant in vitro, n’a pas amélioré la survie à la même dose. Les auteurs suggèrent que de petites différences dans l’affinité de liaison de ces médicaments aux protéines sanguines — et donc dans la quantité de médicament libre disponible pour neutraliser la toxine — pourraient expliquer cet écart. Dans un second modèle, où des souris ont été infectées au muscle de la patte par C. perfringens vivant, la caspofongine a significativement retardé la mort et réduit les lésions musculaires. En association avec l’antibiotique standard clindamycine, la survie et la préservation musculaire se sont encore améliorées.
Ce que cela pourrait signifier pour le traitement de la gangrène gazeuse
L’étude conclut que la caspofongine, un médicament déjà utilisé en clinique pour des infections fongiques graves, présente un fort potentiel comme thérapie ciblant la toxine pour la gangrène gazeuse. Plutôt que de tuer directement les bactéries, la caspofongine désarme leur arme principale, donnant aux antibiotiques et à la chirurgie plus de temps pour agir et aidant à protéger le muscle et les vaisseaux sanguins d’une lésion catastrophique. Parce que la caspofongine est déjà approuvée et largement disponible, elle pourrait, en principe, être rapidement orientée vers des essais cliniques pour la gangrène gazeuse, plus vite qu’un nouveau composé. Plus largement, ce travail montre comment le criblage de bibliothèques de médicaments existantes peut révéler des petites molécules qui neutralisent des toxines bactériennes, ouvrant la voie à une nouvelle classe de traitements focalisés sur le blocage des dommages plutôt que sur l’attaque des microbes.
Citation: Takehara, M., Homma, Y., Ishihara, T. et al. Repurposing caspofungin as a small-molecule inhibitor of Clostridium perfringens α-toxin for treatment of gas gangrene. Commun Med 6, 225 (2026). https://doi.org/10.1038/s43856-026-01503-y
Mots-clés: gangrène gazeuse, Clostridium perfringens, toxines bactériennes, réaffectation de médicaments, caspofongine