Clear Sky Science · pl
Predykcja uczenia maszynowego i stratyfikacja ryzyka 12-miesięcznego spadku funkcji poznawczych w chorobie Alzheimera z wykorzystaniem rutynowych danych klinicznych i MRI
Dlaczego przewidywanie pogorszenia pamięci ma znaczenie
Choroba Alzheimera stopniowo pozbawia ludzi pamięci i zdolności myślenia, ale tempo pogorszenia nie jest jednakowe u wszystkich. Niektórzy pacjenci tracą kilka punktów w prostych testach poznawczych w ciągu roku, podczas gdy inni pozostają względnie stabilni. Możliwość określenia już przy rozpoznaniu, kto szybko się pogorszy, mogłaby pomóc lekarzom zaplanować wizyty, wspierać rodziny oraz wybrać pacjentów do badań klinicznych nowych terapii. W tym badaniu sprawdzono, czy informacje, które wiele poradni pamięci już zbiera — krótkie testy poznawcze i rutynowe badania mózgu — można połączyć z nowoczesnymi metodami komputerowymi, aby przewidzieć, kto pogorszy się w ciągu następnych 12 miesięcy.
Kogo objęto badaniem i co mierzono
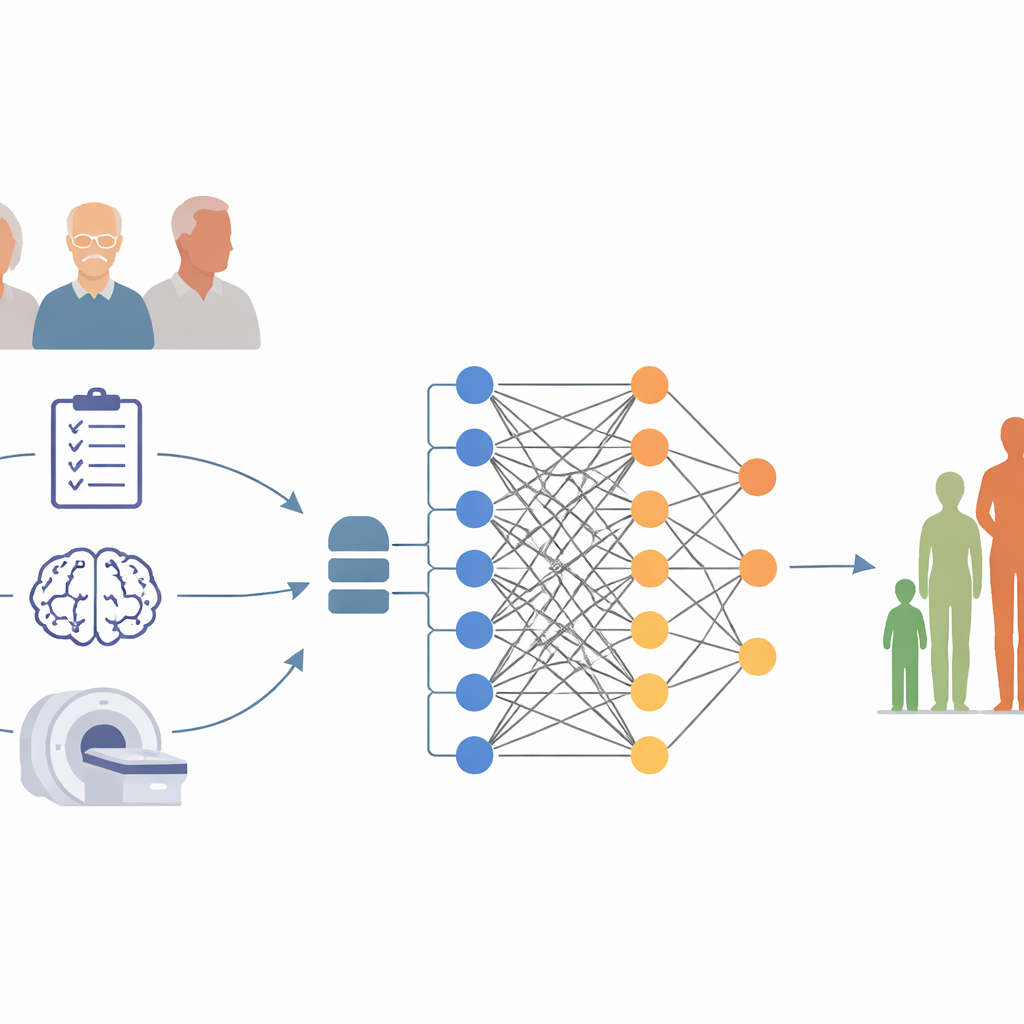
Naukowcy wykorzystali dane z Alzheimer’s Disease Neuroimaging Initiative, wieloletniego projektu śledzącego osoby z zaburzeniami pamięci za pomocą ustandaryzowanych testów i obrazowania mózgu. Skoncentrowali się na 306 uczestnikach, którzy mieli już rozpoznanie choroby Alzheimera i którzy wykonali test pamięci zwany Mini-Mental State Examination (MMSE) na początku badania oraz ponownie po roku. Spadek o trzy lub więcej punktów w MMSE w ciągu 12 miesięcy uznano za istotne pogorszenie. Na początku każdy uczestnik podawał podstawowe dane, takie jak wiek, płeć i lata wykształcenia, wypełniał kilka szczegółowych kwestionariuszy dotyczących funkcji poznawczych i codziennego funkcjonowania oraz poddawał się badaniu MRI mózgu, które mierzyło wielkość kluczowych regionów mózgu zaangażowanych w pamięć.
Jak zbudowano modele komputerowe
Aby sprawdzić, czy można przewidzieć pogorszenie w krótkim terminie, zespół zbudował i porównał dwa typy narzędzi prognostycznych. Pierwszym była prosta formuła statystyczna wykorzystująca tylko kilka przyjaznych dla kliniki miar: wiek, płeć oraz wyniki w dwóch standardowych testach poznawczych. Drugim był bardziej elastyczny model uczenia maszynowego znany jako random forest, który mógł uwzględnić pełen zestaw wyników klinicznych wraz z miarami z MRI, takimi jak objętość hipokampa i rozmiar przestrzeni wypełnionych płynem. Dane były wielokrotnie dzielone na zestawy treningowe i testowe, tak aby wynik każdego uczestnika był przewidywany przez model, który wcześniej nie „widział” tej osoby, co naśladuje działanie narzędzia wobec nowych pacjentów.
Jak dobrze modele przewidywały pogorszenie
Około 43% uczestników doświadczyło istotnego spadku MMSE w ciągu 12 miesięcy. Oba podejścia wypadły lepiej niż przypadek w identyfikowaniu tych osób. Prosty model kliniczny osiągnął poziom wydajności zwykle uznawany za „umiarkowany” dla narzędzi predykcyjnych w medycynie. Model random forest wypadł nieco lepiej ogólnie i, co ważne, wykazał większy „czysty zysk” w szerokim zakresie praktycznych progów ryzyka. Czysty zysk to sposób ważenia poprawnych i błędnych przewidywań w odniesieniu do konsekwencji działania na ich podstawie — na przykład decyzji, którzy pacjenci powinni być częściej monitorowani lub kierowani do intensywniejszej opieki. Chociaż bardziej złożony model nie był doskonały i wykazywał pewne oznaki przeuczenia, konsekwentnie dostarczał bardziej użytecznych wskazówek niż strategie zakładające, że wszyscy pacjenci się pogorszą lub że nikt się nie pogorszy.
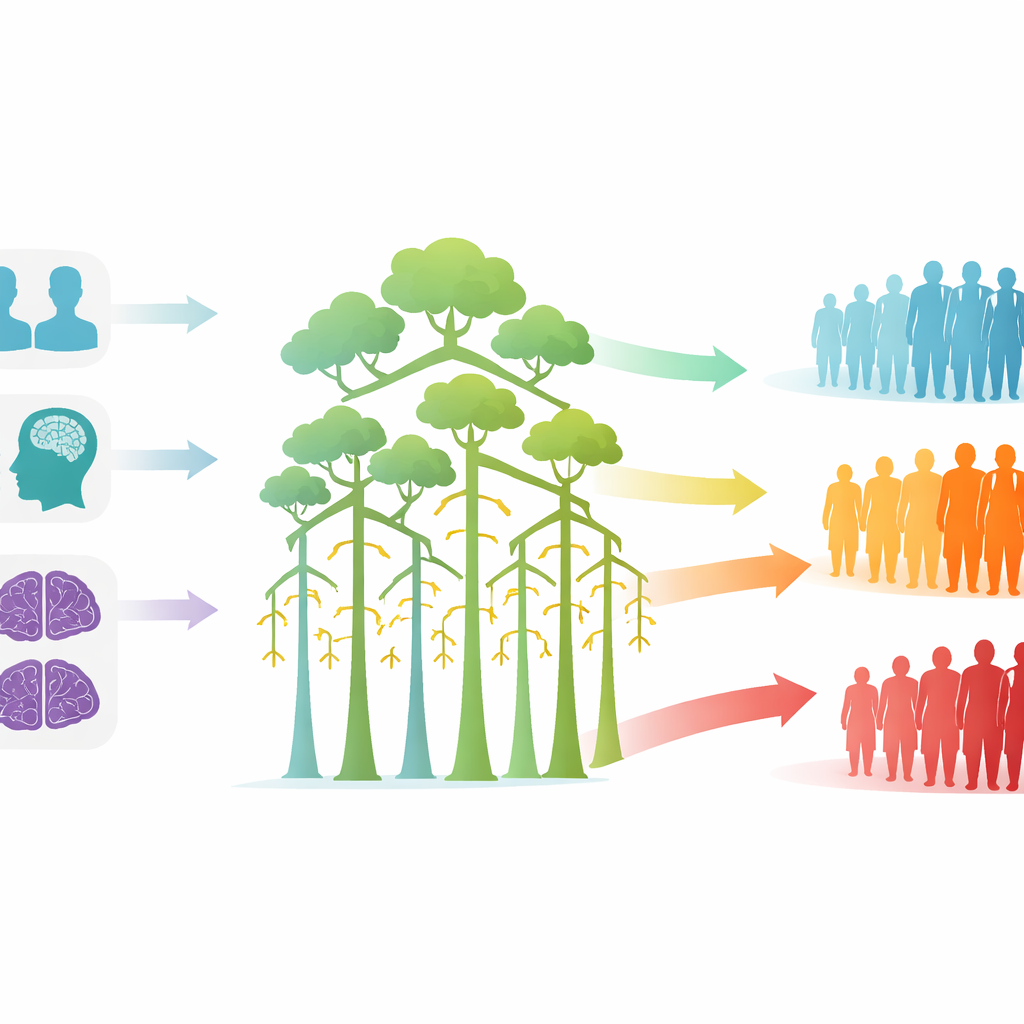
Przekształcanie wyników na niskie, średnie i wysokie ryzyko
Aby ułatwić wykorzystanie wyników w poradniach, badacze przetłumaczyli wyjście modelu na trzy proste pasma ryzyka. Osoby, których przewidywane prawdopodobieństwo pogorszenia było poniżej jednej czwartej, tworzyły grupę niskiego ryzyka; tylko około jedna na osiem z nich faktycznie się pogorszyła, a ich średnie wyniki testów pozostały niemal niezmienione po roku. Osoby ze środkowego pasma miały mniej więcej jedno na trzy szanse pogorszenia i średnio straciły około półtora punktu w MMSE. Grupa wysokiego ryzyka, z przewidywanym prawdopodobieństwem powyżej jednej połowy, wykazała pogorszenie u około dwóch na trzech pacjentów i przeciętną utratę ponad czterech punktów MMSE. Ten wyraźny, stopniowy wzorzec sugeruje, że prawdopodobieństwa modelu można przekształcić w praktyczne kategorie, które mogą kierować częstotliwością wizyt i wskazywać, którzy pacjenci powinni być priorytetowani do badań klinicznych lub dodatkowych badań.
Co to oznacza dla pacjentów i poradni
Badanie pokazuje, że łącząc rutynowe testy pamięci ze standardowymi skanami MRI mózgu i analizując je nowoczesnymi metodami komputerowymi, można z umiarkowaną dokładnością oszacować indywidualne ryzyko zauważalnego pogorszenia u pacjenta z chorobą Alzheimera w ciągu następnego roku. Choć narzędzie wymaga jeszcze weryfikacji i dostosowania w różnych szpitalach oraz w bardziej zróżnicowanych populacjach, zanim zostanie zastosowane w codziennej opiece, wskazuje na przyszłość, w której harmonogramy kontroli i kwalifikacja do badań będą dopasowane do prawdopodobnej trajektorii każdej osoby, zamiast traktować wszystkich pacjentów, jakby choroba rozwijała się u nich w tym samym tempie.
Cytowanie: Geng, Y., Zhang, H. Machine-learning prediction and risk stratification of 12-month cognitive decline in Alzheimer’s disease using routine clinical and MRI data. Sci Rep 16, 12227 (2026). https://doi.org/10.1038/s41598-026-43321-1
Słowa kluczowe: choroba Alzheimera, spadek funkcji poznawczych, uczenie maszynowe, rezonans magnetyczny mózgu, stratyfikacja ryzyka