Clear Sky Science · de
Vorhersage mittels maschinellen Lernens und Risikostratifizierung des kognitiven Abfalls über 12 Monate bei Alzheimer durch routinemäßige klinische Daten und MRT
Warum die Vorhersage des Gedächtnisverlusts wichtig ist
Die Alzheimer-Krankheit raubt Menschen langsam ihr Gedächtnis und Denkvermögen, doch nicht alle verschlechtern sich im gleichen Tempo. Manche Patientinnen und Patienten verlieren innerhalb eines Jahres mehrere Punkte bei einfachen Gedächtnistests, andere bleiben weitgehend stabil. Wenn man bereits zum Zeitpunkt der Diagnose vorhersagen könnte, wer sich schnell verschlechtert, würde das Ärztinnen und Ärzten helfen, Besuchsintervalle zu planen, Familien zu unterstützen und geeignete Teilnehmer für klinische Studien auszuwählen. Diese Studie untersucht, ob Informationen, die viele Gedächtnisambulanzen bereits erheben – kurze kognitive Tests und routinemäßige Hirnscans – in Kombination mit modernen Computerverfahren genutzt werden können, um vorherzusagen, wer innerhalb der nächsten 12 Monate abnehmen wird.
Wer untersucht wurde und was gemessen wurde
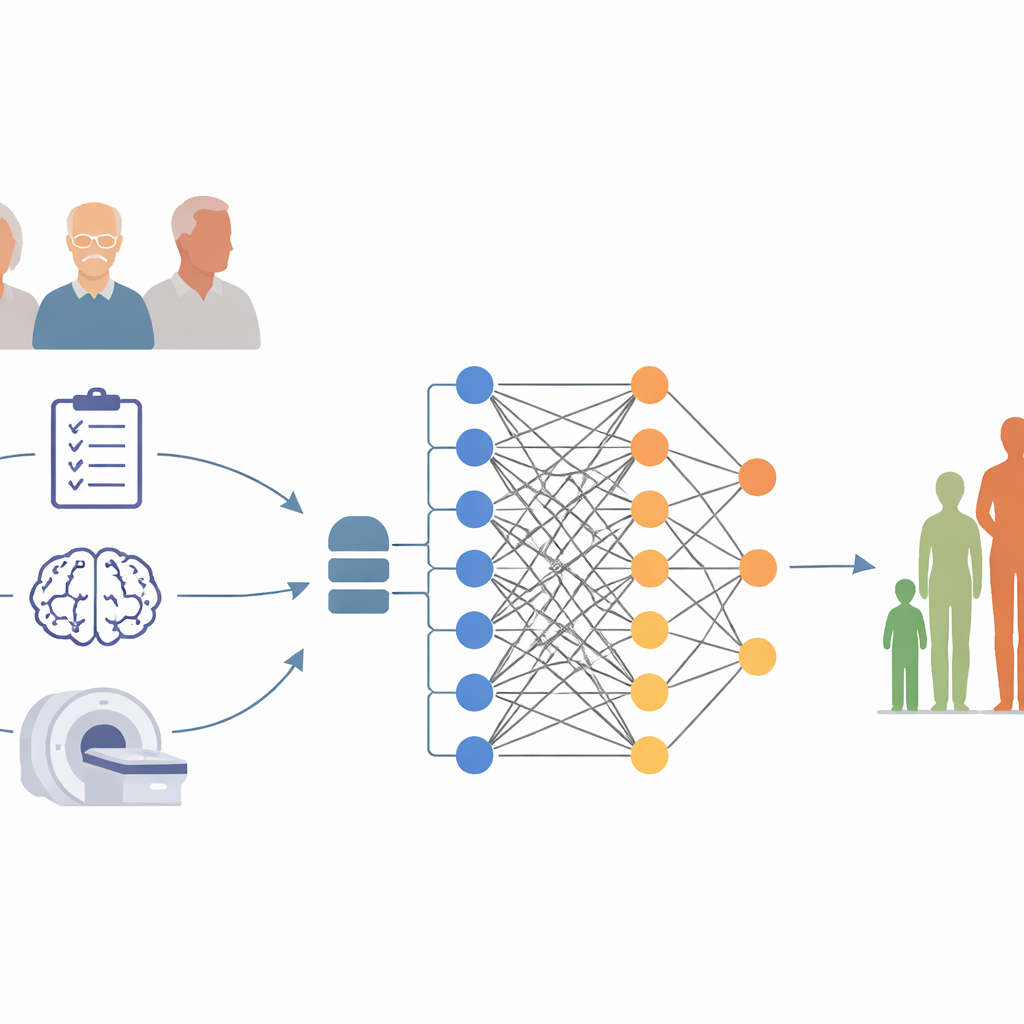
Die Forschenden nutzten Daten der Alzheimer’s Disease Neuroimaging Initiative, eines langjährigen Projekts, das Menschen mit Gedächtnisproblemen mit standardisierten Tests und Bildgebung begleitet. Sie konzentrierten sich auf 306 Teilnehmende, bei denen bereits eine Alzheimer-Diagnose vorlag und die zu Studienbeginn sowie ein Jahr später einen Gedächtnistest namens Mini-Mental State Examination (MMSE) absolviert hatten. Ein Abfall von drei oder mehr MMSE-Punkten innerhalb von 12 Monaten wurde als bedeutsamer Rückgang gewertet. Zu Beginn gab jede Person Basisinformationen wie Alter, Geschlecht und Bildungsjahre an, füllte mehrere detaillierte Fragebögen zu kognitiven Fähigkeiten und Alltagstätigkeiten aus und unterzog sich einer Hirn-MRT, die die Größe wichtiger für das Gedächtnis relevanter Hirnregionen maß.
Wie die Computermodelle erstellt wurden
Um zu prüfen, ob ein kurzfristiger Abfall vorhergesagt werden kann, entwickelten und verglichen die Forschenden zwei Typen von Vorhersagewerkzeugen. Das erste war eine einfache statistische Formel, die nur eine Handvoll klinikfreundlicher Maße nutzte: Alter, Geschlecht und die Ergebnisse zweier gängiger kognitiver Tests. Das zweite war ein flexibleres Modell des maschinellen Lernens, bekannt als Random Forest, das das gesamte Set klinischer Werte zusammen mit MRT-Messungen wie Hippocampusvolumen und der Größe der mit Flüssigkeit gefüllten Räume im Gehirn berücksichtigen konnte. Die Daten wurden wiederholt in Trainings- und Testmengen aufgeteilt, sodass das Ergebnis jeder Person von einem Modell vorhergesagt wurde, das diese Person noch nicht „gesehen“ hatte – ein Vorgehen, das das Verhalten des Werkzeugs bei neuen Patientinnen und Patienten nachahmt.
Wie gut die Modelle den Abfall vorhersagten
Etwa 43 % der Teilnehmenden erlebten innerhalb von 12 Monaten einen bedeutsamen MMSE-Abfall. Beide Ansätze schnitten besser ab als reiner Zufall, diese Personen zu identifizieren. Das einfache klinische Modell erreichte ein Leistungsniveau, das bei medizinischen Vorhersagewerkzeugen typischerweise als „moderat" eingestuft wird. Das Random-Forest-Modell war insgesamt etwas leistungsfähiger und zeigte vor allem über einen weiten Bereich praktischer Risikoschwellen einen größeren „Nettonutzen“. Nettonutzen ist eine Methode, richtige und falsche Vorhersagen gegen die Folgen von Handlungen abzuwägen – etwa die Entscheidung, welche Patientinnen und Patienten häufiger überwacht oder für intensivere Versorgung in Betracht gezogen werden sollten. Obwohl das komplexere Modell nicht perfekt war und Anzeichen von Überanpassung zeigte, lieferte es beständig nützlichere Hinweise als Strategien, die davon ausgingen, entweder würden alle abnehmen oder niemand würde abnehmen.
Umwandlung der Ergebnisse in niedriges, mittleres und hohes Risiko
Um die Ergebnisse für Kliniken leichter nutzbar zu machen, übersetzten die Forschenden die Modellausgabe in drei einfache Risikogruppen. Personen, deren vorhergesene Wahrscheinlichkeit für einen Abfall unter einem Viertel lag, bildeten die Niedrigrisikogruppe; von ihnen nahm nur etwa eine von acht tatsächlich ab, und ihre durchschnittlichen Testergebnisse blieben nach einem Jahr nahezu unverändert. Die Mittelgruppierten hatten etwa eine Eins-zu-Drei-Chance auf Abfall und verloren im Mittel rund anderthalb MMSE-Punkte. Die Hochrisikogruppe mit vorhergesagten Wahrscheinlichkeiten über der Hälfte zeigte bei etwa zwei von drei Patienten einen Abfall und einen mittleren Verlust von mehr als vier MMSE-Punkten. Dieses klare stufenweise Muster legt nahe, dass sich die Modellwahrscheinlichkeiten in praktische Kategorien übersetzen lassen, die darüber informieren könnten, wie häufig Patientinnen und Patienten gesehen werden sollten und welche vorrangig für Studien oder zusätzliche Untersuchungen eingeplant werden könnten.
Was das für Patientinnen, Patienten und Kliniken bedeutet
Die Studie zeigt, dass sich durch die Kombination routinemäßiger Gedächtnistests mit standardmäßigen MRT-Aufnahmen und deren Analyse mit modernen Computerverfahren das Risiko eines merklichen Abfalls innerhalb des nächsten Jahres bei einzelnen Alzheimer-Patientinnen und -Patienten mäßig genau abschätzen lässt. Während das Werkzeug noch in verschiedenen Kliniken und vielfältigeren Populationen überprüft und angepasst werden muss, bevor es im Alltag eingesetzt wird, weist es auf eine Zukunft hin, in der Nachsorgeintervalle und Einschlusskriterien für Studien an die voraussichtliche Krankheitsentwicklung jeder einzelnen Person angepasst werden, statt alle Patientinnen und Patienten so zu behandeln, als würde die Erkrankung bei allen gleich schnell fortschreiten.
Zitation: Geng, Y., Zhang, H. Machine-learning prediction and risk stratification of 12-month cognitive decline in Alzheimer’s disease using routine clinical and MRI data. Sci Rep 16, 12227 (2026). https://doi.org/10.1038/s41598-026-43321-1
Schlüsselwörter: Alzheimer-Krankheit, kognitiver Abbau, maschinelles Lernen, Hirn-MRT, Risikostratifizierung