Clear Sky Science · pl
Interakcja kalretikuliny z IRE1α zależna od wapnia napędza dynamiczne fluktuacje aktywności IRE1α podczas przewlekłego stresu siateczki endoplazmatycznej
Jak komórki surfują po falach wewnętrznego stresu
W każdej komórce rozciąga się rozległa sieć pofałdowanych błon zwana siateczką endoplazmatyczną, która działa jak hala produkcyjna do tworzenia i przetwarzania białek. Gdy ta „fabryka” zostaje przeciążona, komórka stoi przed dylematem: naprawić i zaadaptować się albo wyłączyć się i zginąć. Badanie to pokazuje, że jeden z kluczowych czujników stresu w tej fabryce, białko IRE1α, nie działa jak prosty włącznik. Jego aktywność rośnie, maleje i znów rośnie falami — precyzyjnie regulowana przez jony wapnia i białko pomocnicze o nazwie kalretikulina. Zrozumienie tej subtelnej kontroli może rzucić światło na choroby, w których długotrwały stres komórkowy odgrywa istotną rolę, takie jak cukrzyca, nowotwory i neurodegeneracja.
Gdy fabryki białek ulegają przeciążeniu
W zdrowych komórkach świeże białka trafiają do siateczki endoplazmatycznej, gdzie są składane w precyzyjne kształty. Jeśli zbyt wiele niesfałdowanych białek zaczyna się kumulować, komórka doświadcza tzw. „stresu ER”. Aby sobie poradzić, uruchamia program ochronny znany jako odpowiedź na nieprawidłowo sfałdowane białka. Trzy strażniczki na błonie ER wykrywają problemy i przekazują sygnały do reszty komórki. Jedna z tych strażniczek, IRE1α, jest szczególnie ważna, ponieważ pomaga wzmocnić zdolność komórki do fałdowania i przetwarzania białek. Jednak jeśli stres jest zbyt silny lub trwa zbyt długo, ten sam system może się odwrócić i pchnąć komórkę ku autodestrukcji. Jak komórki zarządzają tą równowagą przy utrzymującym się, nieśmiertelnym stresie — to było kluczowe, nierozwiązane pytanie.
Sygnał stresowy, który pulsuje zamiast utrzymywać stały poziom
Naukowcy wystawili komórki ludzkie na działanie związków wywołujących różne poziomy stresu ER — łagodny, umiarkowany i silny — i śledzili, co się dzieje przez dwa dni. Mierzyli, jak mocno IRE1α jest aktywowany, badając jego modyfikacje chemiczne oraz przetwarzanie „partnera” będącego cząsteczką informacyjną, którą kontroluje. Przy stresie umiarkowanym i silnym zaobserwowali uderzający schemat „w górę‑w dół‑znowu w górę”: IRE1α stawał się silnie aktywny w ciągu kilku godzin, potem się wyciszał, a wiele godzin później znowu gwałtownie wzrastał. To nie był jednorazowy incydent ani cecha jednego typu komórek; podobne fale pojawiały się w kilku rodzajach komórek ludzkich i mysich. Dla porównania, inna gałąź sygnalizacji stresowej sprzyjająca śmierci komórki aktywowała się tylko w najdotkliwszych, śmiertelnych warunkach. Obserwacje te sugerują, że komórka stosuje dynamiczną, pulsującą strategię, aby przetrwać przy przewlekłym obciążeniu.
Przeciąganie liny między dwoma pomocnikami
Aby zrozumieć, co kontroluje te fale, zespół przeanalizował, które białka fizycznie łączą się z IRE1α podczas długotrwałego stresu. Odkryli wahadłową interakcję między dwoma pomocnikami ER. Jeden z nich, BIP, jest dobrze znany jako hamulec trzymający IRE1α w ryzach. Drugi, kalretikulina, zwykle pomaga w fałdowaniu określonych białek, ale tutaj okazała się nieoczekiwanym aktywatorem IRE1α. Przy utrzymującym się stresie uchwyt kalretikuliny na IRE1α narastał i słabł równolegle do aktywności IRE1α, podczas gdy wiązanie BIP wykazywało odwrotny wzorzec. Eksperymenty z oczyszczonymi białkami i komórkami inżynierowanymi potwierdziły, że kalretikulina i BIP konkurują bezpośrednio o ten sam czujnik: gdy jedno wiąże się silniej, drugie zostaje wypychane. Komórki pozbawione kalretikuliny nie rozwijały późnej „drugiej fali” aktywności IRE1α i były bardziej podatne na śmierć, co podkreśla rolę kalretikuliny jako partnera sprzyjającego przeżyciu.
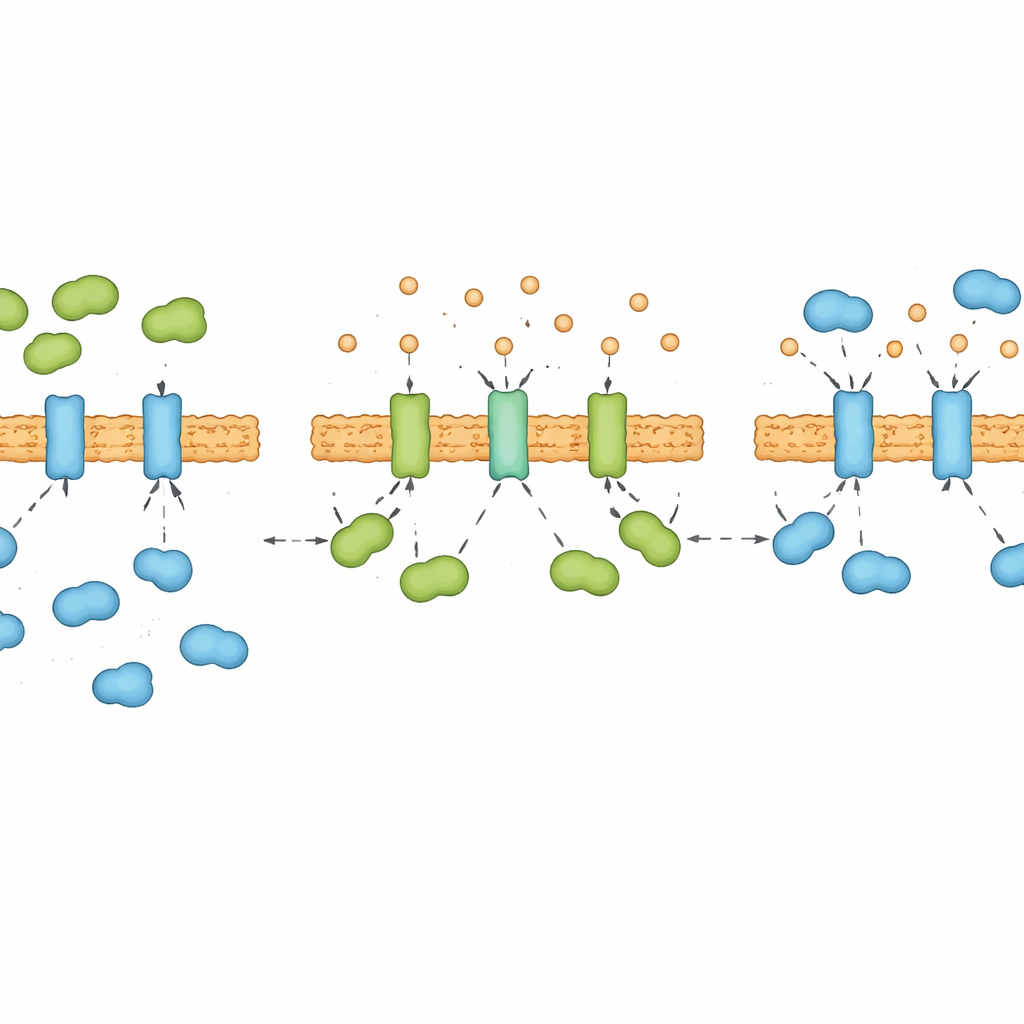
Wapń jako ukryty regulator sygnału stresowego
Kalretikulina jest też istotnym magazynem i partnerem wiążącym wapń w ER, a badacze stwierdzili, że to powiązanie jest kluczowe. Gdy w testach in vitro odjęto wapń od kalretikuliny, białko zmieniało konformację i wiązało IRE1α znacznie mocniej. Krótkotrwałe obniżenie poziomu wapnia wewnątrz ER żywych komórek szybko wzmocniło kontakt kalretikuliny z IRE1α, jeszcze zanim niesfałdowane białka zdążyły się zgromadzić. W ciągu wielu godzin przewlekłego stresu poziomy wapnia w ER same podążały rytmem „w dół‑w górę‑w dół”, który odzwierciedlał naprzemienną dominację kalretikuliny i BIP nad IRE1α. W istocie, wapń działa jak ukryty regulator, który przeobraża kalretikulinę i decyduje, czy to ona, czy BIP wygrywa przeciąganie liny o kontrolę nad czujnikiem stresu.
Dzienny rytm i cienka granica między przeżyciem a śmiercią
Zadziwiająco, ta sama choreografia między IRE1α, kalretikuliną, BIP i wapniem pojawia się w normalnej wątrobie mysiej, nawet bez sztucznego stresu. Tam aktywność IRE1α i jej partnerstwo z kalretikuliną przygasają i ponownie narastają w ciągu dnia, co sugeruje, że mechanizm ten pomaga zdrowym tkankom dostosowywać się do naturalnych cykli obciążenia, takich jak dobowe wahania metabolizmu. Podsumowując, praca przedstawia IRE1α nie jako prosty włącznik, lecz jako precyzyjnie dostrojony oscylator, kierowany przez wapniem ukształtowaną kalretikulę i jej rywalizację z BIP. Dla czytelnika nietechnicznego kluczowy wniosek jest taki, że komórki poddane długotrwałemu stresowi nie podejmują raz decyzji o życiu lub śmierci; wielokrotnie wracają do tej decyzji, wykorzystując wewnętrzne chemiczne fale, by zyskać czas, zaadaptować się i, gdy trzeba, poddać się.
Cytowanie: Cao, J., Zhao, X., Xu, Y. et al. Calcium-mediated calreticulin-IRE1α interaction drives dynamic fluctuation of IRE1α activity under chronic endoplasmic reticulum stress. Nat Commun 17, 4043 (2026). https://doi.org/10.1038/s41467-026-70679-7
Słowa kluczowe: stres siateczki endoplazmatycznej, odpowiedź na nieprawidłowo sfałdowane białka, sygnalizacja wapniowa, kalretikulina, przeżycie komórki