Clear Sky Science · de
Calciumvermittelte Calreticulin‑IRE1α‑Interaktion treibt die dynamische Schwankung der IRE1α‑Aktivität unter chronischem endoplasmatischem Retikulumstress
Wie Zellen die Wellen inneren Stresses reiten
Im Inneren jeder Zelle fungiert ein weit verzweigtes Netz aus gefalteten Membranen, das endoplasmatische Retikulum, wie eine Fabrikhalle zum Aufbau und zur Verarbeitung von Proteinen. Wird diese Fabrik überlastet, steht die Zelle vor einer Entscheidung: reparieren und anpassen oder herunterfahren und sterben. Diese Studie zeigt, dass ein Schlüssel‑Stresssensor in dieser Fabrik, ein Protein namens IRE1α, nicht einfach ein- oder ausgeschaltet wird. Vielmehr steigt seine Aktivität in Wellen an, fällt wieder ab und steigt erneut — fein abgestimmt durch Calciumionen und ein Helferprotein namens Calreticulin. Das Verständnis dieser subtilen Steuerung könnte Hinweise auf Krankheiten liefern, bei denen langfristiger zellulärer Stress eine zentrale Rolle spielt, etwa Diabetes, Krebs und Neurodegeneration.
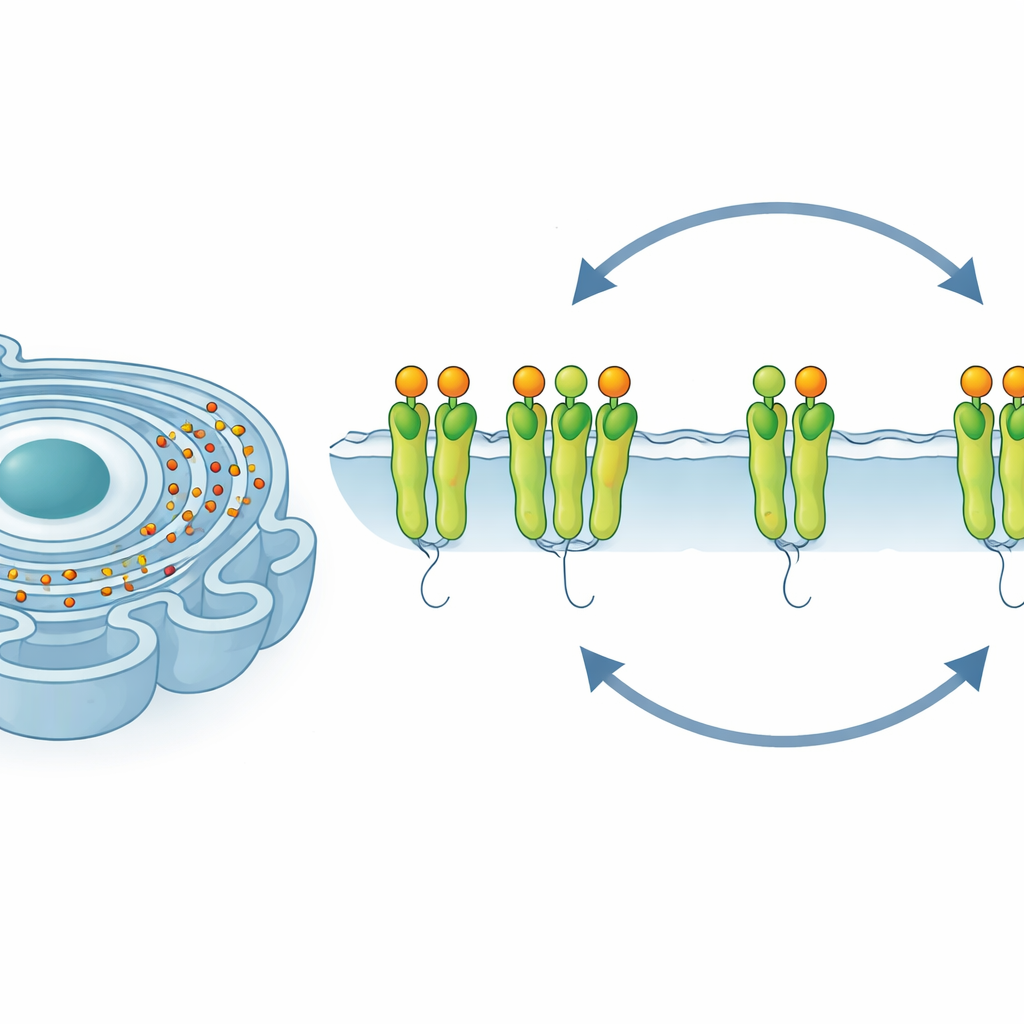
Wenn Proteinfabriken überlastet sind
In gesunden Zellen werden frisch synthetisierte Proteine in das endoplasmatische Retikulum eingespeist, wo sie in präzise Formen gefaltet werden. Haufen sich zu viele ungefaltete Proteine an, entsteht sogenannter „ER‑Stress“. Zur Bewältigung startet die Zelle ein Schutzprogramm, die Antwort auf fehlgefaltete Proteine. Drei Wächter in der ER‑Membran erkennen Probleme und leiten Signale an den Rest der Zelle weiter. Einer dieser Wächter, IRE1α, ist besonders wichtig, weil er die Fähigkeit der Zelle erhöht, Proteine zu falten und zu verarbeiten. Ist der Stress jedoch zu stark oder zu lang anhaltend, kann dasselbe System die Zelle stattdessen in Richtung Selbstzerstörung treiben. Wie Zellen dieses Gleichgewicht unter anhaltendem, nicht‑tödlichem Stress managen, war eine zentrale offene Frage.
Ein Stresssignal, das pulsiert statt konstant zu bleiben
Die Forscher setzten menschliche Zellen Chemikalien aus, die unterschiedliche Stärken von ER‑Stress hervorrufen — gering, mittel und stark — und verfolgten die Vorgänge über zwei Tage. Sie maßen, wie stark IRE1α aktiviert war, indem sie seine chemische Modifikation und die Verarbeitung einer von ihm gesteuerten Messenger‑RNA untersuchten. Unter mittlerem und starkem Stress zeigten sich auffällige „auf‑runter‑auf“‑Muster: IRE1α wurde innerhalb weniger Stunden stark aktiv, beruhigte sich später und schoss viele Stunden danach wieder in die Höhe. Dies war kein einmaliges Ereignis oder eine Eigenart eines einzelnen Zelltyps; ähnliche Wellen traten in mehreren menschlichen und murinen Zellarten auf. Im Gegensatz dazu wurde ein anderer Stresszweig, der den Zelltod fördert, nur unter den härtesten, tödlichen Bedingungen wieder aktiv. Diese Beobachtungen legen nahe, dass die Zelle eine dynamische, pulsierende Strategie nutzt, um unter chronischer Belastung zu überleben.
Das Tauziehen zwischen zwei Helfern
Um zu verstehen, was diese Wellen steuert, untersuchte das Team, welche Proteine bei langfristigem Stress physisch an IRE1α andocken. Sie entdeckten eine Wippe zwischen zwei ER‑Hilfsproteinen. Eines, BIP, ist bekannt als Bremse, die IRE1α in Schach hält. Das andere, Calreticulin, hilft normalerweise beim Falten bestimmter Proteine, entpuppte sich hier jedoch als unerwarteter Aktivator von IRE1α. Unter anhaltendem Stress stieg und fiel die Bindung von Calreticulin an IRE1α im Einklang mit der IRE1α‑Aktivität, während die Bindung von BIP das entgegengesetzte Muster zeigte. Experimente mit gereinigten Proteinen und gentechnisch veränderten Zellen bestätigten, dass Calreticulin und BIP direkt um denselben Sensor konkurrieren: Bindet das eine stärker, wird das andere verdrängt. Zellen ohne Calreticulin schafften die späte „zweite Welle“ der IRE1α‑Aktivität nicht und neigten eher zum Zelltod, was die Rolle von Calreticulin als pro‑überlebensfördernder Partner unterstreicht.
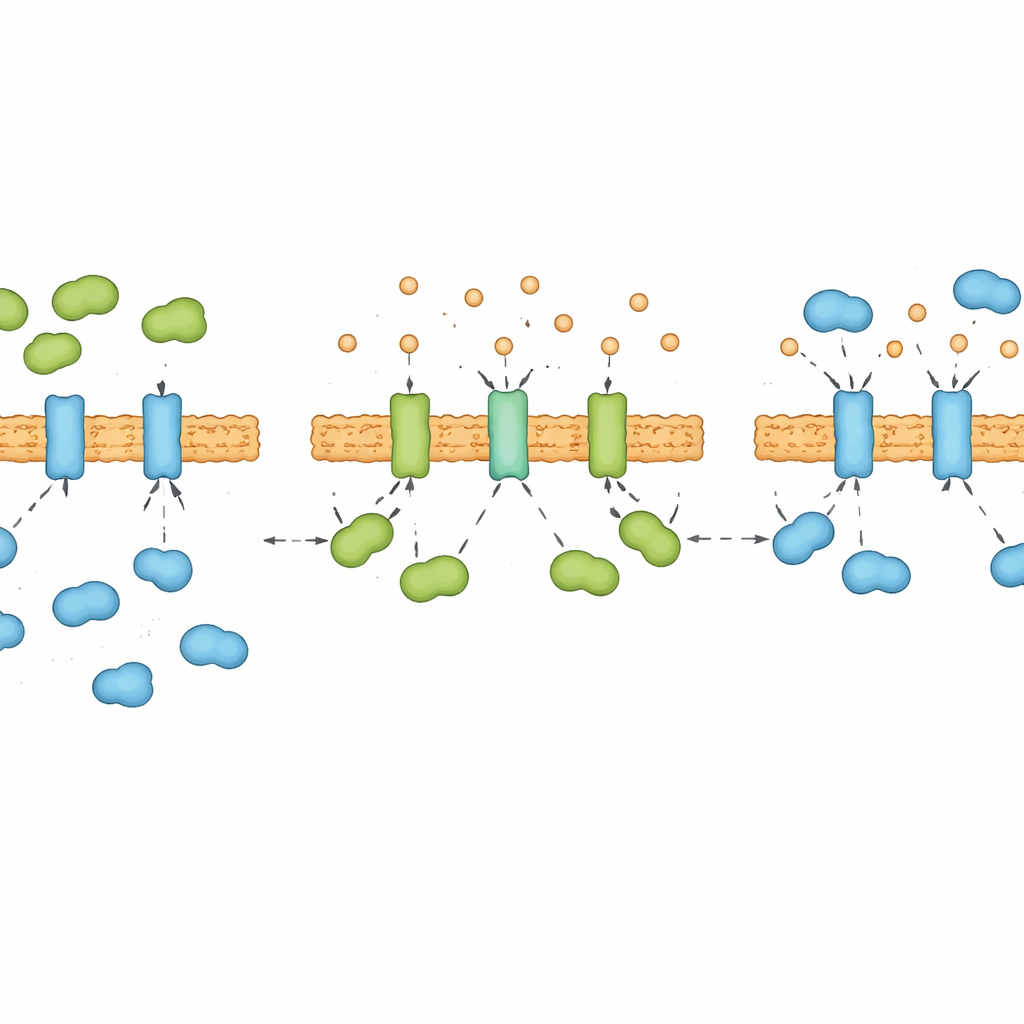
Calcium als versteckter Regler der Stress‑Signalgebung
Calreticulin ist zudem eine wichtige Speicher‑ und Bindepartnerin für Calcium im ER, und die Forscher stellten fest, dass diese Verbindung entscheidend ist. Wurde Calcium in Reagenzglasversuchen aus Calreticulin entfernt, änderte das Protein seine Form und band IRE1α deutlich fester. Kurzzeitiges Absenken der Calciumspiegel im ER lebender Zellen verstärkte rasch die Kontaktaufnahme von Calreticulin mit IRE1α, noch bevor sich ungefaltete Proteine ansammeln konnten. Über viele Stunden chronischen Stresses zeigten die ER‑Calciumspiegel selbst einen „runter‑hoch‑runter“‑Rhythmus, der die wechselnde Dominanz von Calreticulin und BIP an IRE1α spiegelte. Im Wesentlichen wirkt Calcium als versteckter Regler, der Calreticulin umgestaltet und darüber entscheidet, ob Calreticulin oder BIP das Tauziehen um die Kontrolle des Stresssensors gewinnt.
Tagesrhythmen und die schmale Grenze zwischen Überleben und Tod
Bemerkenswerterweise tritt derselbe Tanz zwischen IRE1α, Calreticulin, BIP und Calcium auch in der normalen Leber von Mäusen auf, selbst ohne künstlichen Stress. Dort schwankt die Aktivität von IRE1α und seine Partnerschaft mit Calreticulin im Tagesverlauf, was darauf hindeutet, dass dieser Mechanismus gesunden Geweben hilft, sich an natürliche Zyklusmuster der Arbeitsbelastung anzupassen, etwa tägliche Stoffwechselschwankungen. Zusammengenommen zeichnen die Ergebnisse IRE1α nicht als einfachen Ein/Aus‑Schalter, sondern als fein abgestimmten Oszillator, gesteuert von calciumgeformtem Calreticulin und dessen Rivalität mit BIP. Für Laien lautet die zentrale Botschaft: Zellen, die langfristigem Stress ausgesetzt sind, treffen nicht nur einmalig die Entscheidung zwischen Leben und Tod; sie überprüfen diese Entscheidung wiederholt und nutzen dabei innere chemische Wellen, um Zeit zu gewinnen, sich anzupassen und, falls nötig, zu kapitulieren.
Zitation: Cao, J., Zhao, X., Xu, Y. et al. Calcium-mediated calreticulin-IRE1α interaction drives dynamic fluctuation of IRE1α activity under chronic endoplasmic reticulum stress. Nat Commun 17, 4043 (2026). https://doi.org/10.1038/s41467-026-70679-7
Schlüsselwörter: Stress des endoplasmatischen Retikulums, Antwort auf fehlgefaltete Proteine, Calcium‑Signalgebung, Calreticulin, Zellüberleben