Clear Sky Science · it
L’interazione mediata dal calcio fra calreticolina e IRE1α guida la fluttuazione dinamica dell’attività di IRE1α sotto stress cronico del reticolo endoplasmatico
Come le cellule «navigano» le ondate di stress interno
All’interno di ogni cellula, una fitta rete di membrane ripiegate chiamata reticolo endoplasmatico funziona come il pavimento di una fabbrica per la sintesi e l’elaborazione delle proteine. Quando questa fabbrica è sovraccarica, la cellula si trova di fronte a un dilemma: riparare e adattarsi oppure spegnersi e morire. Questo studio mostra che un importante sensore di stress presente in questa «fabbrica», una proteina chiamata IRE1α, non si limita ad accendersi o spegnersi. La sua attività infatti aumenta, diminuisce e aumenta di nuovo in onde—regolata con precisione dagli ioni calcio e da una proteina ausiliaria chiamata calreticolina. Comprendere questo controllo sottile potrebbe far luce su malattie in cui lo stress cellulare a lungo termine ha un ruolo centrale, come il diabete, il cancro e le patologie neurodegenerative.
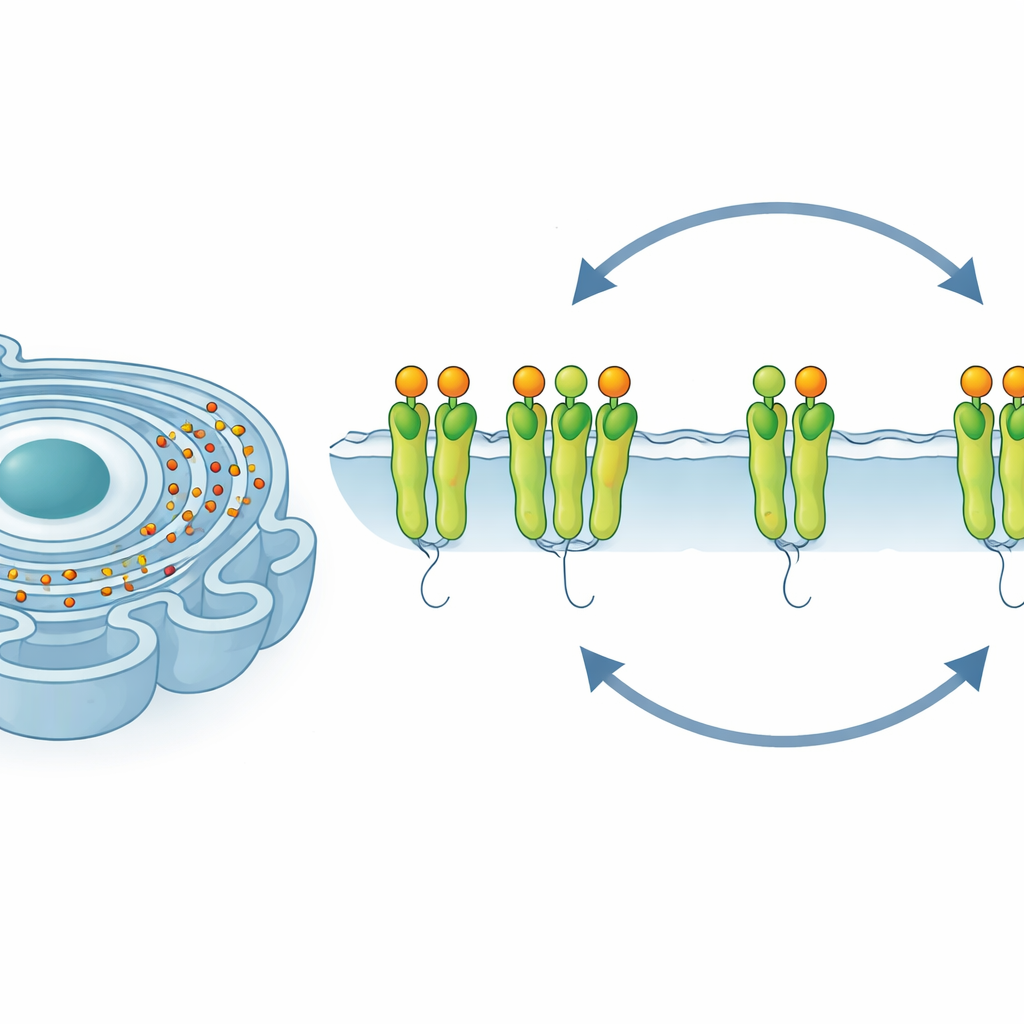
Quando le fabbriche di proteine si sovraccaricano
Nelle cellule sane, le proteine appena sintetizzate vengono inviate nel reticolo endoplasmatico, dove assumono la loro forma precisa. Se troppe proteine non ripiegate si accumulano, la cellula sperimenta ciò che gli scienziati chiamano «stress del RE». Per farvi fronte, le cellule attivano un programma protettivo noto come risposta alle proteine ripiegate. Tre sentinelle sulla membrana del RE rilevano i guasti e trasmettono segnali al resto della cellula. Una di queste sentinelle, IRE1α, è particolarmente importante perché contribuisce ad aumentare la capacità della cellula di ripiegare ed elaborare le proteine. Ma se lo stress è troppo intenso o prolungato, lo stesso sistema può ribaltarsi e favorire la morte cellulare. Come le cellule gestiscono questo equilibrio durante uno stress persistente ma non letale è stata a lungo una questione aperta.
Un segnale di stress che pulsa invece di rimanere costante
I ricercatori hanno esposto cellule umane a sostanze chimiche che inducono diversi livelli di stress del RE—lieve, intermedio e severo—e hanno seguito gli eventi per due giorni. Hanno misurato quanto IRE1α fosse attivato osservando le sue modifiche chimiche e l’elaborazione di una molecola messaggera partner che controlla. Sotto stress moderato e forte, hanno osservato un chiaro andamento «su‑giù‑su»: IRE1α diventava fortemente attivo entro poche ore, si attenuava più tardi e poi riprendeva molte ore dopo. Questo non era un evento isolato né un artefatto di un unico tipo cellulare; onde simili sono emerse in diversi tipi di cellule umane e murine. Al contrario, un altro ramo di risposta che favorisce la morte cellulare si riattivava solo nelle condizioni più severe e letali. Queste osservazioni suggeriscono che la cellula usa una strategia dinamica a impulsi per restare in vita sotto sforzo cronico.
La sfida a braccio di ferro tra due «aiutanti»
Per capire che cosa controlla queste onde, il gruppo ha esaminato quali proteine si legano fisicamente a IRE1α durante lo stress prolungato. Hanno scoperto un’interazione a bilico tra due assistenti del RE. Una, BIP, è nota come un freno che mantiene IRE1α sotto controllo. L’altra, la calreticolina, solitamente aiuta a ripiegare certe proteine ma qui si è rivelata un inatteso attivatore di IRE1α. Sotto stress persistente, il legame della calreticolina con IRE1α aumentava e diminuiva in parallelo con l’attività di IRE1α, mentre l’associazione di BIP mostrava il modello opposto. Esperimenti con proteine purificate e cellule ingegnerizzate hanno confermato che calreticolina e BIP competono direttamente per lo stesso sensore: quando una si lega più fortemente, l’altra viene respinta. Le cellule prive di calreticolina non riuscivano a generare la tarda «seconda ondata» di attività di IRE1α e risultavano più soggette alla morte, sottolineando il ruolo della calreticolina come partner pro‑sopravvivenza.
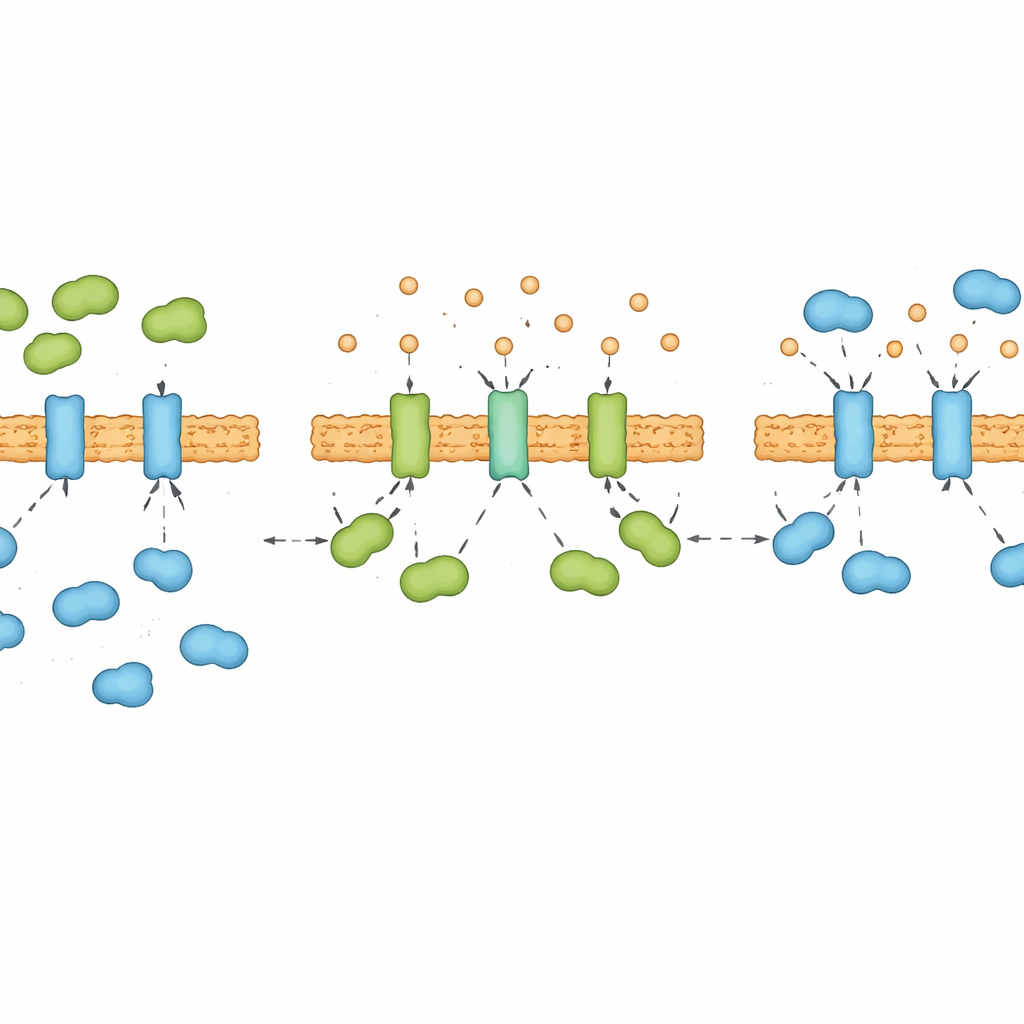
Il calcio come manopola nascosta della segnalazione di stress
La calreticolina è anche un importante serbatoio e partner di legame per il calcio all’interno del RE, e i ricercatori hanno scoperto che questa connessione è cruciale. Quando il calcio veniva rimosso dalla calreticolina in esperimenti in provetta, la proteina cambiava conformazione e si legava a IRE1α molto più saldamente. Una breve diminuzione dei livelli di calcio all’interno del RE nelle cellule vive rafforzava rapidamente il contatto della calreticolina con IRE1α, persino prima che le proteine non ripiegate avessero il tempo di accumularsi. Nel corso di molte ore di stress cronico, i livelli di calcio nel RE seguivano essi stessi un ritmo «giù‑su‑giù» che rispecchiava l’alternarsi della predominanza di calreticolina e BIP su IRE1α. In sostanza, il calcio agisce come una manopola nascosta che rimodella la calreticolina e decide se sia lei, o BIP, a vincere il braccio di ferro per il controllo del sensore di stress.
Ritmi quotidiani e la sottile linea tra sopravvivenza e morte
Emblematicamente, la stessa danza tra IRE1α, calreticolina, BIP e calcio si osserva nel fegato murino normale, anche in assenza di stress artificiale. Lì, l’attività di IRE1α e la sua associazione con la calreticolina aumentano e diminuiscono nel corso della giornata, suggerendo che questo meccanismo aiuta i tessuti sani ad adattarsi ai cicli naturali di lavoro, come le oscillazioni metaboliche giornaliere. Nel complesso, il lavoro descrive IRE1α non come un semplice interruttore acceso/spento, ma come un oscillatore finemente regolato, guidato da una calreticolina plasmata dal calcio e dalla sua rivalità con BIP. Per il lettore non specialistico, il messaggio chiave è che le cellule sottoposte a stress a lungo termine non scelgono vita o morte una sola volta; riesaminano ripetutamente quella decisione, usando onde chimiche interne per guadagnare tempo, adattarsi e, quando necessario, arrendersi.
Citazione: Cao, J., Zhao, X., Xu, Y. et al. Calcium-mediated calreticulin-IRE1α interaction drives dynamic fluctuation of IRE1α activity under chronic endoplasmic reticulum stress. Nat Commun 17, 4043 (2026). https://doi.org/10.1038/s41467-026-70679-7
Parole chiave: stress del reticolo endoplasmatico, risposta alle proteine ripiegate, segnalazione del calcio, calreticolina, sopravvivenza cellulare