Clear Sky Science · es
La interacción mediada por calcio entre calreticulina e IRE1α impulsa la fluctuación dinámica de la actividad de IRE1α bajo estrés crónico del retículo endoplásmico
Cómo las células surfean las olas del estrés interno
Dentro de cada célula, una extensa red de membranas plegadas llamada retículo endoplásmico actúa como la planta de producción para ensamblar y procesar proteínas. Cuando esta fábrica se sobrecarga, la célula afronta un dilema: reparar y adaptarse, o apagarse y morir. Este estudio revela que un sensor clave del estrés en esta fábrica, una proteína llamada IRE1α, no se limita a encenderse o apagarse. En su lugar, su actividad sube, baja y vuelve a subir en ondas—finamente moduladas por iones de calcio y una proteína auxiliar llamada calreticulina. Comprender este control sutil podría arrojar luz sobre enfermedades en las que el estrés celular a largo plazo desempeña un papel central, como la diabetes, el cáncer y la neurodegeneración.
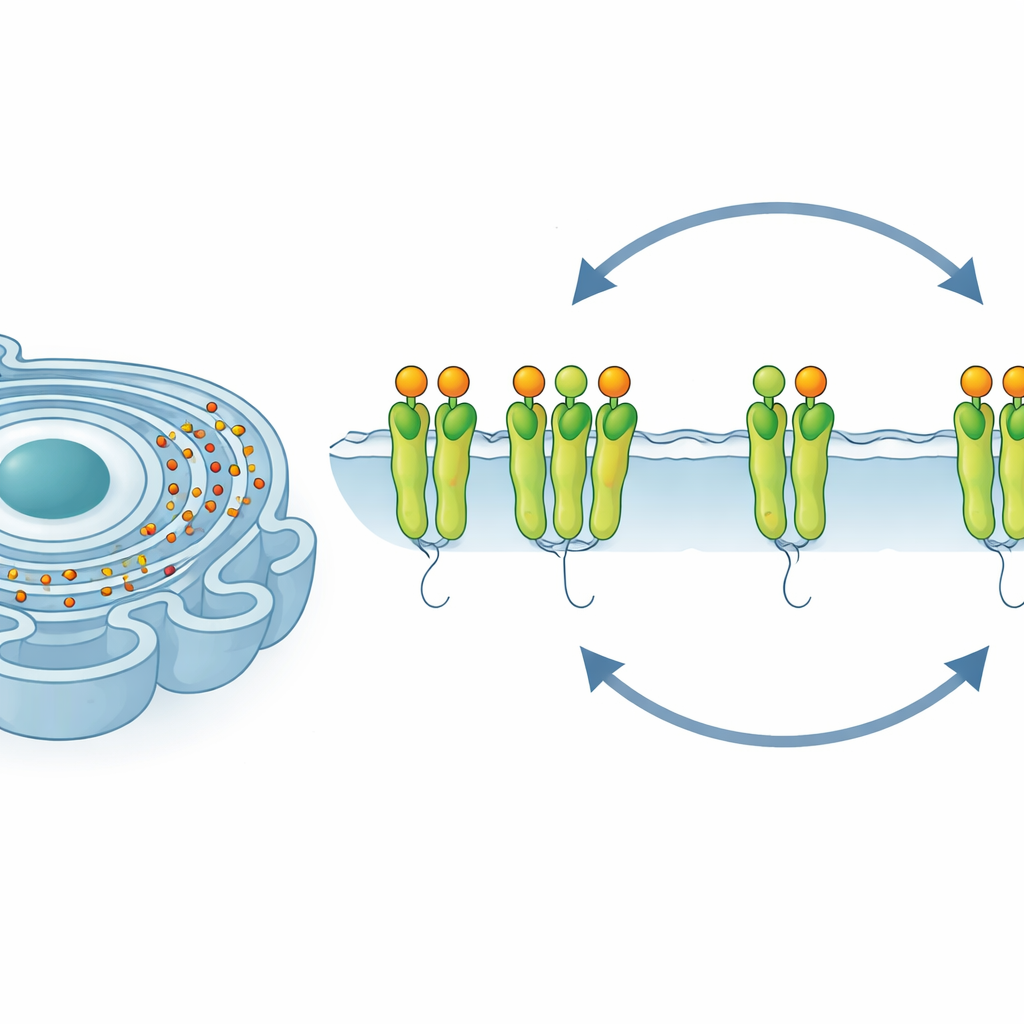
Cuando las fábricas de proteínas se saturan
En células sanas, las proteínas recién sintetizadas se introducen en el retículo endoplásmico, donde se pliegan en formas precisas. Si se acumulan demasiadas proteínas no plegadas, la célula experimenta lo que los científicos llaman “estrés del RE”. Para hacer frente, las células activan un programa de protección conocido como la respuesta a proteínas desplegadas. Tres centinelas en la membrana del RE detectan problemas y transmiten señales al resto de la célula. Uno de estos centinelas, IRE1α, es especialmente importante porque ayuda a aumentar la capacidad de la célula para plegar y procesar proteínas. Pero si el estrés es demasiado intenso o prolongado, ese mismo sistema puede cambiar de función y contribuir a empujar a la célula hacia la autodestrucción. Cómo gestionan las células este equilibrio bajo un estrés sostenido y no letal ha sido una cuestión abierta importante.
Una señal de estrés que pulsa en lugar de mantenerse plana
Los investigadores expusieron células humanas a químicos que provocan distintos niveles de estrés del RE—leve, intermedio y severo—y siguieron lo que ocurría durante dos días. Midieron la intensidad con la que IRE1α se activaba observando su modificación química y el procesamiento de una molécula mensajera asociada que controla. Bajo estrés moderado y fuerte, encontraron un patrón llamativo de “sube‑baja‑sube”: IRE1α se activó intensamente en varias horas, se silenció después y volvió a dispararse muchas horas más tarde. Esto no fue un evento aislado ni una rareza de un solo tipo celular; ondas similares aparecieron en varios tipos de células humanas y de ratón. En contraste, otra rama de la respuesta al estrés que favorece la muerte celular se reactiva solo en las condiciones más duras y letales. Estas observaciones sugieren que la célula emplea una estrategia dinámica y pulsante para mantenerse con vida bajo tensión crónica.
La lucha de poderes entre dos auxiliares
Para entender qué controla estas ondas, el equipo examinó qué proteínas se unen físicamente a IRE1α durante el estrés prolongado. Descubrieron una interacción de balancín entre dos colaboradores del RE. Una, BIP, es bien conocida como un freno que mantiene a IRE1α bajo control. La otra, la calreticulina, normalmente ayuda a plegar ciertas proteínas pero aquí resultó ser un activador inesperado de IRE1α. Bajo estrés sostenido, la unión de calreticulina a IRE1α aumentó y disminuyó en sincronía con la actividad de IRE1α, mientras que la unión de BIP mostró el patrón opuesto. Experimentos con proteínas purificadas y células manipuladas confirmaron que calreticulina y BIP compiten directamente por el mismo sensor: cuando una se une con más fuerza, la otra es desplazada. Las células sin calreticulina no pudieron generar la «segunda ola» tardía de actividad de IRE1α y fueron más propensas a morir, lo que subraya el papel de la calreticulina como un socio pro‑supervivencia.
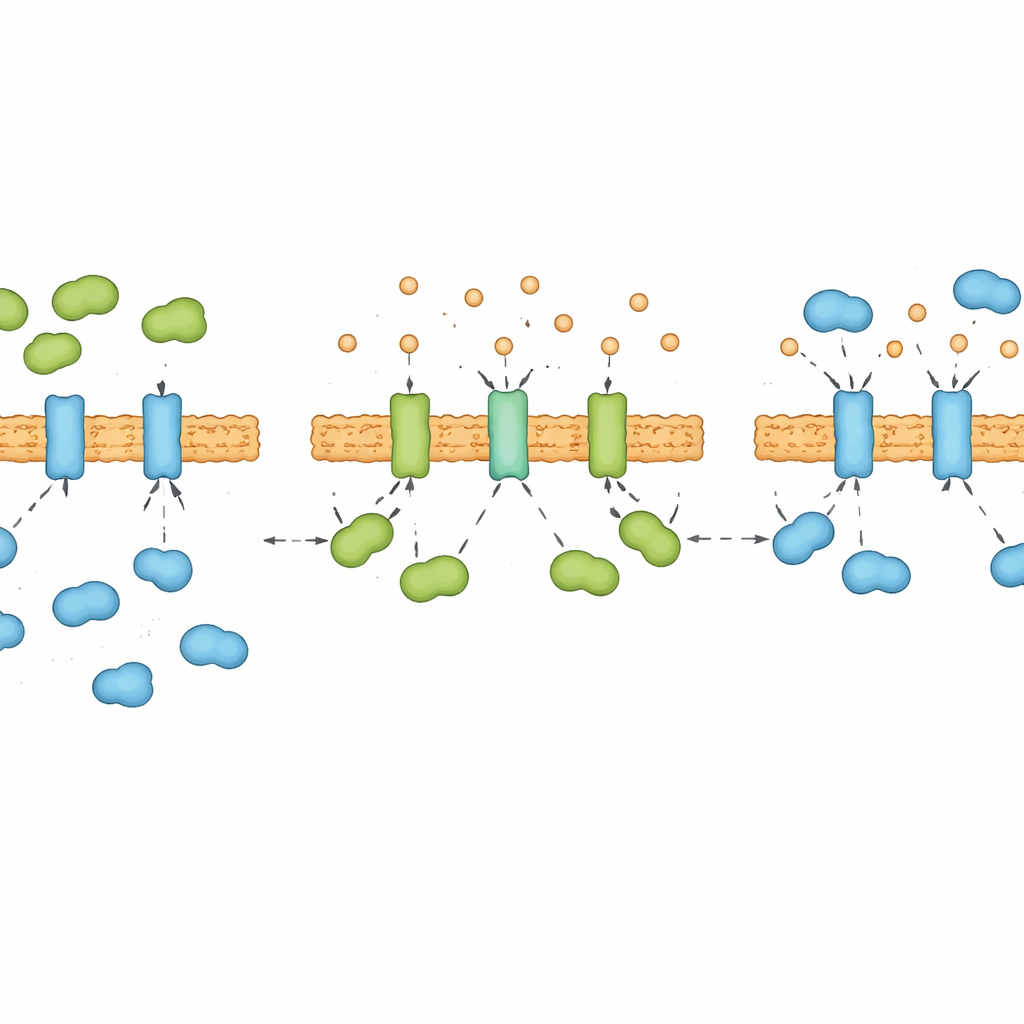
El calcio como un mando oculto de la señalización del estrés
La calreticulina también es una reserva importante y un ligando del calcio dentro del RE, y los investigadores encontraron que esta conexión es crucial. Cuando se despojó de calcio a la calreticulina en experimentos in vitro, la proteína cambió de conformación y se unió mucho más fuertemente a IRE1α. Una reducción breve de los niveles de calcio dentro del RE de células vivas fortaleció rápidamente el contacto de la calreticulina con IRE1α, incluso antes de que las proteínas desplegadas tuvieran tiempo de acumularse. Durante muchas horas de estrés crónico, los propios niveles de calcio en el RE siguieron un ritmo de “baja‑sube‑baja” que reflejaba la alternancia en la dominancia de la calreticulina y BIP sobre IRE1α. En esencia, el calcio actúa como un mando oculto que remodela la calreticulina y decide si ella o BIP ganan la lucha por el control del sensor de estrés.
Ritmos diarios y la delgada línea entre la supervivencia y la muerte
De forma llamativa, el mismo baile entre IRE1α, calreticulina, BIP y el calcio aparece en el hígado de ratón sano, incluso sin estrés artificial. Allí, la actividad de IRE1α y su asociación con la calreticulina aumentan y disminuyen a lo largo del día, lo que sugiere que este mecanismo ayuda a los tejidos sanos a ajustarse a ciclos naturales de carga de trabajo, como las oscilaciones diarias del metabolismo. En conjunto, el trabajo retrata a IRE1α no como un simple interruptor de encendido/apagado, sino como un oscilador finamente ajustado, guiado por la calreticulina moldeada por el calcio y su rivalidad con BIP. Para un lector general, el mensaje clave es que las células sometidas a tensión a largo plazo no toman una decisión única sobre la vida o la muerte; la revisitan repetidamente, usando ondas químicas internas para ganar tiempo, adaptarse y, cuando es necesario, rendirse.
Cita: Cao, J., Zhao, X., Xu, Y. et al. Calcium-mediated calreticulin-IRE1α interaction drives dynamic fluctuation of IRE1α activity under chronic endoplasmic reticulum stress. Nat Commun 17, 4043 (2026). https://doi.org/10.1038/s41467-026-70679-7
Palabras clave: estrés del retículo endoplásmico, respuesta a proteínas desplegadas, señalización por calcio, calreticulina, supervivencia celular