Clear Sky Science · pl
Przesiewowe badanie zachowań określa molekularne podgrupy parkinsonizmu u Drosophila
Dlaczego małe muszki mają znaczenie dla dużej choroby mózgu
Choroba Parkinsona jest najczęściej kojarzona z drżeniem i sztywnością, ale pod tymi objawami kryje się plątanina różnych przyczyn biologicznych. W tym badaniu wykorzystano muszki owocowe, by odpowiedzieć na kluczowe pytanie: czy liczne genetyczne formy parkinsonizmu można sprowadzić do zaledwie kilku podstawowych rodzajów zaburzeń wewnątrzkomórkowych? Jeśli tak, w przyszłości lekarze mogliby dobierać leczenie do konkretnego problemu komórkowego neuronów pacjenta, zamiast stosować jedno, uogólnione podejście.
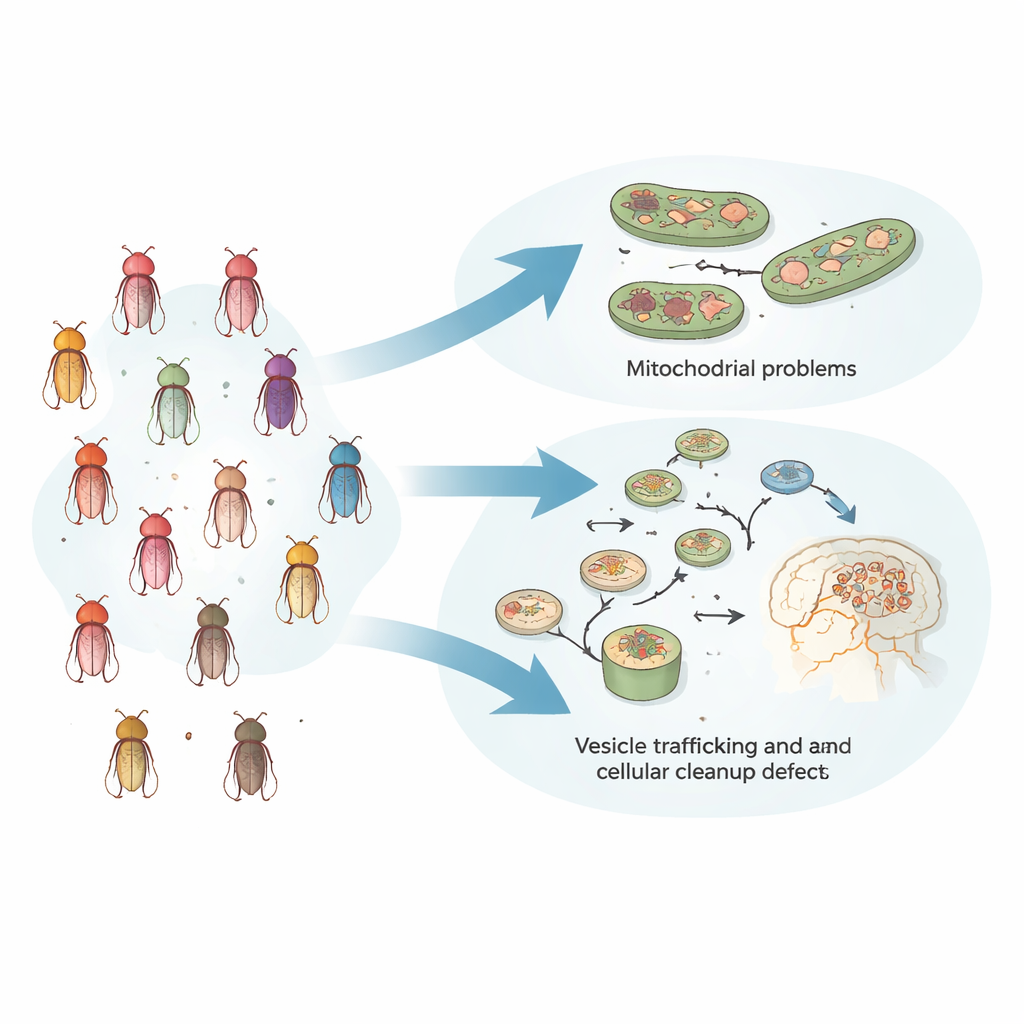
Wiele genów, jeden wspólny problem z ruchem
Naukowcy zaczęli od stworzenia kolekcji 24 linii muszek, z których każda nosiła defekt w innym genie znanym z wywoływania lub zwiększania ryzyka parkinsonizmu u ludzi. Muszki zostały starannie zmodyfikowane tak, by jedyną różnicą między nimi był wybrany gen, co pozwalało na czyste porównania. W miarę starzenia się owadów większość wykazywała zaburzenia ruchu w standardowym teście wspinaczkowym, przypominając stopniową utratę kontroli ruchowej u pacjentów. Problemy te wiązały się z uszkodzeniem komórek nerwowych produkujących dopaminę w mózgu muszki, a w wielu przypadkach można je było złagodzić, podając muszkom L‑Dopę — ten sam lek stosowany w leczeniu objawów Parkinsona u ludzi.
Ponad ruchem: sen, aktywność i ukryte wzorce
Parkinsonizm wpływa także na sen, czujność i inne rytmy dobowo‑behawioralne na długo przed pojawieniem się ciężkich zaburzeń ruchu. Aby uchwycić ten wczesny etap, zespół umieścił młode muszki — zanim pojawił się wyraźny spadek sprawności motorycznej — w zautomatyzowanych urządzeniach monitorujących aktywność i sen przez kilka dni. Wykorzystując uczenie maszynowe do analizy cech takich jak długość snu, moment zasypiania i częstotliwość wybudzeń, badacze odkryli wyraźne behawioralne odciski palców dla każdego modelu genetycznego. Po zgrupowaniu te wzory spójnie rozdzieliły 24 linie muszek na dwie szerokie grupy, z charakterystycznym profilem snu i aktywności dla każdej z nich, co sugeruje, że bardzo różne geny mogą wywoływać podobne zachowania całego organizmu, zaburzając powiązane procesy wewnątrzkomórkowe.
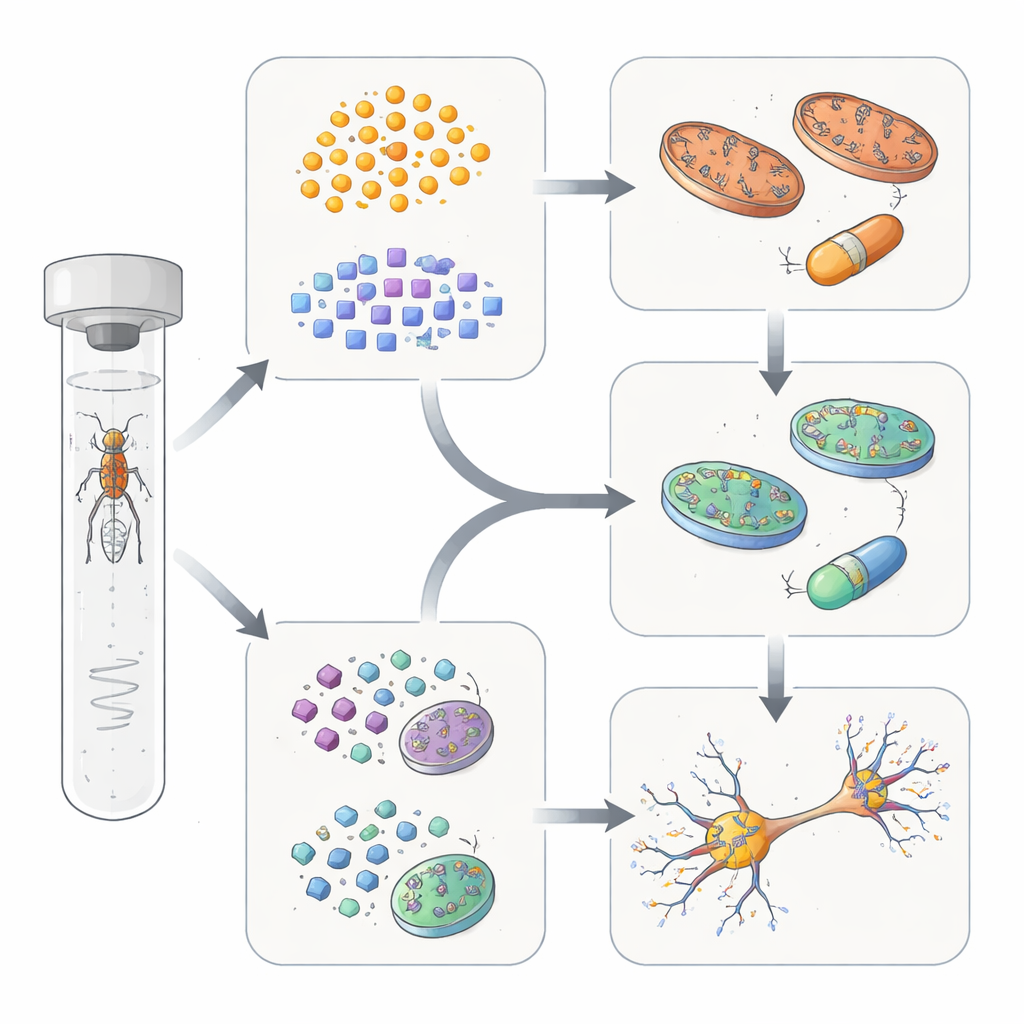
Dwa główne rodzaje problemów wewnątrzkomórkowych
Aby sprawdzić, czy grupy wyłonione na podstawie zachowań odzwierciedlają głębszą biologię, zespół zastosował dwa niezależne podejścia. Po pierwsze, zmierzył, jak pary mutacji genowych wchodzą ze sobą w interakcje w układzie wzrokowym muszki, używając czułego odczytu elektrycznego z oka. Pary genów, które znacząco pogarszały lub niespodziewanie poprawiały nawzajem swoje defekty, zwykle pochodziły z tej samej podgrupy określonej przez zachowanie, co wskazuje, że działają w wspólnych lub ściśle powiązanych szlakach. Po drugie, znane funkcje genów w każdej grupie układały się w czytelną narrację: jedna grupa koncentrowała się wokół mitochondriów — fabryk energii komórkowej, podczas gdy druga dotyczyła transportu pęcherzykowego, recyklingu składników komórkowych i systemów usuwania białek. Co istotne, miejsca i poziomy ekspresji genów w organizmie nie wyjaśniały podziału — istotne były ich funkcjonalne interakcje.
Testowanie ukierunkowanych napraw w mózgu muszki
Następnie autorzy sprawdzili, czy różnice między podgrupami mogą wskazywać drogę leczenia. U muszek, których geny należały do grupy mitochondrialnej, podawanie koenzymu Q10 — związku wspomagającego produkcję energii w mitochondriach — poprawiło zarówno zdrowie połączeń dopaminergicznych, jak i wydajność ruchową. W przeciwieństwie do tego te same wskaźniki nie poprawiły się u muszek z grupy zajmującej się transportem i recyklingiem. Zamiast tego muszki z tej drugiej grupy lepiej reagowały na związek stabilizujący kompleks białkowy zaangażowany w recykling komórkowy, który przywracał zakończenia nerwowe dopaminergiczne i ruch bez korzystnego efektu w grupie mitochondrialnej. Niektóre geny w trzeciej, mniejszej podgrupie wykazywały mieszane reakcje, co sugeruje, że pewne formy choroby leżą na skrzyżowaniu tych szlaków.
Co to oznacza dla osób z parkinsonizmem
Podsumowując, praca wskazuje, że wiele dziedzicznych form parkinsonizmu można przyporządkować do dwóch głównych typów problemów komórkowych: jeden z nich dominuje w uszkodzonej produkcji energii w mitochondriach, drugi — w zaburzeniach transportu i utylizacji ładunku komórkowego. Chociaż badanie przeprowadzono na muszkach owocowych, zaangażowane geny i szlaki są zgodne z tymi, które odgrywają rolę w chorobie u ludzi. Wyniki wspierają wizję przyszłości, w której pacjenci mogą być klasyfikowani nie tylko na podstawie objawów, lecz także na podstawie podstawowego szlaku chorobowego — i w której leki takie jak koenzym Q10 lub związki poprawiające recykling mogłyby być testowane specyficznie u pacjentów najbardziej prawdopodobnie na tym skorzystających, zamiast w szerokich, mieszanych populacjach, gdzie ich rzeczywista wartość może zostać ukryta.
Cytowanie: Kaempf, N., Valadas, J.S., Robberechts, P. et al. Behavioral screening defines the molecular Parkinsonism-related subgroups in Drosophila. Nat Commun 17, 3761 (2026). https://doi.org/10.1038/s41467-026-70303-8
Słowa kluczowe: Choroba Parkinsona, modele Drosophila, dysfunkcja mitochondriów, transport pęcherzykowy, spersonalizowana neurologia