Clear Sky Science · nl
Gedragscreening definieert de moleculaire, aan Parkinsonisme gerelateerde subgroepen in Drosophila
Waarom kleine vliegen ertoe doen bij een grote hersenziekte
De ziekte van Parkinson is het bekendst om trillen en stijfheid, maar onder die symptomen schuilen uiteenlopende biologische oorzaken. Deze studie gebruikt fruitvliegen om een cruciale vraag aan te pakken: komen de vele genetische vormen van Parkinsonisme uiteindelijk neer op slechts enkele kernproblemen binnen cellen? Als dat zo is, zouden artsen patiënten in de toekomst mogelijk op behandelingen kunnen afstemmen op basis van het specifieke cellulaire probleem van hun neuronen, in plaats van te vertrouwen op één standaardbehandeling voor iedereen.
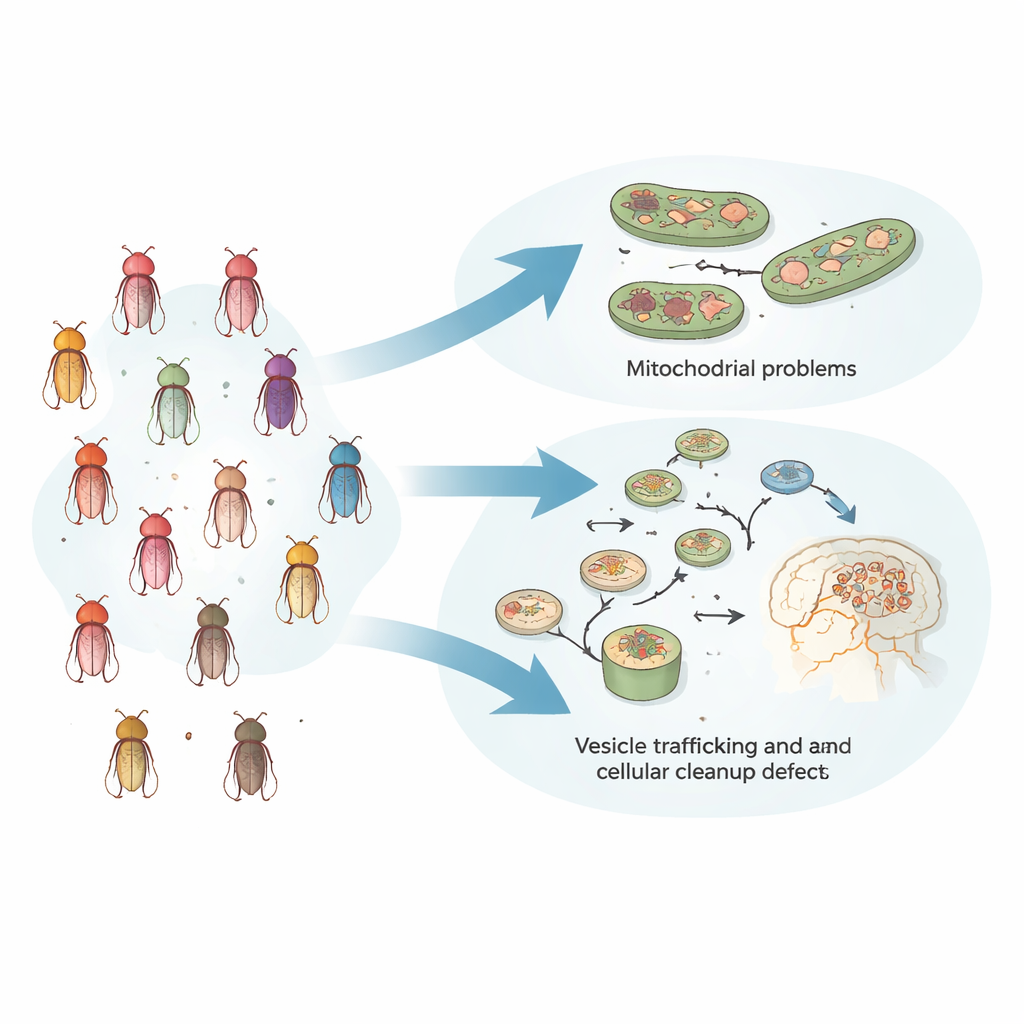
Veel genen, één gedeeld bewegingsprobleem
De onderzoekers begonnen met het opbouwen van een verzameling van 24 fruitvliegenlijnen, elk met een defect in een ander gen dat bekendstaat als veroorzaker of risicofactor voor Parkinsonisme bij mensen. Deze vliegen werden zorgvuldig geconstrueerd zodat alleen het gekozen gen tussen de lijnen verschilde, wat schone vergelijkingen mogelijk maakte. Naarmate de vliegen ouder werden, ontwikkelden de meeste bewegingsproblemen in een standaard klimtest, wat het geleidelijke verlies van motorische controle bij menselijke patiënten weerspiegelt. Deze problemen waren gekoppeld aan schade in dopamine-producerende zenuwcellen in de vlieg hersenen, en in veel gevallen konden ze worden verlicht door de vliegen L‑Dopa te geven, hetzelfde middel dat bij mensen de symptomen van Parkinson behandelt.
Verder dan beweging: slaap, activiteit en verborgen patronen
Parkinsonisme beïnvloedt ook slaap, waakzaamheid en andere dagelijkse ritmes lang voordat ernstige bewegingsproblemen optreden. Om dit vroege stadium vast te leggen, plaatste het team jonge vliegen — voordat sterke motorische achteruitgang zichtbaar was — in geautomatiseerde monitoringsapparaten die hun activiteit en slaap gedurende meerdere dagen registreerden. Met machine learning om kenmerken zoals slaapperiodes, wanneer ze in slaap vielen en hoe vaak ze wakker werden te analyseren, ontdekten de onderzoekers duidelijke gedragsvingerafdrukken voor elk genetisch model. Wanneer deze patronen werden geclusterd, vielen de 24 vlieg lijnen consequent in twee brede groepen, elk met een eigen kenmerkend slaap- en activiteitsprofiel, wat suggereert dat zeer verschillende genen vergelijkbaar gedrag in het hele dier kunnen veroorzaken door verwante interne processen te verstoren.
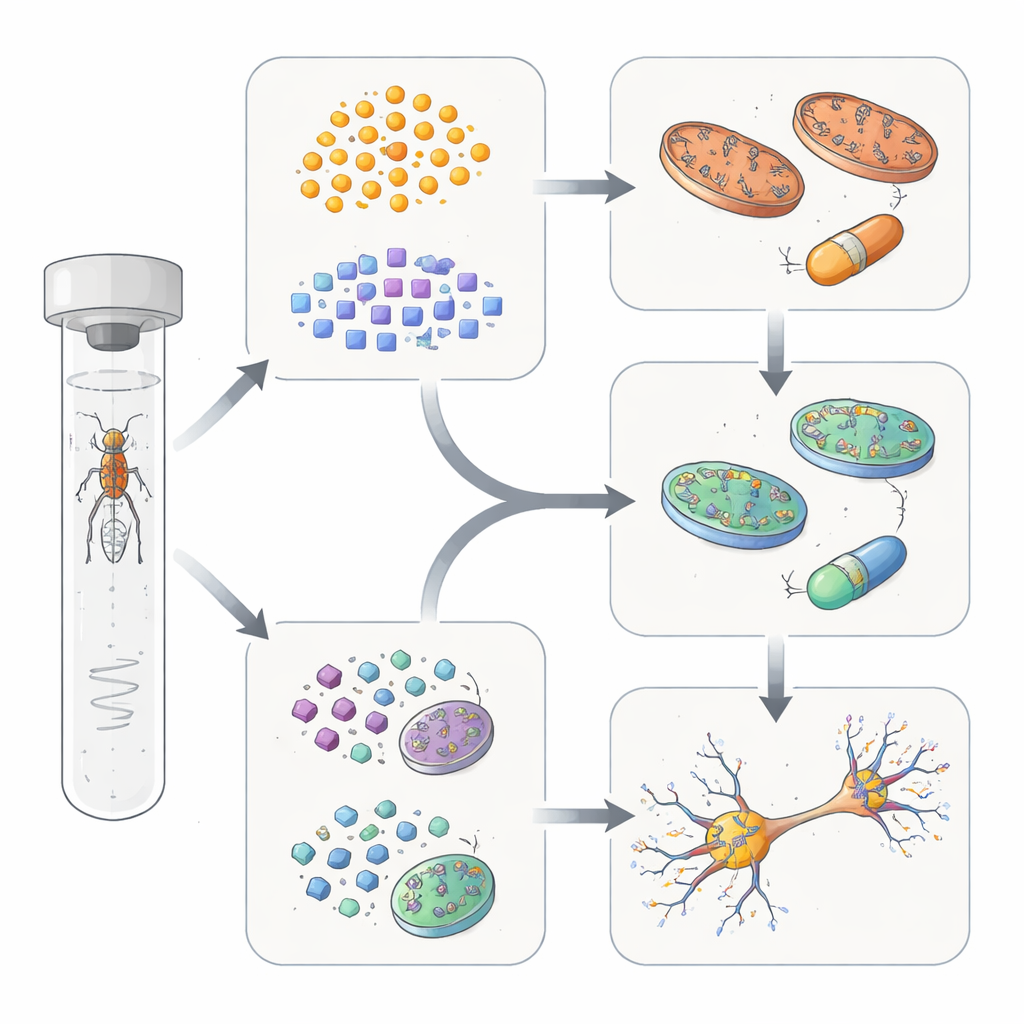
Twee hoofdtypen problemen binnen cellen
Om te onderzoeken of deze op gedrag gebaseerde groepen een diepere biologische onderbouwing hadden, gebruikte het team twee onafhankelijke benaderingen. Ten eerste maten ze hoe paren van genmutaties met elkaar interageerden in het vaatbare systeem van de vlieg met een gevoelige elektrische meting van het oog. Genparen die elkaars defecten sterk verergerden of onverwacht verbeterden, kwamen vaak uit dezelfde gedragsgedefinieerde subgroep, wat aangeeft dat ze in gedeelde of nauw verbonden routes werken. Ten tweede vertelde de bekende functie van de genen in elke groep een helder verhaal: de ene groep draaide om mitochondriën, de energiecentrales van de cel, terwijl de andere draaide om vesikelverkeer, recycling van cellulaire componenten en eiwitopruimsystemen. Belangrijk is dat waar en hoe sterk de genen in het lichaam werden tot expressie gebracht de indeling niet verklaarden — wat telde was hoe ze functioneel met elkaar interageerden.
Gerichte ingrepen testen in het vliegbrein
De auteurs vroegen zich vervolgens af of deze subgroepverschillen behandeling konden sturen. Bij vliegen waarvan de genen tot de mitochondriale groep behoorden, verbeterde voeding met Co-enzym Q10 — een molecuul dat de energieproductie in mitochondriën ondersteunt — zowel de gezondheid van dopaminerge verbindingen als de motorische prestaties. Daarentegen verbeterden deze metingen niet bij vliegen uit de verkeer- en opruimgroep. In plaats daarvan reageerden vliegen uit die tweede groep beter op een verbinding die een eiwitcomplex stabiliseert dat betrokken is bij cellulaire recycling; dit herstelde dopamine-eindigingen en beweging zonder de mitochondriale groep te helpen. Sommige genen in een derde, kleinere subgroep vertoonden gemengde reacties, wat erop wijst dat bepaalde ziektevormen op het kruispunt van deze routes liggen.
Wat dit betekent voor mensen met Parkinsonisme
Gezamenlijk suggereren de bevindingen dat veel erfelijke vormen van Parkinsonisme ingedeeld kunnen worden in twee belangrijke cellulaire probleemtypen: één gedomineerd door foutieve energieproductie in mitochondriën, en een andere door verstoord transport en afvoer van cellulaire lading. Hoewel deze studie in fruitvliegen is uitgevoerd, weerspiegelen de betrokken genen en routes nauw de mechanismen die bij de menselijke ziekte betrokken zijn. De resultaten ondersteunen een toekomst waarin patiënten niet alleen op symptomen worden geclassificeerd, maar ook op de onderliggende route die hun ziekte aandrijft — en waarin geneesmiddelen zoals Co-enzym Q10 of recyclingversterkende verbindingen specifiek getest kunnen worden bij de patiënten die het meest waarschijnlijk baat hebben, in plaats van in brede, gemengde populaties waar hun werkelijke waarde verborgen kan blijven.
Bronvermelding: Kaempf, N., Valadas, J.S., Robberechts, P. et al. Behavioral screening defines the molecular Parkinsonism-related subgroups in Drosophila. Nat Commun 17, 3761 (2026). https://doi.org/10.1038/s41467-026-70303-8
Trefwoorden: Ziekte van Parkinson, Drosophila-modellen, mitochondriale disfunctie, vesikelverkeer, gepersonaliseerde neurologie