Clear Sky Science · de
Verhaltens-Screening definiert die molekularen Parkinsonismus-Subgruppen in Drosophila
Warum winzige Fliegen für eine große Hirnkrankheit wichtig sind
Parkinson-Krankheit ist am bekanntesten für Zittern und Steifheit, doch unter diesen Symptomen verbergen sich viele unterschiedliche biologische Ursachen. Diese Studie nutzt Fruchtfliegen, um eine wichtige Frage zu klären: Laufen die vielen genetischen Formen des Parkinsonismus letztlich auf nur wenige Kernprobleme in den Zellen hinaus? Falls ja, könnten Ärztinnen und Ärzte eines Tages Patientinnen und Patienten anhand des spezifischen zellulären Defekts ihrer Neurone mit passenden Therapien versorgen, anstatt eine Einheitsbehandlung für alle zu verwenden.
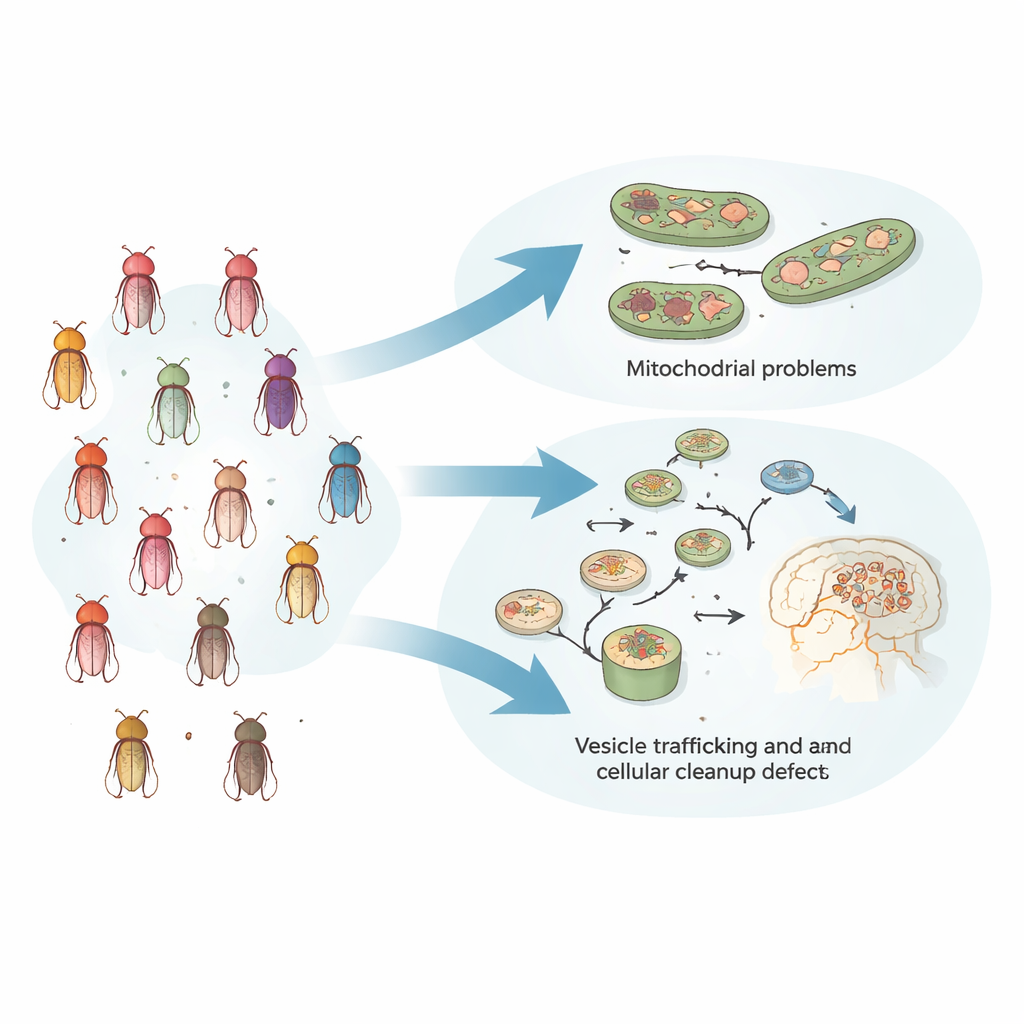
Viele Gene, ein gemeinsames Bewegungsproblem
Die Forschenden begannen damit, eine Sammlung von 24 Fruchtfliegenstämmen aufzubauen, von denen jeder einen Defekt in einem anderen Gen trug, das beim Menschen Parkinsonismus verursacht oder das Risiko erhöht. Diese Fliegen wurden so konstruiert, dass nur das gewählte Gen zwischen ihnen variierte, um saubere Vergleiche zu ermöglichen. Mit dem Alter entwickelten die meisten Fliegen Bewegungsprobleme in einem standardisierten Klettertest, was dem langsamen Verlust der motorischen Kontrolle bei Patientinnen und Patienten ähnelt. Diese Probleme standen im Zusammenhang mit Schäden an dopaminproduzierenden Nervenzellen im Fliegenhirn und ließen sich in vielen Fällen durch Fütterung mit L-Dopa lindern — demselben Medikament, das bei Menschen gegen Parkinson-Symptome eingesetzt wird.
Über die Bewegung hinaus: Schlaf, Aktivität und verborgene Muster
Parkinsonismus beeinflusst auch Schlaf, Wachheit und andere Tagesrhythmen lange bevor schwere Bewegungsstörungen auftreten. Um diese frühe Phase zu erfassen, setzten die Forschenden junge Fliegen — vor dem Auftreten starker motorischer Defizite — in automatisierte Überwachungsgeräte, die ihre Aktivität und ihren Schlaf über mehrere Tage verfolgten. Mithilfe von maschinellem Lernen zur Auswertung von Merkmalen wie Schlafdauer, Einschlafzeitpunkt und Aufwachhäufigkeit entdeckten sie deutliche Verhaltens-Fingerabdrücke für jedes genetische Modell. Beim Clustern dieser Muster fielen die 24 Linien beständig in zwei große Gruppen, jeweils mit charakteristischem Schlaf- und Aktivitätsprofil, was nahelegt, dass sehr unterschiedliche Gene ähnliche Verhaltensweisen des gesamten Organismus hervorrufen können, indem sie verwandte interne Prozesse stören.
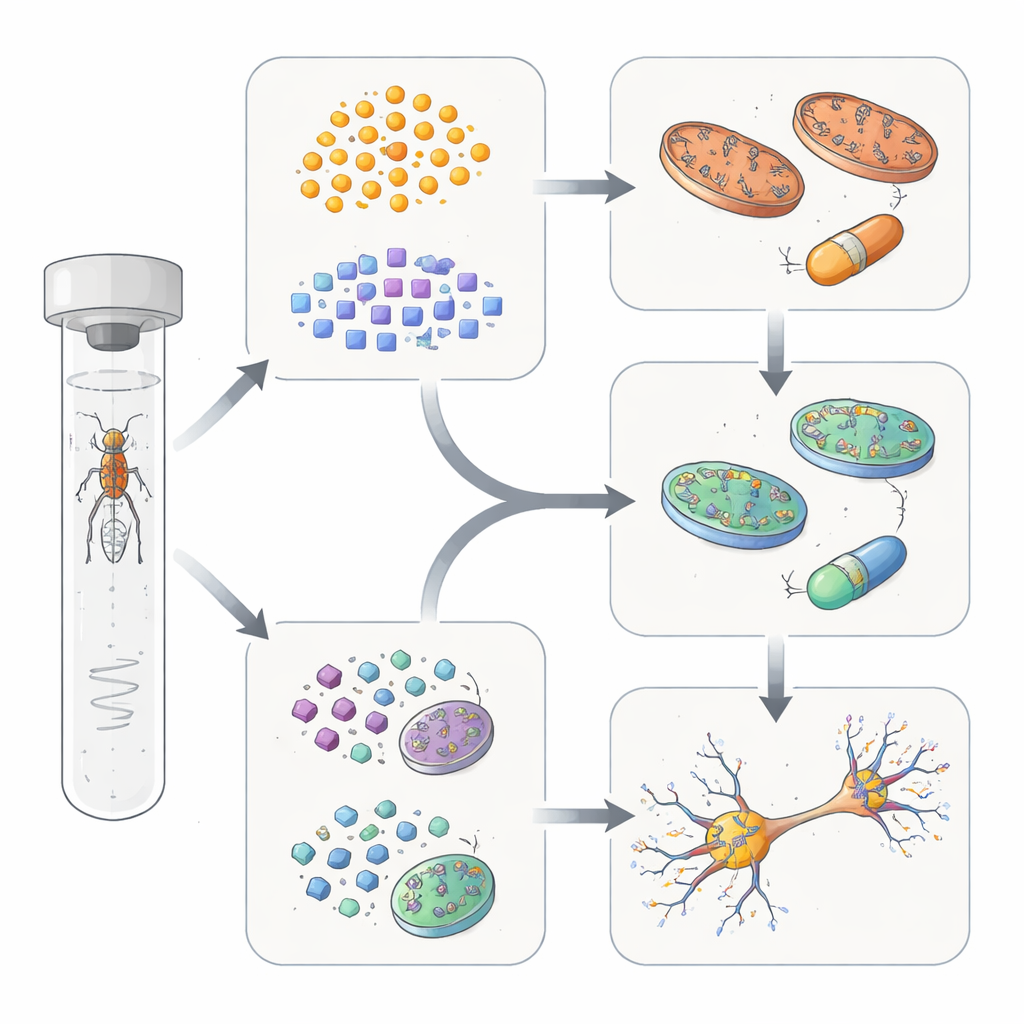
Zwei Hauptproblemtypen in den Zellen
Um zu prüfen, ob diese verhaltensbasierten Gruppen tiefere biologische Unterschiede widerspiegeln, nutzte das Team zwei unabhängige Ansätze. Zuerst maßen sie, wie sich Genpaar-Mutationen im visuellen System der Fliege mit einem empfindlichen elektrischen Messsignal aus dem Auge gegenseitig beeinflussten. Genpaare, die einander stark verschlechterten oder unerwartet verbesserten, stammten tendenziell aus derselben verhaltensdefinierten Untergruppe, was darauf hindeutet, dass sie in gemeinsamen oder eng verknüpften Signalwegen wirken. Zweitens ergaben die bekannten Funktionen der Gene in jeder Gruppe ein klares Bild: Eine Gruppe konzentrierte sich auf Mitochondrien, die Energieproduktionswerke der Zelle, während die andere den Vesikeltransport, das Recycling zellulärer Komponenten und Proteinentsorgungssysteme betraf. Wichtig war, dass das räumliche Muster oder die Stärke der Genexpression im Körper die Gruppierung nicht erklärte — entscheidend waren die funktionellen Wechselwirkungen.
Gezielte Eingriffe im Fliegenhirn testen
Die Autorinnen und Autoren fragten dann, ob diese Gruppenunterschiede die Therapie leiten könnten. Bei Fliegen aus der Mitochondriengruppe verbesserte die Gabe von Coenzym Q10 — einem Molekül, das die Energieproduktion in Mitochondrien unterstützt — sowohl die Gesundheit der Dopaminverbindungen als auch die motorische Leistung. Im Gegensatz dazu besserten sich diese Messgrößen bei Fliegen aus der Transport- und Recyclinggruppe nicht. Stattdessen sprachen Fliegen aus dieser zweiten Gruppe besser auf eine Verbindung an, die einen Protein-Komplex stabilisiert, der am zellulären Recycling beteiligt ist; dadurch wurden Dopamin-Nervenendigungen und Bewegung wiederhergestellt, ohne der Mitochondriengruppe zu nützen. Einige Gene in einer dritten, kleineren Untergruppe zeigten gemischte Reaktionen, was andeutet, dass bestimmte Krankheitsformen an den Schnittstellen dieser Wege liegen.
Was das für Menschen mit Parkinsonismus bedeutet
Zusammengefasst legt die Arbeit nahe, dass viele erbliche Formen des Parkinsonismus in zwei große zelluläre Problemtypen eingeteilt werden können: einer, der von fehlerhafter Energieproduktion in Mitochondrien dominiert wird, und ein anderer, der durch gestörten Transport und Abbau zellulärer Ladung geprägt ist. Obwohl die Studie an Fruchtfliegen durchgeführt wurde, spiegeln die beteiligten Gene und Signalwege jene wider, die auch bei der menschlichen Erkrankung eine Rolle spielen. Die Ergebnisse stützen die Vorstellung einer Zukunft, in der Patientinnen und Patienten nicht nur nach Symptomen, sondern auch nach dem zugrunde liegenden Pathway klassifiziert werden — und in der Wirkstoffe wie Coenzym Q10 oder recyclingfördernde Verbindungen gezielt in denjenigen Patienten getestet werden könnten, die am meisten davon profitieren, statt in breiten, heterogenen Gruppen, in denen ihr Nutzen verschleiert werden kann.
Zitation: Kaempf, N., Valadas, J.S., Robberechts, P. et al. Behavioral screening defines the molecular Parkinsonism-related subgroups in Drosophila. Nat Commun 17, 3761 (2026). https://doi.org/10.1038/s41467-026-70303-8
Schlüsselwörter: Parkinson-Krankheit, Drosophila-Modelle, mitochondriale Dysfunktion, Vesikeltransport, personalisierte Neurologie