Clear Sky Science · fr
Le criblage comportemental définit les sous-groupes moléculaires liés au parkinsonisme chez Drosophila
Pourquoi de minuscules mouches comptent pour une grande maladie cérébrale
La maladie de Parkinson est surtout connue pour les tremblements et la raideur, mais sous ces symptômes se cachent une mosaïque de causes biologiques différentes. Cette étude utilise la mouche du vinaigre pour aborder une question cruciale : les nombreuses formes génétiques du parkinsonisme se ramènent-elles réellement à seulement quelques types fondamentaux de dysfonctionnements cellulaires ? Si tel est le cas, les médecins pourraient un jour adapter les traitements aux patients en fonction des perturbations cellulaires spécifiques de leurs neurones, plutôt que d’appliquer une approche universelle.
Beaucoup de gènes, un même trouble moteur
Les chercheurs ont commencé par constituer une collection de 24 lignées de mouches, chacune portant une altération d’un gène différent connu pour causer ou augmenter le risque de parkinsonisme chez l’humain. Ces mouches ont été conçues de manière à ce que seul le gène choisi diffère entre elles, permettant des comparaisons nettes. En vieillissant, la plupart ont développé des troubles moteurs mesurables dans un test standard d’escalade, reflétant la perte progressive du contrôle moteur observée chez les patients. Ces déficits étaient associés à des atteintes des neurones producteurs de dopamine dans le cerveau des mouches et, dans de nombreux cas, pouvaient être atténués en administrant de la L‑Dopa, le même médicament utilisé pour traiter les symptômes parkinsoniens chez l’humain.
Au‑delà du mouvement : sommeil, activité et motifs cachés
Le parkinsonisme affecte aussi le sommeil, la vigilance et d’autres rythmes quotidiens bien avant l’apparition des troubles moteurs sévères. Pour capturer ce stade précoce, l’équipe a placé de jeunes mouches — avant le déclin moteur marqué — dans des dispositifs de surveillance automatisés suivant leur activité et leur sommeil sur plusieurs jours. En appliquant l’apprentissage automatique à des caractéristiques telles que la durée du sommeil, les moments d’endormissement et la fréquence des réveils, les chercheurs ont identifié des empreintes comportementales nettes pour chaque modèle génétique. En regroupant ces profils, les 24 lignées se sont constamment classées en deux grands groupes, chacun avec un profil de sommeil et d’activité caractéristique, suggérant que des gènes très différents peuvent produire des comportements animaux similaires en perturbant des processus cellulaires apparentés.
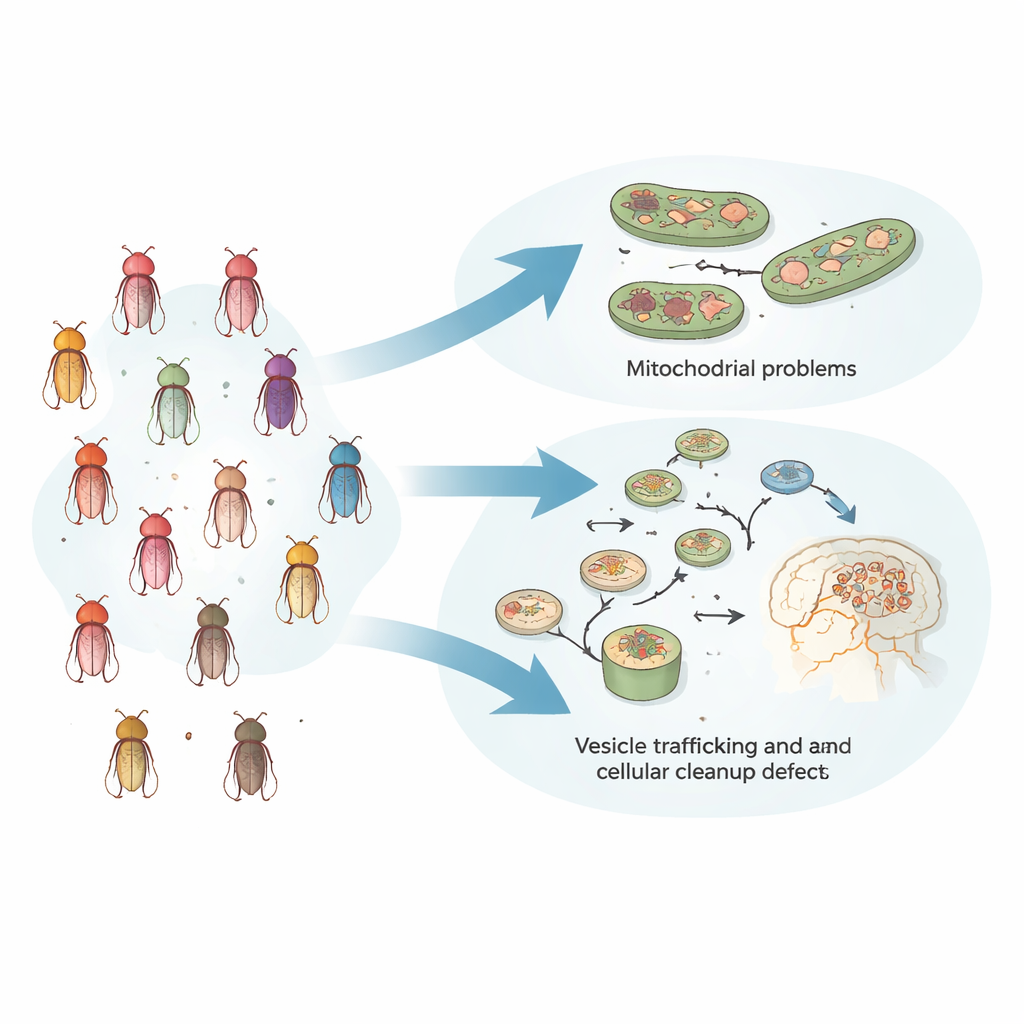
Deux types principaux de dysfonctionnements cellulaires
Pour vérifier si ces groupes basés sur le comportement reflétaient une biologie plus profonde, l’équipe a adopté deux approches indépendantes. D’abord, elle a mesuré comment des paires de mutations interagissaient dans le système visuel des mouches en utilisant un enregistrement électrique sensible de l’œil. Les paires de gènes qui aggravaient fortement ou, au contraire, amélioraient de façon inattendue les défauts l’une de l’autre provenaient souvent du même sous‑groupe défini par le comportement, ce qui indique qu’elles opèrent dans des voies partagées ou étroitement liées. Ensuite, les fonctions connues des gènes de chaque groupe ont livré un récit clair : un groupe était centré sur les mitochondries, les centrales énergétiques de la cellule, tandis que l’autre concernait le trafic vésiculaire, le recyclage des composants cellulaires et les systèmes d’élimination des protéines. De manière importante, la localisation ou le niveau d’expression des gènes dans l’organisme n’expliquaient pas le regroupement — ce qui comptait, c’était leurs interactions fonctionnelles.
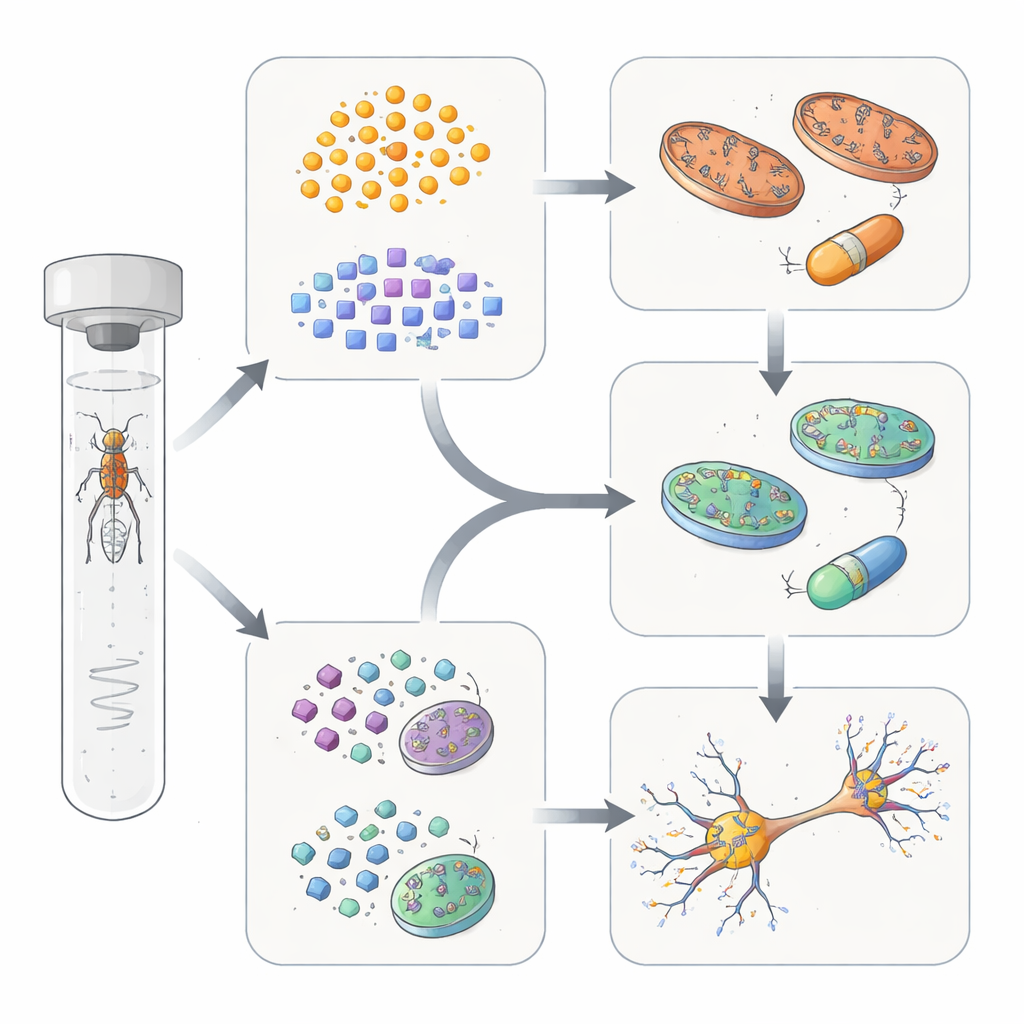
Tester des corrections ciblées dans le cerveau de la mouche
Les auteurs se sont ensuite demandé si ces différences de sous‑groupes pouvaient orienter les traitements. Chez les mouches dont les gènes appartenaient au groupe mitochondrial, l’administration de Coenzyme Q10 — une molécule soutenant la production d’énergie mitochondriale — a amélioré à la fois la santé des connexions dopaminergiques et les performances motrices. En revanche, ces mêmes mesures ne se sont pas améliorées chez les mouches du groupe axé sur le trafic et le recyclage. Ces dernières ont plutôt mieux répondu à un composé connu pour stabiliser un complexe protéique impliqué dans le recyclage cellulaire, qui a restauré les terminaisons dopaminergiques et le mouvement sans bénéfice pour le groupe mitochondrial. Certains gènes d’un troisième sous‑groupe, plus petit, ont montré des réponses mixtes, suggérant que certaines formes de la maladie se situent à l’intersection de ces voies.
Ce que cela signifie pour les personnes atteintes de parkinsonisme
Pris ensemble, ces résultats suggèrent que de nombreuses formes héréditaires de parkinsonisme peuvent être classées en deux grands types de dysfonctionnements cellulaires : l’un dominé par une production d’énergie déficiente au niveau des mitochondries, l’autre par un transport et une élimination perturbés des cargaisons cellulaires. Bien que l’étude ait été menée chez la mouche, les gènes et les voies impliqués reflètent étroitement ceux impliqués dans la maladie humaine. Ces conclusions plaident en faveur d’un avenir où les patients pourraient être classés non seulement par leurs symptômes, mais aussi par la voie sous‑jacente responsable de leur maladie — et où des médicaments comme la Coenzyme Q10 ou des composés favorisant le recyclage pourraient être testés spécifiquement chez les patients les plus susceptibles d’en tirer profit, plutôt que dans des populations larges et hétérogènes où leur valeur réelle pourrait rester masquée.
Citation: Kaempf, N., Valadas, J.S., Robberechts, P. et al. Behavioral screening defines the molecular Parkinsonism-related subgroups in Drosophila. Nat Commun 17, 3761 (2026). https://doi.org/10.1038/s41467-026-70303-8
Mots-clés: Maladie de Parkinson, Modèles Drosophila, Dysfonction mitochondriale, Trafic vésiculaire, Neurologie personnalisée