Clear Sky Science · pl
iCLAP: innowacyjna metoda do zintegrowanej wspólnej detekcji antygenów o niskim stężeniu przy wysokowydajnym barwieniu immunologicznym
Dostrzeganie trudno zauważalnych wskazówek w powszechnych tkankach
Lekarze i naukowcy często polegają na cienkich plasterkach zakonserwowanej tkanki, przechowywanych przez lata w archiwach szpitalnych, by zrozumieć, jak rozwijają się choroby takie jak rak czy cukrzyca. Jednak niektóre z najważniejszych alarmujących sygnałów w tych próbkach — białka występujące w bardzo małych ilościach — są praktycznie niewidoczne dla obecnych narzędzi obrazowania. W tym badaniu przedstawiono nową metodę, nazwaną iCLAP, która zamienia te słabe molekularne szepty w wyraźne sygnały, używając jednocześnie tych samych rutynowych bloków tkankowych, jakie znajdują się w pracowniach patologii.
Sprawianie, by słabe sygnały jaśniały
Większość zaawansowanych metod obrazowania może jednocześnie wykrywać wiele białek, ale działają najlepiej dla tych obecnych w dużych ilościach. Kluczowi regulatorzy starzenia, unikania nadzoru immunologicznego i zachowania nowotworów są często rzadcy i zostają pominięci. iCLAP (Integrable Co-detection of Low-Abundance Proteins) rozwiązuje ten problem, opierając się na chemicznym triku znanym jako amplifikacja sygnału. Metoda najpierw wykorzystuje reakcję napędzaną enzymatycznie, aby zgromadzić wiele fluorescencyjnych znaczników w pobliżu każdego białka docelowego, znacznie zwiększając emitowane światło. Następnie precyzyjnie dostosowany etap wybielania usuwa ten silny sygnał bez uszkadzania tkanki lub białek leżących poniżej. Pozwala to na wielokrotne barwienie, obrazowanie, kasowanie i ponowne użycie tego samego plasterka tkanki w kolejnych cyklach.
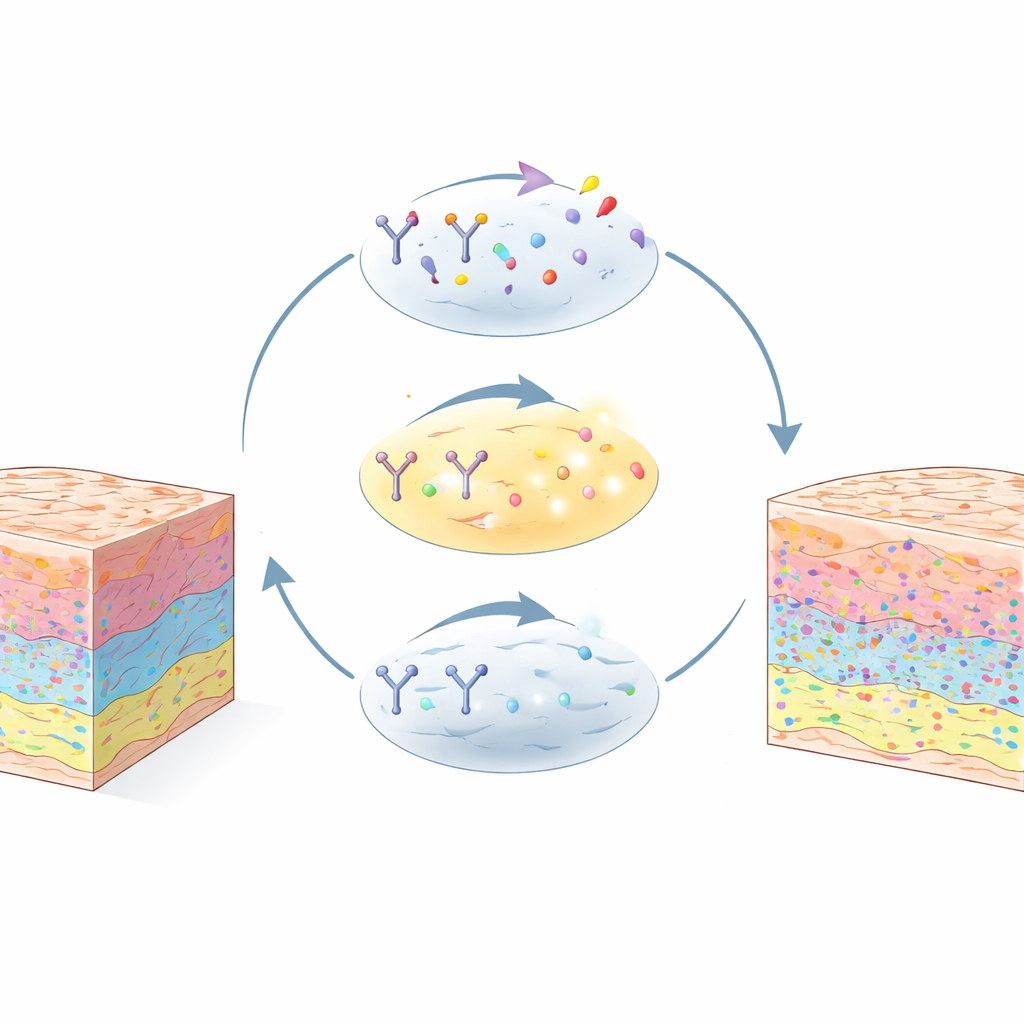
Praca z tkankami, które kliniki już posiadają
Co istotne, iCLAP zaprojektowano z myślą o tkankach utrwalonych formaliną i zatopionych w parafinie (FFPE) — standardowym sposobie przechowywania biopsji i próbek chirurgicznych w szpitalach. Autorzy wykazali, że powtarzane cykle amplifikacji i wybielania powodują jedynie minimalne straty tkanki, porównywalne z istniejącymi metodami obrazowania wielopleksowego. Po zobrazowaniu białek o niskim stężeniu za pomocą iCLAP, ten sam przekrój można ponownie zabarwić bardziej konwencjonalnymi metodami, aby ujawnić obfite markery strukturalne lub typów komórek. iCLAP można łączyć z kilkoma popularnymi platformami wysokopleksowymi, w tym CyCIF, CODEX i imaging mass cytometry, umożliwiając mapowanie ponad 40 różnych białek w pojedynczym plasterku tkanki.
Śledzenie starzenia komórek w trzustce
Aby zademonstrować, co daje ta zwiększona czułość, zespół skupił się na senescencji komórkowej — zmienionym stanie, w którym komórki przestają się dzielić i często zmieniają swoje zachowanie. Komórki senescentne uważa się za mające wpływ na starzenie, cukrzycę i raka, ale markery tego stanu mogą być bardzo rzadkie w tkankach ludzkich. Dzięki iCLAP badacze byli w stanie wyraźnie wykryć wiele markerów senescencji, w tym P16, P21, P53, 53BP1, HMGB1 i Lamin B1, w przechowywanych przekrojach ludzkiej trzustki. Porównując amplifikację opartą na iCLAP ze standardowym barwieniem fluorescencyjnym, wiele markerów niemal niewidocznych wcześniej stało się wyraźnie zdefiniowanych. Pozwoliło to mierzyć poziomy markerów w dziesiątkach tysięcy pojedynczych komórek i grupować komórki w odrębne subpopulacje na podstawie ich profili senescencyjnych.
Łączenie sygnałów starzeniowych ze strukturą i funkcją tkanki
Dzięki temu bardziej szczegółowemu widokowi naukowcy odwzorowali, gdzie w trzustce pojawiały się białka związane z senescencją. Stwierdzili, że różne markery miały tendencję do dominowania w różnych kompartmentach: niektóre były wzbogacone w obrębie wysepek produkujących hormony, inne w regionach pęcherzykowych produkujących enzymy, a jeszcze inne w strukturach przewodowych. W obrębie wysepek komórki z wysokim poziomem markera P16 były częstsze w większych i starszych wysepkach i wiązały się ze zmianami w równowadze komórek produkujących insulinę i glukagon. Na poziomie pojedynczej komórki jednak większość komórek silnie wyrażała tylko jeden marker senescencyjny, co sugeruje, że stan „starzenia” w tkankach ludzkich jest bardziej zróżnicowany i fragmentaryczny niż szerokie, wielomarkerowe wzorce często obserwowane w hodowlach komórkowych.
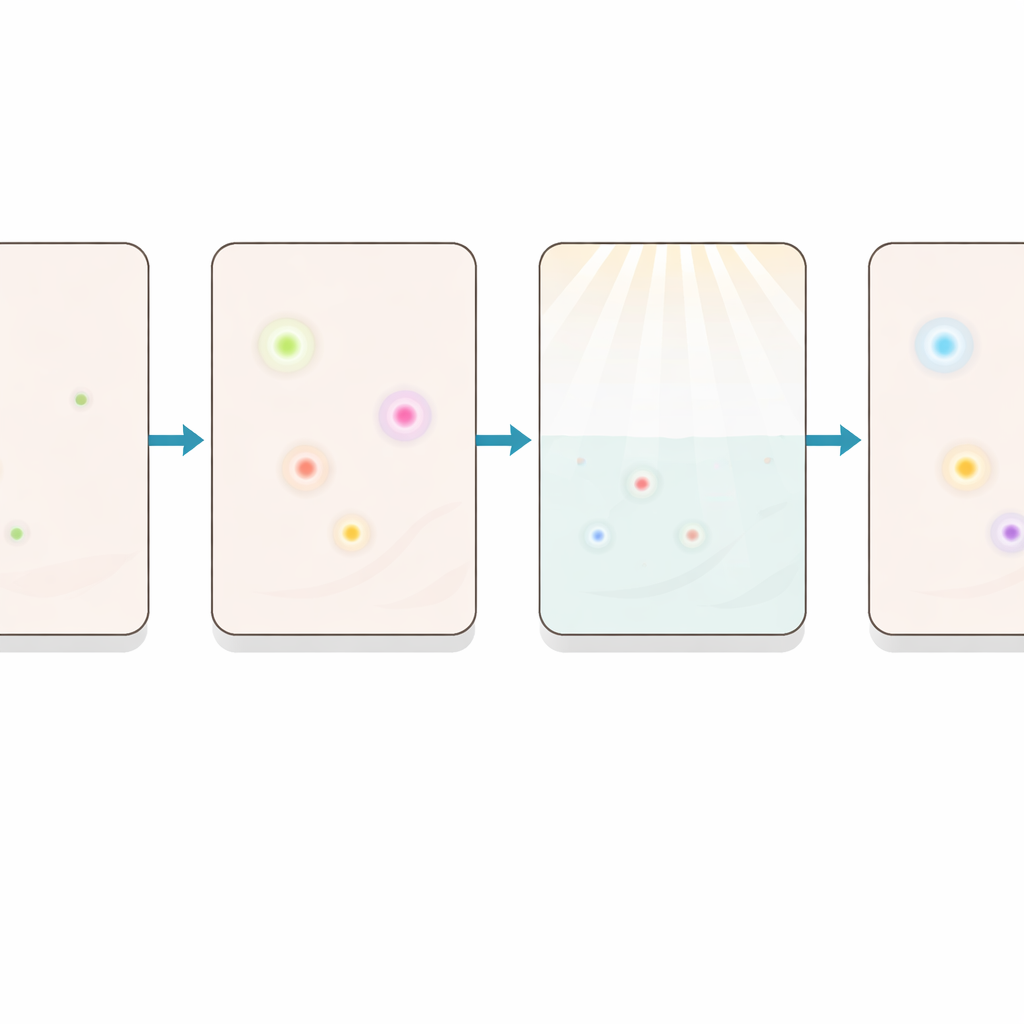
Wszechstronne okno na subtelne sygnały chorobowe
Na koniec zespół zastosował iCLAP do szeregu tkanek zdrowych i nowotworowych z narządów takich jak pierś, wątroba, szyjka macicy, jajnik i skóra. W tych próbkach nowotwory wykazywały znacznie silniejsze sygnały markerów senescencji niż pobliska zdrowa tkanka, co podkreśla potencjał metody w badaniach nad rakiem. Dzięki uwidocznieniu białek na niskim poziomie przy jednoczesnym zachowaniu możliwości obserwacji dziesiątek markerów na raz, iCLAP przekształca archiwalne próbki kliniczne w bogate, wysokowymiarowe mapy stanów komórkowych i ich sąsiedztw. Dla osób spoza specjalizacji kluczowe przesłanie jest takie, że wiele istotnych sygnałów chorobowych ukrywało się na widoku w istniejących kolekcjach tkanek — a nowe podejście oferuje praktyczny sposób, by je ujawnić.
Cytowanie: Wu, F., Zheng, S., Chen, Y. et al. iCLAP: an innovative method for integrable co-detection of low-abundance antigens with high-plex immunostaining. Nat Commun 17, 3104 (2026). https://doi.org/10.1038/s41467-026-69752-y
Słowa kluczowe: proteomika przestrzenna, senescencja komórkowa, obrazowanie wielopleksowe, tkanka FFPE, wyspy trzustkowe