Clear Sky Science · nl
iCLAP: een innovatieve methode voor integreerbare co-detectie van laag-abundante antigenen met high-plex immunokleuring
Zichtbaar maken van moeilijk waarneembare aanwijzingen in alledaagse weefsels
Artsen en wetenschappers vertrouwen vaak op dunne plakjes geconserveerd weefsel, jarenlang bewaard in ziekenhuisarchieven, om te begrijpen hoe ziekten zoals kanker of diabetes ontstaan. Maar sommige van de belangrijkste waarschuwingssignalen in deze monsters — eiwitten die slechts in zeer kleine hoeveelheden voorkomen — zijn met de huidige beeldvormingstools bijna onzichtbaar. Deze studie introduceert een nieuwe methode, iCLAP, die deze vage moleculaire fluisteringen in duidelijke signalen verandert, terwijl dezelfde routinematige weefselblokken gebruikt blijven worden die al in pathologielaboratoria aanwezig zijn.
Zwakke signalen laten opschijnen
De meeste geavanceerde beeldvormingsmethoden kunnen meerdere eiwitten tegelijk bekijken, maar ze werken het beste voor eiwitten die in hoge hoeveelheden aanwezig zijn. Sleutelregulatoren van veroudering, immuunontduiking en kankergedrag zijn vaak schaars en worden gemist. iCLAP (Integrable Co-detection of Low-Abundance Proteins) lost dit probleem op door voort te bouwen op een chemisch trucje dat signaalversterking heet. De methode gebruikt eerst een enzymgedreven reactie om veel fluorescerende labels dicht bij elk doelwit-eiwit op te stapelen, waardoor de uitgestraalde hoeveelheid licht sterk toeneemt. Vervolgens verwijdert een zorgvuldig afgestapte bleeksstap dat sterke signaal zonder het weefsel of de onderliggende eiwitten te beschadigen. Hierdoor kan dezelfde weefselschijf meerdere keren gekleurd, afgebeeld, uitgeveegd en hergebruikt worden.
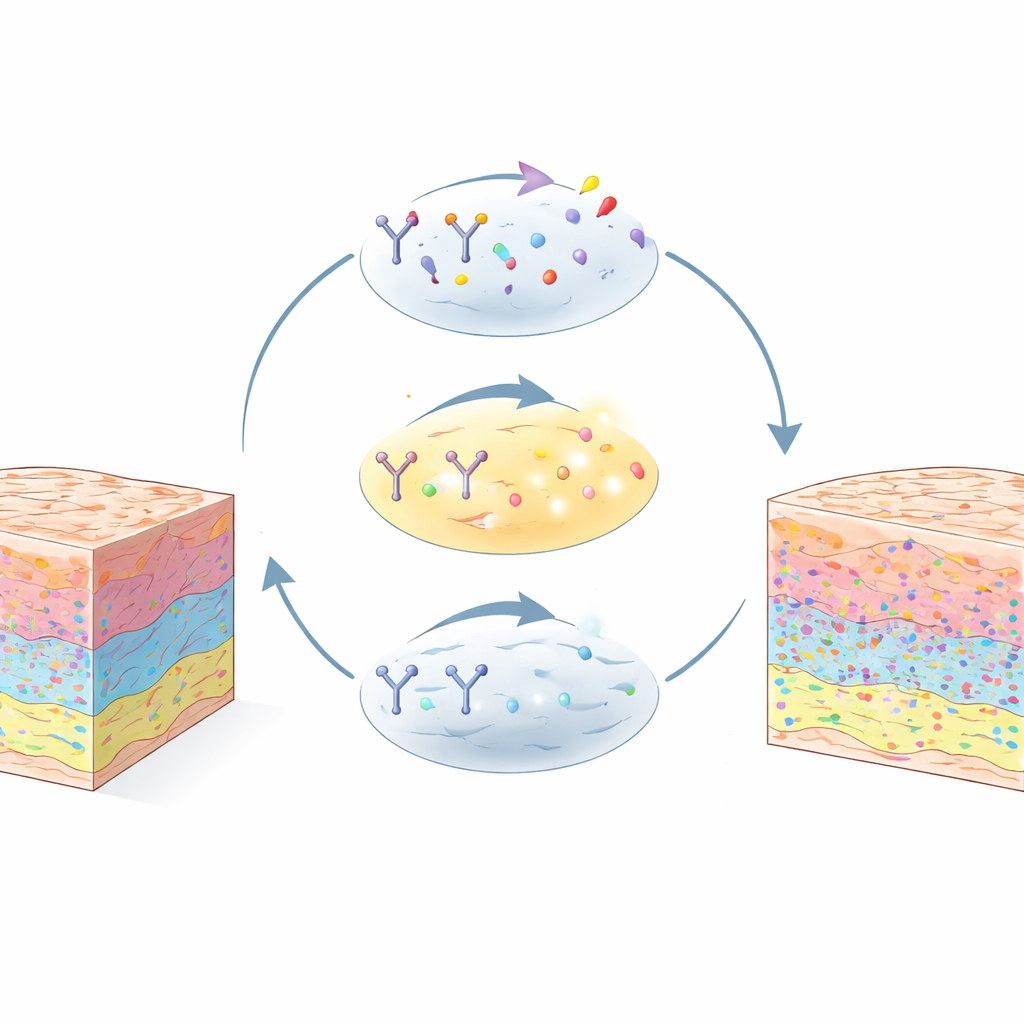
Werken met het weefsel dat klinieken al hebben
Cruciaal is dat iCLAP is ontworpen voor formaline-gefixeerd, paraffine-ingebed (FFPE) weefsel — de standaardmethode waarmee ziekenhuizen biopsieën en chirurgische monsters bewaren. De auteurs tonen aan dat herhaalde versterkings- en bleekcycli slechts minimale weefselverlies veroorzaken, vergelijkbaar met bestaande multiplexbeeldvormingsmethoden. Nadat de laag-abundante eiwitten met iCLAP zijn afgebeeld, kan dezelfde sectie opnieuw worden gekleurd met meer conventionele benaderingen om overvloedige structurele of cel-type markers zichtbaar te maken. iCLAP kan worden gecombineerd met verschillende populaire high-plex platformen, waaronder CyCIF, CODEX en imaging mass cytometry, waardoor kaartlegging van meer dan 40 verschillende eiwitten in één weefselschijf mogelijk wordt.
Cellulaire veroudering opsporen in de alvleesklier
Om te demonstreren wat deze extra gevoeligheid mogelijk maakt, richtte het team zich op cellulaire senescentie — een veranderde toestand waarbij cellen stoppen met delen en vaak hun gedrag aanpassen. Senescente cellen zouden invloed hebben op veroudering, diabetes en kanker, maar de eiwitten die deze toestand markeren kunnen in menselijke weefsels zeer schaars zijn. Met iCLAP konden de onderzoekers meerdere senescentiemarkers duidelijk detecteren, waaronder P16, P21, P53, 53BP1, HMGB1 en Lamin B1, in bewaarde secties van menselijke alvleesklier. Wanneer zij iCLAP-gebaseerde versterking vergeleken met standaard fluorescentiekleuring, werden veel markers die eerder bijna onzichtbaar waren scherp afgebakend. Dit stelde hen in staat om markerniveaus in tienduizenden individuele cellen te meten en cellen in verschillende subpopulaties te groeperen op basis van hun senescentieprofielen.
Verouderingssignalen koppelen aan weefselstructuur en functie
Met dit gedetailleerdere beeld brachten de wetenschappers in kaart waar senescentie-gerelateerde eiwitten in de alvleesklier voorkwamen. Ze ontdekten dat verschillende markers de neiging hadden te domineren in verschillende compartimenten: sommige waren verrijkt binnen de hormoonproducerende eilandjes, andere in de enzymproducerende acinaire gebieden en weer andere in ductale structuren. Binnen eilandjes kwamen cellen met hoge niveaus van de marker P16 vaker voor in grotere en oudere eilandjes en waren ze geassocieerd met verschuivingen in de balans tussen insuline- en glucagon-producerende cellen. Op het niveau van individuele cellen drukte de meeste cellen echter slechts één senescentiemarker sterk uit, wat suggereert dat de “verouderings”-toestand in menselijke weefsels diverser en gefragmenteerder is dan de brede, multi-markerpatronen die vaak in kweekcellen worden gezien.
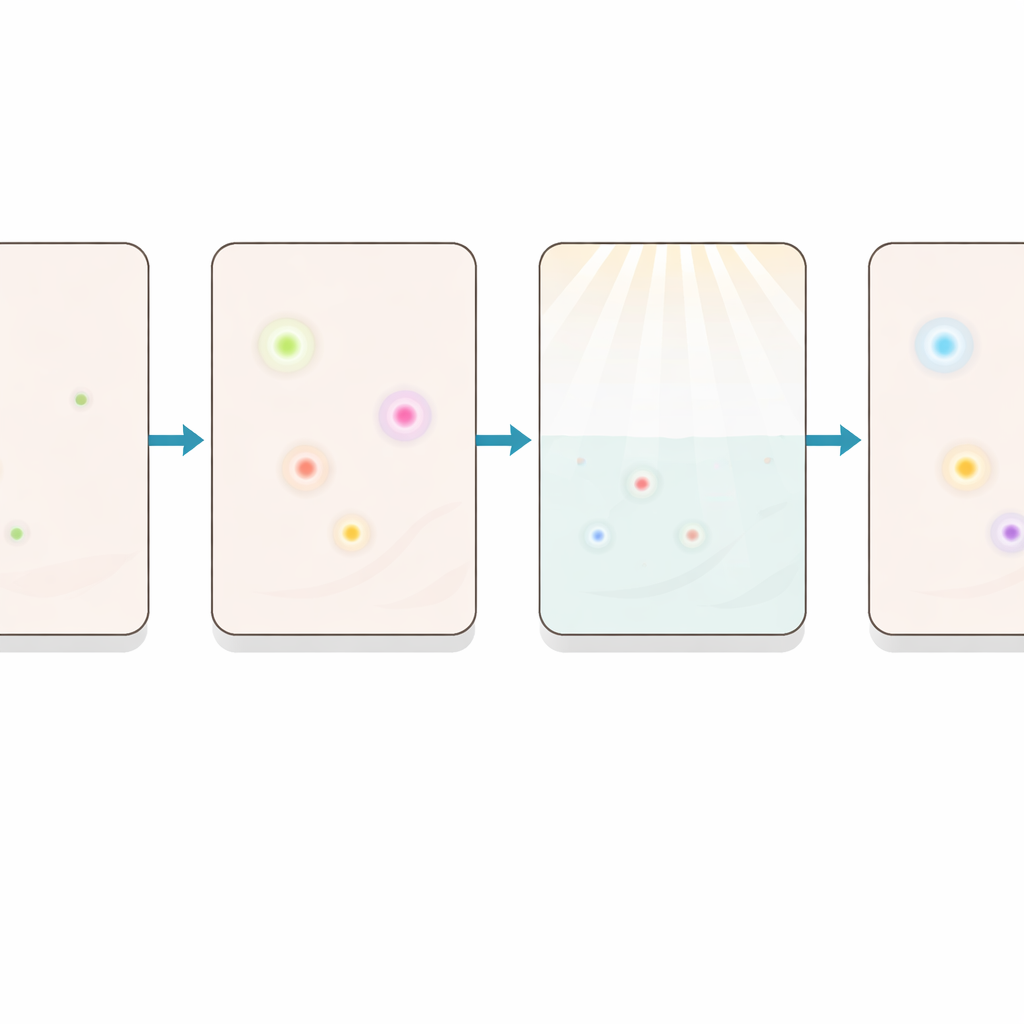
Een veelzijdig venster op subtiele ziektesignalen
Tot slot paste het team iCLAP toe op een reeks normale en tumorweefsels uit organen zoals borst, lever, baarmoederhals, eierstok en huid. In deze monsters vertoonden tumoren veel sterkere senescentiemarkersignalen dan het omliggende gezonde weefsel, wat het potentieel van de methode voor kankeronderzoek onderstreept. Door laag-niveau eiwitten zichtbaar te maken terwijl de mogelijkheid behouden blijft om tientallen markers tegelijk te bekijken, verandert iCLAP gearchiveerde klinische monsters in rijke, hoge-dimensionale kaarten van celtoestanden en buurten. Voor niet-specialisten is de kernboodschap dat veel cruciale ziektesignalen al in het zicht in bestaande weefselscollecties verborgen waren — en dat deze nieuwe benadering een praktische manier biedt om ze te onthullen.
Bronvermelding: Wu, F., Zheng, S., Chen, Y. et al. iCLAP: an innovative method for integrable co-detection of low-abundance antigens with high-plex immunostaining. Nat Commun 17, 3104 (2026). https://doi.org/10.1038/s41467-026-69752-y
Trefwoorden: ruimtelijke proteomica, cellulaire veroudering, multiplexbeeldvorming, FFPE-weefsel, alvleesklier-eilandjes