Clear Sky Science · it
iCLAP: un metodo innovativo per la co-detezione integrabile di antigeni a bassa abbondanza con immunocolorazione ad alto plex
Individuare indizi difficili da vedere nei tessuti di tutti i giorni
Medici e ricercatori fanno spesso affidamento su sottili sezioni di tessuto preservato, conservate per anni negli archivi ospedalieri, per comprendere come si sviluppano malattie come il cancro o il diabete. Ma alcuni dei segnali d’allarme più importanti in questi campioni — proteine presenti solo in quantità minime — sono quasi invisibili con gli strumenti di imaging attuali. Questo studio presenta un nuovo metodo, chiamato iCLAP, che trasforma questi deboli sussurri molecolari in segnali chiari, utilizzando gli stessi blocchi di tessuto di routine già presenti nei laboratori di patologia.
Far risplendere segnali deboli
La maggior parte dei metodi di imaging avanzati può analizzare molte proteine contemporaneamente, ma funzionano meglio per quelle presenti in elevata quantità. Regolatori chiave dell’invecchiamento, dell’evasione immunitaria e del comportamento tumorale sono spesso rari e vengono persi. iCLAP (Integrable Co-detection of Low-Abundance Proteins) risolve questo problema sfruttando un trucco chimico noto come amplificazione del segnale. Il metodo utilizza innanzitutto una reazione guidata da enzimi per accumulare molte etichette fluorescenti vicino a ciascuna proteina target, incrementando notevolmente la luce emessa. Poi, un passaggio di foto-bleaching calibrato rimuove quel segnale intenso senza danneggiare il tessuto o le proteine sottostanti. Ciò permette alla stessa sezione di essere colorata, immaginata, cancellata e riutilizzata per più cicli.
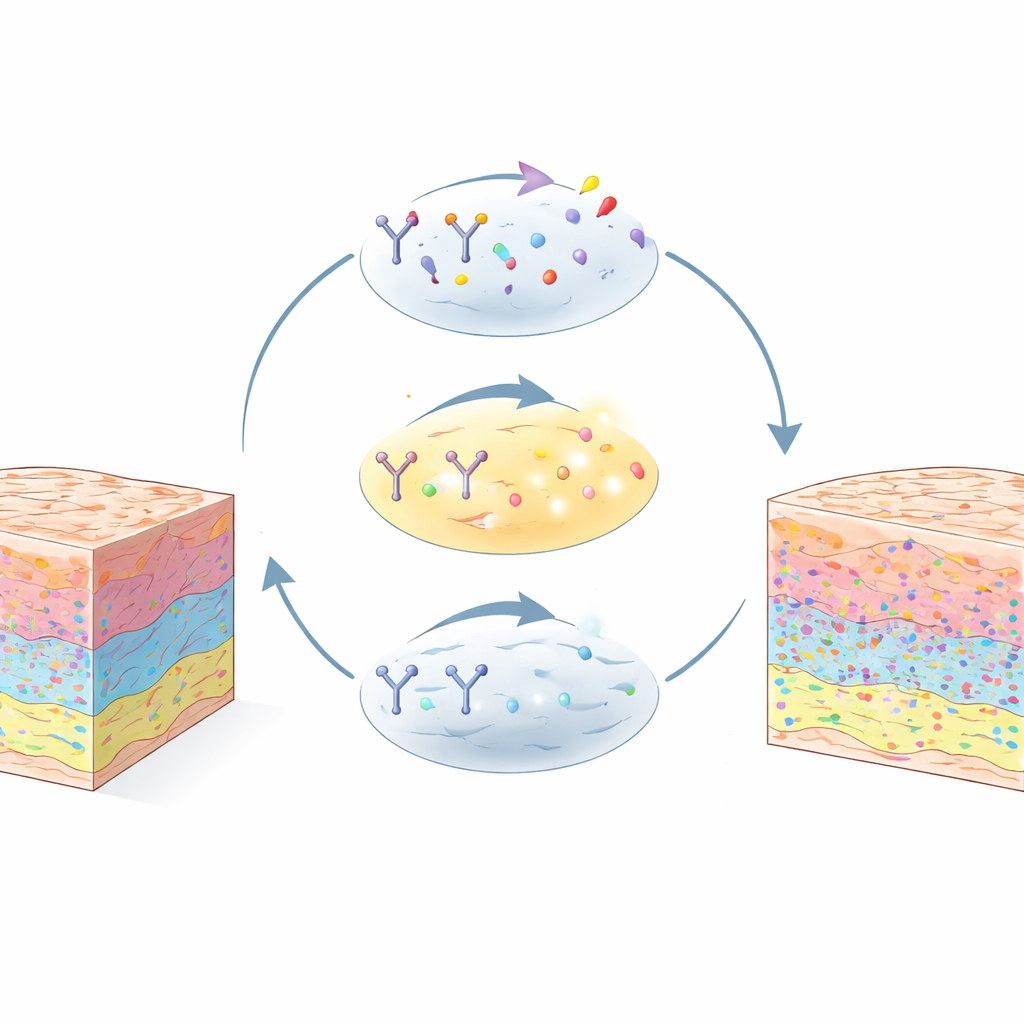
Lavorare con i tessuti che le cliniche già possiedono
Fondamentale, iCLAP è pensato per tessuti fissati in formalina e inclusi in paraffina (FFPE) — il modo standard con cui gli ospedali preservano biopsie e campioni chirurgici. Gli autori mostrano che cicli ripetuti di amplificazione e bleaching causano solo una perdita tissutale minima, comparabile ai metodi di imaging multiplex esistenti. Dopo che le proteine a bassa abbondanza sono state immaginate con iCLAP, la stessa sezione può essere tinta nuovamente con approcci più convenzionali per rivelare marcatori strutturali o di tipo cellulare più abbondanti. iCLAP può essere combinato con diverse piattaforme high-plex popolari, tra cui CyCIF, CODEX e imaging mass cytometry, permettendo mappe di oltre 40 proteine diverse in una singola sezione di tessuto.
Monitorare l’invecchiamento cellulare nel pancreas
Per dimostrare cosa rende possibile questa sensibilità aumentata, il team si è concentrato sulla senescenza cellulare — uno stato alterato in cui le cellule smettono di dividersi e spesso modificano il proprio comportamento. Le cellule senescenti si ritiene influenzino l’invecchiamento, il diabete e il cancro, ma le proteine che marcano questo stato possono essere molto scarse nei tessuti umani. Usando iCLAP, i ricercatori sono riusciti a rilevare chiaramente molteplici marcatori di senescenza, inclusi P16, P21, P53, 53BP1, HMGB1 e Lamin B1, in sezioni conservate di pancreas umano. Confrontando l’amplificazione basata su iCLAP con la colorazione fluorescente standard, molti marcatori quasi invisibili in precedenza sono diventati nitidamente definiti. Ciò ha permesso di misurare i livelli dei marcatori in decine di migliaia di singole cellule e di raggruppare le cellule in sottopopolazioni distinte in base ai loro profili di senescenza.
Collegare i segnali di invecchiamento alla struttura e funzione del tessuto
Con questa vista più dettagliata, gli scienziati hanno mappato dove comparivano le proteine correlate alla senescenza all’interno del pancreas. Hanno riscontrato che diversi marcatori tendevano a predominare in compartimenti differenti: alcuni erano arricchiti nelle isole produttrici di ormoni, altri nelle regioni acinari produttrici di enzimi e altri nelle strutture duttali. All’interno delle isole, le cellule con elevati livelli del marcatore P16 erano più comuni nelle isole più grandi e più anziane e erano associate a cambiamenti nell’equilibrio tra cellule produttrici di insulina e di glucagone. Tuttavia, a livello di singola cellula, la maggior parte delle cellule esprimeva fortemente solo un marcatore di senescenza, suggerendo che lo stato di “invecchiamento” nei tessuti umani è più vario e frammentato rispetto ai pattern multi-marcatori ampiamente osservati nelle cellule coltivate in vitro.
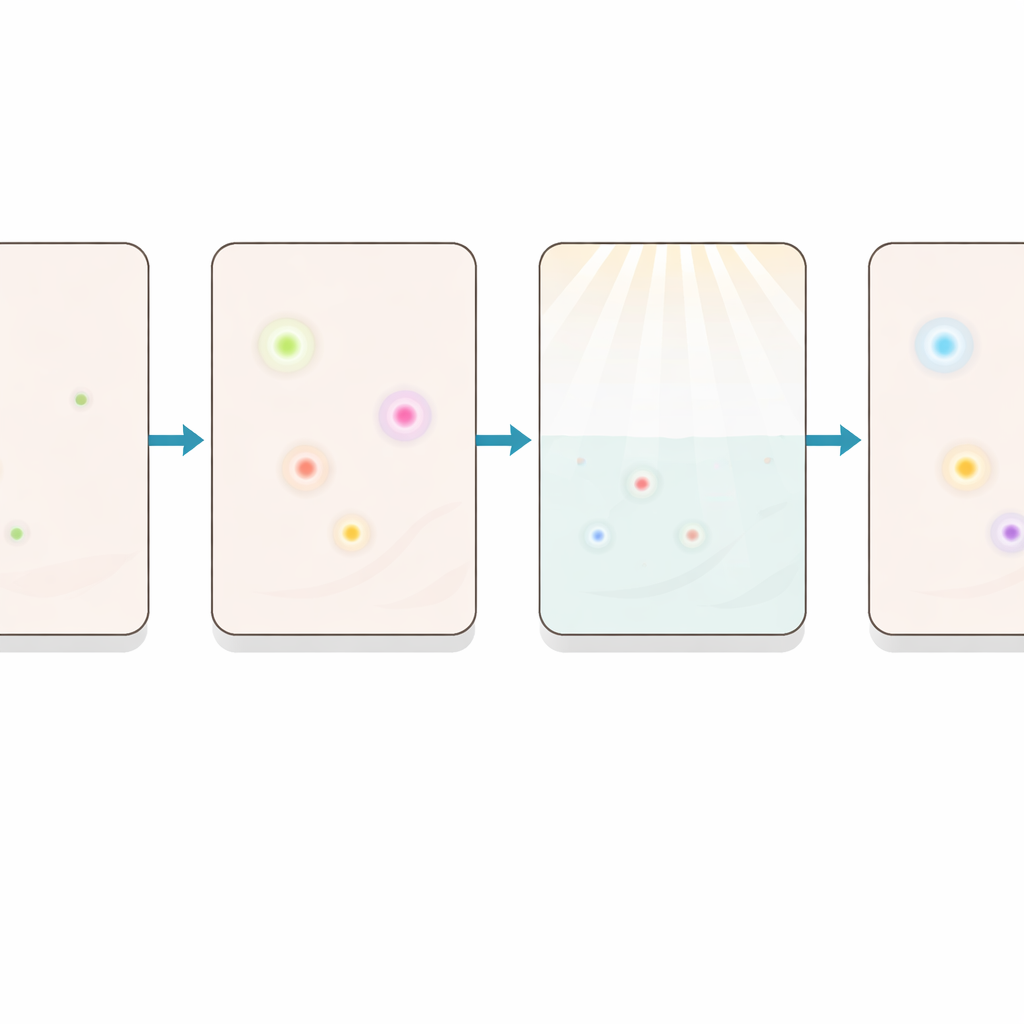
Una finestra versatile sui segnali sottili della malattia
Infine, il gruppo ha applicato iCLAP a una gamma di tessuti normali e tumorali provenienti da organi come seno, fegato, cervice, ovaio e pelle. In questi campioni, i tumori mostravano segnali di marcatori di senescenza molto più intensi rispetto al tessuto sano circostante, sottolineando il potenziale del metodo per la ricerca sul cancro. Rendendo visibili proteine a basso livello pur preservando la possibilità di osservare decine di marcatori contemporaneamente, iCLAP trasforma i campioni clinici d’archivio in mappe ricche e ad alta dimensionalità di stati e vicinanze cellulari. Per i non specialisti, il messaggio chiave è che molti segnali cruciali delle malattie sono stati nascosti alla vista nelle collezioni di tessuti esistenti — e questo nuovo approccio offre un modo praticabile per rivelarli.
Citazione: Wu, F., Zheng, S., Chen, Y. et al. iCLAP: an innovative method for integrable co-detection of low-abundance antigens with high-plex immunostaining. Nat Commun 17, 3104 (2026). https://doi.org/10.1038/s41467-026-69752-y
Parole chiave: proteomica spaziale, senescenza cellulare, imaging multiplex, tessuto FFPE, isole pancreatiche