Clear Sky Science · pl
Nowe zintegrowane podejście genetyczno-transkryptomiczne do badania DUX4 i DUX4C
Geny na krawędzi naszych chromosomów
Na samych końcach chromosomów znajdują się odcinki silnie powtarzalnego DNA, które są wyjątkowo trudne do zbadania. W tym labiryncie mieszczą się dwa geny, DUX4 i DUX4C, powiązane z pewną postacią dystrofii mięśniowej oraz z kilkoma nowotworami, lecz ich dokładna rola pozostawała niejasna, ponieważ standardowe narzędzia genetyczne mają trudność z ich rozróżnieniem. To badanie przedstawia nowe sposoby odczytu i interpretacji tych złożonych regionów, ujawniając, jak różne warianty DUX4 i DUX4C mogą kształtować ryzyko choroby i zachowania układu odpornościowego.
Rozplątywanie dwóch podobnych genów
DUX4 i DUX4C znajdują się blisko siebie przy końcu chromosomu 4, otoczone dziesiątkami niemal identycznych jednostek powtórzeniowych. Krótkodystansowe sekwencjonowanie DNA, podstawowe narzędzie współczesnej genetyki, często nie potrafi rozróżnić tych powtórzeń, ani DUX4 od DUX4C, ani ich licznych krewnych rozproszonych po genomie. Aby to obejść, badacze połączyli sekwencjonowanie długodystansowe i krótkodystansowe, aby odtworzyć pełne sekwencje najczęstszych wersji, czyli haplotypów, DUX4 i DUX4C. Następnie zbudowali niestandardowy genom referencyjny, nazwany D4Ref-T2T, który zastępuje mylący blok powtórzeń jasno zdefiniowanymi kopiami każdego głównego haplotypu, pozwalając na precyzyjniejsze mapowanie standardowych danych sekwencyjnych.
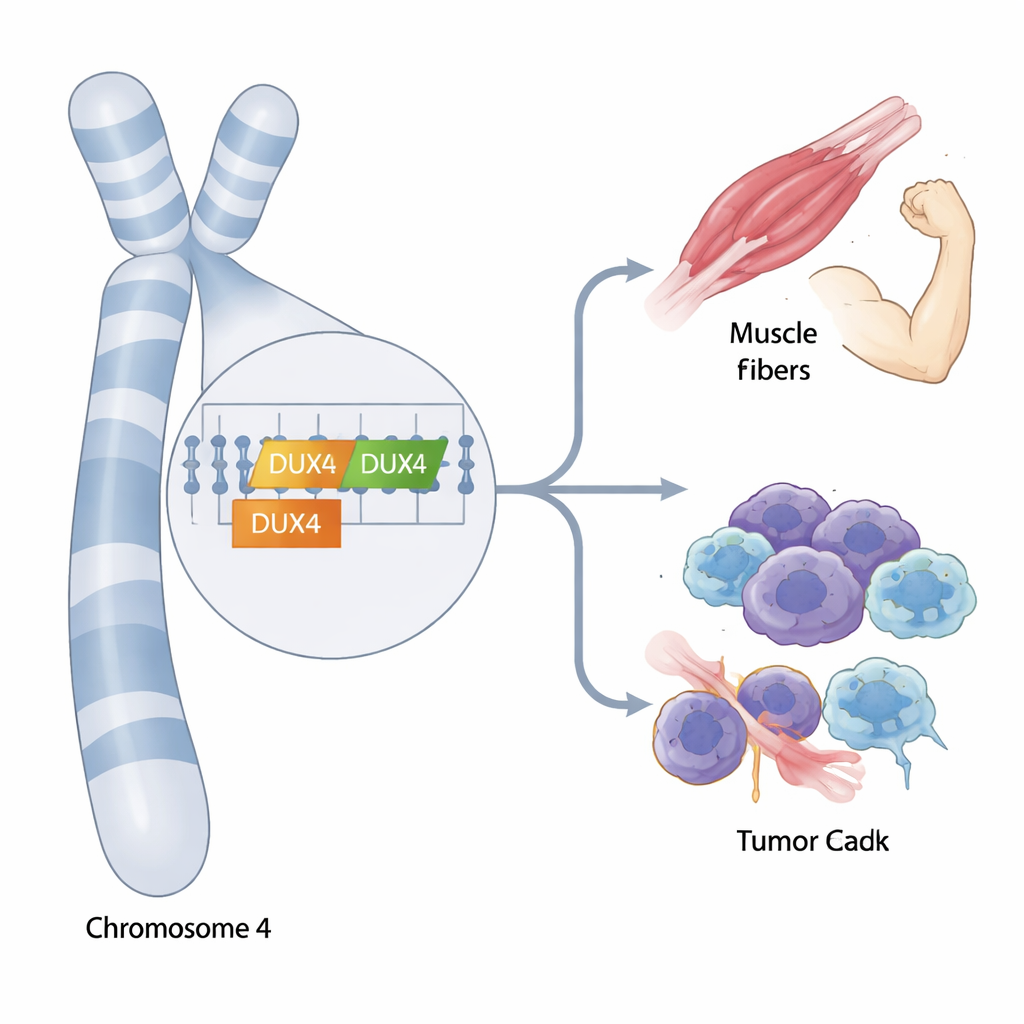
Wspólne warianty genów i kto je nosi
Wykorzystując duże publiczne zbiory danych z populacji europejskich i japońskich, zespół zidentyfikował dwa główne haplotypy DUX4C, które określili jako 4qα i 4qβ. Wersje te różnią się kilkoma zmianami w regionie regulacyjnym blisko końca genu i występują w podobnych częstościach zarówno u Europejczyków, jak i u Japończyków. Analizując DUX4, potwierdzili, że istniejące genomy referencyjne wiernie odzwierciedlają tylko niektóre jego formy, a jeden szeroko stosowany referencyjny zestaw błędnie umieszcza fragmenty haplotypu DUX4 powiązanego z chorobą. Dzięki nowemu referencyjnemu D4Ref-T2T mogli bardziej wiarygodnie genotypować oba geny i odkryli, że wariant DUX4C-4qα ma tendencję do występowania w parze z określonym wariantem DUX4, nazwanym 4qB, wykazując silne sprzężenie genetyczne między tymi locusami.
Nowe komunikaty od DUX4C
Ponad samym DNA, naukowcy zbadali, jak DUX4C jest transkryptowany na RNA w żywych komórkach. Wykorzystując długodystansowe sekwencjonowanie RNA w ludzkich liniach komórek układu odpornościowego stymulowanych interferonem, odtworzyli pełnej długości transkrypty DUX4C i odkryli dwa wcześniej niecharakteryzowane izoformy RNA z wyraźnie określonymi regionami startu i końca. Te izoformy kodują białko, które dzieli te same domeny wiążące DNA co DUX4, ale pozbawione jest jego klasycznego ogona aktywacyjnego. Zamiast tego ogon DUX4C jest wewnętrznie nieuporządkowany i pełen krótkich motywów sekwencyjnych, które często służą jako elastyczne miejsca dokowania dla innych białek i cząsteczek sygnałowych, co sugeruje, że DUX4C może pełnić rolę węzła regulacyjnego zamiast prostego przełącznika włącz/wyłącz geny.
Gdzie i kiedy geny się włączają
Zespół zapytał następnie, kiedy DUX4 i DUX4C są faktycznie ekspresjonowane w ludzkich tkankach. Poprzez ponowną analizę danych RNA z guzów piersi, biopsji mięśni pacjentów z facioscapulohumeral muscular dystrophy (FSHD) oraz linii komórek odpornościowych stymulowanych interferonem, znaleźli różne wzorce. Zarówno DUX4, jak i DUX4C były podwyższone w guzach piersi w porównaniu do prawidłowej tkanki piersi, podczas gdy tylko DUX4 był konsekwentnie zwiększony w mięśniach pacjentów z FSHD. DUX4C był w dużej mierze cichy w próbkach FSHD, choć u kilku nieobjętych chorobą członków rodzin odnotowano umiarkowane poziomy, co sugeruje, że może być mniej szkodliwy dla mięśni niż DUX4 lub nawet odgrywać rolę ochronną bądź naprawczą. W liniach komórek odpornościowych żaden z genów nie był silnie indukowany jedynie przez leczenie interferonem.
Wskazówki dotyczące roli kierującej układem odpornościowym
Na koniec badacze skupili się na niewielkim zestawie linii komórkowych układu odpornościowego, które różniły się zarówno haplotypami DUX4C i DUX4, jak i tym, czy DUX4C był eksprymowany. Komórki noszące kombinację DUX4C-4qα / DUX4-4qB i aktywnie eksprymujące DUX4C wykazywały zwiększoną aktywność genów zaangażowanych w ruch komórek odpornościowych, takich jak chemotaksja leukocytów i limfocytów. To, wraz z motywami sygnalizacyjnymi znalezionymi w ogonie białka DUX4C, sugeruje, że DUX4C może pomagać kierować migracją lub aktywacją komórek odpornościowych w określonych podłożach genetycznych, potencjalnie wpływając na sposób, w jaki guzy i zapalone tkanki są nadzorowane przez układ odpornościowy.
Dlaczego ta praca ma znaczenie
Poprzez zbudowanie dostosowanych map genetycznych i transkryptomicznych dla DUX4 i DUX4C, to badanie dostarcza narzędzi do jasnego zobaczenia jednego z najbardziej powtarzalnych i podatnych na błędy zakątków ludzkiego genomu. Wyniki pokazują, że różne wersje tych genów są ściśle sprzężone i mogą działać przeciwstawnie: DUX4 jako znany sprawca uszkodzeń mięśni i tłumienia odporności, oraz DUX4C jako potencjalny modulator sygnalizacji immunologicznej i ruchu komórek. Te spostrzeżenia otwierają drogę do lepszej diagnostyki genetycznej FSHD, dokładniejszej interpretacji danych sekwencjonowania w onkologii oraz przyszłych badań nad tym, jak subtelne różnice na końcach chromosomów mogą przechylić równowagę między uszkodzeniem tkanek, naprawą i obroną immunologiczną.
Cytowanie: Zhuang, Z., Ueda, M.T., Yamaguchi, K. et al. A new integrated genetic and transcriptomic approach for investigating DUX4 and DUX4C. J Hum Genet 71, 373–381 (2026). https://doi.org/10.1038/s10038-025-01450-x
Słowa kluczowe: DUX4, DUX4C, miopatia obręczowo-twarzowo-ramienna (FSHD), rak piersi, chemotaksja immunologiczna