Clear Sky Science · de
Ein neues integriertes genetisches und transkriptomisches Vorgehen zur Untersuchung von DUX4 und DUX4C
Gene am Rand unserer Chromosomen
An den äußersten Enden unserer Chromosomen finden sich Abschnitte hoch repetitiver DNA, die notorisch schwer zu untersuchen sind. Zwei Gene, die sich in diesem Geflecht verbergen — DUX4 und DUX4C — werden mit einer Form der Muskeldystrophie und mit mehreren Krebsarten in Verbindung gebracht, doch ihre genauen Funktionen blieben unklar, weil gängige genetische Werkzeuge Probleme haben, sie zu unterscheiden. Diese Studie stellt neue Methoden vor, um diese verwirrenden Regionen zu lesen und zu interpretieren, und zeigt, wie verschiedene Varianten von DUX4 und DUX4C das Krankheitsrisiko und das Immunverhalten beeinflussen können.
Die Entwirrung zweier sich ähnelnder Gene
DUX4 und DUX4C liegen nahe beieinander in der Nähe der Spitze von Chromosom 4, umgeben von Dutzenden nahezu identischer Wiederholungseinheiten. Kurzread-DNA-Sequenzierung, das Arbeitspferd der modernen Genetik, kann häufig nicht zwischen diesen Repeats, zwischen DUX4 und DUX4C oder ihren vielen Verwandten im Genom unterscheiden. Um dies zu überwinden, kombinierten die Forschenden Langread- und Kurzread-Sequenzierung, um die vollständigen Sequenzen der häufigsten Varianten, also Haplotypen, von DUX4 und DUX4C zu rekonstruieren. Anschließend bauten sie ein maßgeschneidertes Referenzgenom, genannt D4Ref-T2T, das den verwirrenden Repeats-Block durch klar definierte Kopien jedes Haupt-Haplotyps ersetzt und so erlaubt, Standardsequenzdaten präziser zuzuordnen.
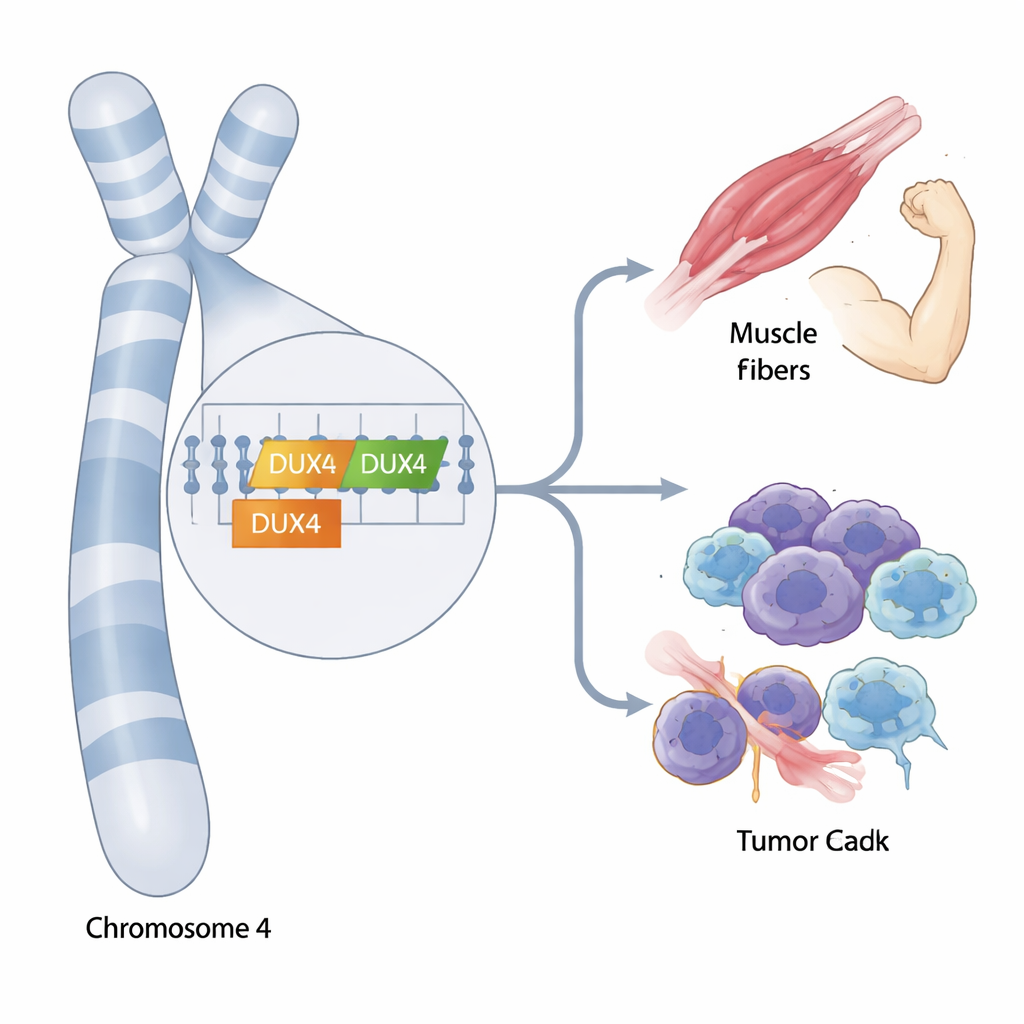
Häufige Genvarianten und wer sie trägt
Anhand großer öffentlicher Datensätze aus europäischen und japanischen Populationen identifizierte das Team zwei Haupt-Haplotypen von DUX4C, die sie 4qα und 4qβ nannten. Diese Versionen unterscheiden sich durch eine Handvoll DNA-Veränderungen in einer regulatorischen Region nahe dem Ende des Gens und kommen bei Europäern und Japanern in ähnlicher Häufigkeit vor. Bei der Untersuchung von DUX4 bestätigten sie, dass existierende Referenzgenome nur einige seiner Formen korrekt abbilden und dass ein weit verbreitetes Referenzgenom Teile des mit Krankheit assoziierten DUX4-Haplotyps fehlplatziert. Mit ihrem neuen D4Ref-T2T-Referenzgenom konnten sie beide Gene zuverlässiger genotypisieren und entdeckten, dass die DUX4C-4qα-Variante häufig gemeinsam mit einer bestimmten DUX4-Variante, genannt 4qB, auftritt, was auf eine starke genetische Kopplung zwischen den beiden Loci hinweist.
Neue Botschaften von DUX4C
Über die DNA hinaus untersuchten die Wissenschaftler, wie DUX4C in lebenden Zellen in RNA transkribiert wird. Mithilfe von Langread-RNA-Sequenzierung in mit Interferon stimulierten menschlichen Immunzelllinien rekonstruierten sie vollständige DUX4C-Transkripte und entdeckten zwei zuvor nicht charakterisierte RNA-Isoformen mit klar definierten Start- und Endregionen. Diese Isoformen kodieren für ein Protein, das dieselben DNA-Bindedomänen wie DUX4 besitzt, jedoch auf dessen klassisches Aktivierungsschwanzstück verzichtet. Stattdessen ist der Schwanz von DUX4C intrinsisch ungeordnet und reich an kurzen Sequenzmotiven, die häufig als flexible Andockstellen für andere Proteine und Signalstoffe dienen — ein Hinweis darauf, dass DUX4C eher als regulatorischer Knotenpunkt denn als einfacher Ein/Aus-Schalter für Gene fungieren könnte.
Wo und wann die Gene angeschaltet werden
Das Team fragte dann, wann DUX4 und DUX4C tatsächlich in menschlichem Gewebe exprimiert werden. Durch die Reanalyse von RNA-Daten aus Brusttumoren, Muskelbiopsien von Patient:innen mit fascioskapulohumeraler Muskeldystrophie (FSHD) und interferon-stimulierten Immunzelllinien fanden sie unterschiedliche Muster. Sowohl DUX4 als auch DUX4C waren in Brusttumoren gegenüber normalem Brustgewebe erhöht, während nur DUX4 in FSHD-Muskelproben konsistent erhöht war. DUX4C war in FSHD-Proben weitgehend still, obwohl einige nicht betroffene Familienmitglieder moderate Mengen zeigten, was darauf hindeutet, dass es dem Muskel weniger schaden könnte als DUX4 oder sogar eine schützende bzw. reparative Rolle spielen könnte. In Immunzelllinien wurden beide Gene nicht stark allein durch Interferonbehandlung induziert.
Hinweise auf eine immunsteuernde Rolle
Schließlich konzentrierten sich die Forschenden auf eine kleine Gruppe von Immunzelllinien, die sich sowohl in ihren DUX4C- und DUX4-Haplotypen als auch darin unterschieden, ob DUX4C exprimiert wurde. Zellen mit der Kombination DUX4C-4qα / DUX4-4qB und aktiver DUX4C-Expression zeigten eine erhöhte Aktivität von Genen, die an der Bewegung von Immunzellen beteiligt sind, etwa bei der Chemotaxis von Leukozyten und Lymphozyten. Dies zusammen mit den in der Schwanzregion des DUX4C-Proteins gefundenen Signalmotiven deutet darauf hin, dass DUX4C in bestimmten genetischen Hintergründen die Migration oder Aktivierung von Immunzellen lenken könnte und so die Überwachung von Tumoren und entzündeten Geweben durch das Immunsystem beeinflusst.
Warum diese Arbeit wichtig ist
Indem sie maßgeschneiderte genetische und transkriptomische Karten für DUX4 und DUX4C erstellten, liefert diese Studie Werkzeuge, um klar in eine der repetitivsten und fehleranfälligsten Ecken des menschlichen Genoms zu blicken. Die Ergebnisse zeigen, dass verschiedene Varianten dieser Gene eng gekoppelt sind und sich möglicherweise gegensätzlich verhalten: DUX4 als bekannter Treiber von Muskelschäden und Immununterdrückung, und DUX4C als möglicher Modulator von Immun‑Signalen und Zellbewegung. Diese Erkenntnisse ebnen den Weg für bessere genetische Diagnosen von FSHD, eine genauere Interpretation von Krebssequenzierungsdaten und weitere Untersuchungen dazu, wie subtile Unterschiede an Chromosomenenden das Gleichgewicht zwischen Gewebeschädigung, Reparatur und Immunabwehr verschieben können.
Zitation: Zhuang, Z., Ueda, M.T., Yamaguchi, K. et al. A new integrated genetic and transcriptomic approach for investigating DUX4 and DUX4C. J Hum Genet 71, 373–381 (2026). https://doi.org/10.1038/s10038-025-01450-x
Schlüsselwörter: DUX4, DUX4C, fascioskapulohumerale Muskeldystrophie, Brustkrebs, Immunchemotaxis