Clear Sky Science · nl
Beschermende rol van natriumpropionaat tegen door glycerol of gefractioneerde doses gammastraling veroorzaakte acute nierschade via ATF5-geïnduceerde mitofagie bij ratten
Waarom nierschade ertoe doet
Acute nierschade is een plotseling falen van het filtratiesysteem van het lichaam en kan optreden na blootstelling aan bepaalde geneesmiddelen, ernstig spierletsel of medische bestraling. Wanneer de nieren falen, stapelen afvalstoffen zich binnen uren tot dagen in het bloed op, waardoor patiënten vaak op de intensivecare belanden. Deze studie onderzoekt of een eenvoudig darmafgeleid molecuul, natriumpropionaat — een korteketenvetzuur dat ontstaat bij de fermentatie van voedingsvezels — de nieren kan beschermen tegen twee zeer verschillende maar klinisch relevante typen schade bij ratten: een veroorzaakt door een spierafbrekende toxine (glycerol) en de ander door herhaalde doses gammastraling.
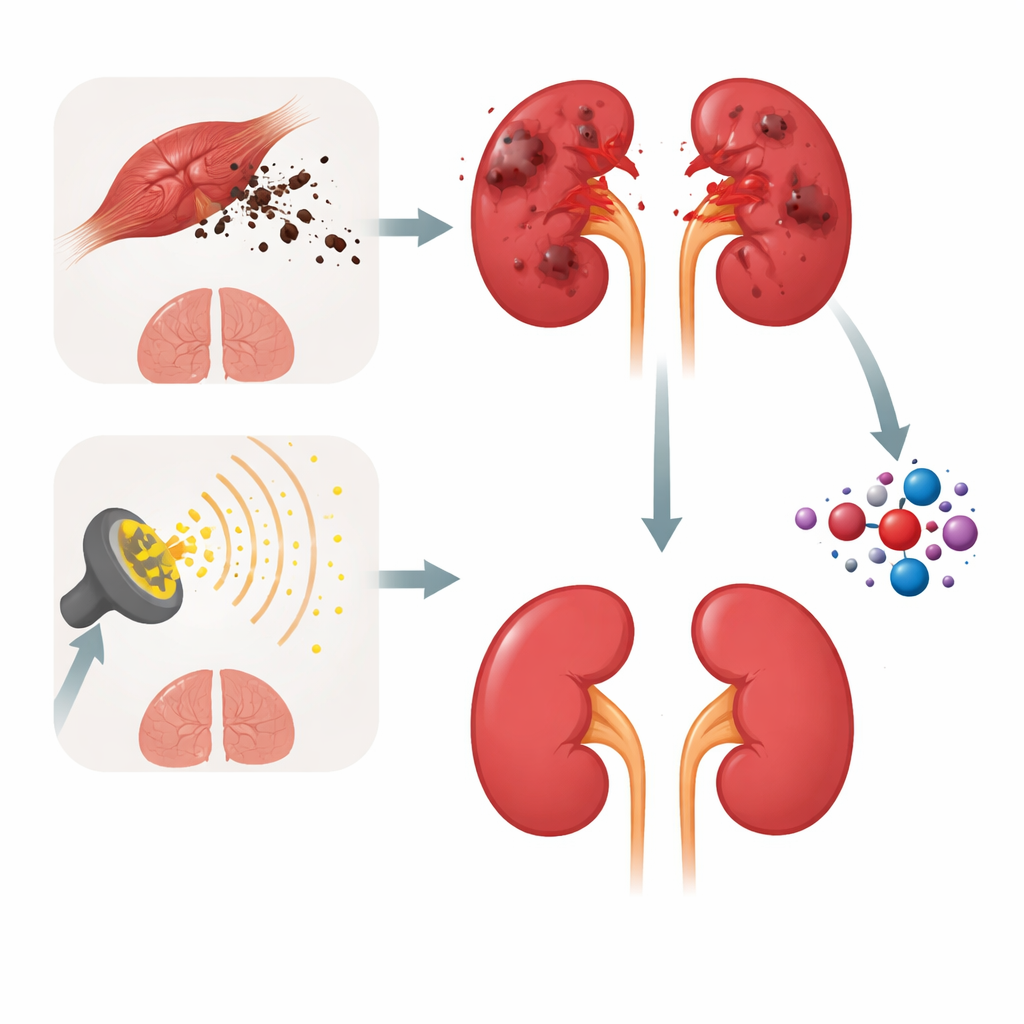
Twee manieren om hetzelfde orgaan te beschadigen
De onderzoekers gebruikten twee erkende experimentele routes om ratnieren te beschadigen. In de ene veroorzaakte een hoge dosis glycerol ernstige spierafbraak, waardoor spierpigmenten en andere verbindingen in de bloedbaan terechtkwamen die de fijne tubuli van de nier verstoppen en vergiftigen. In de andere kregen de dieren meerdere kleinere doses totaallichaams-gammastraling, wat de gefractioneerde blootstellingen nabootst die in radiotherapie worden gebruikt. Hoewel deze verwondingen uit heel verschillende bronnen voortkomen — skeletspier versus stralingsbundels — komen ze uit op hetzelfde resultaat: ontstoken, slecht functionerende nieren, met stijgende bloedureum- en creatinineniveaus en duidelijke tekenen van structurele schade onder de microscoop.
Een eenvoudig molecuul uit de darm
Natriumpropionaat wordt normaal gesproken geproduceerd door darmbacteriën bij de vertering van voedingsvezels. Het is in verband gebracht met lagere ontsteking en betere antioxidantverdediging in verschillende weefsels, maar de rol ervan bij nierbescherming en specifiek bij het opruimen van beschadigde mitochondriën was niet getest in dit soort acute verwondingen. Hier kregen ratten natriumpropionaat oraal toegediend, gedurende of na blootstelling aan glycerol of gammastraling. De behandelingsdosis was bescheiden en werd twee weken gegeven, wat een praktisch supplementatieschema nabootst in plaats van een eenmalige experimentele injectie.
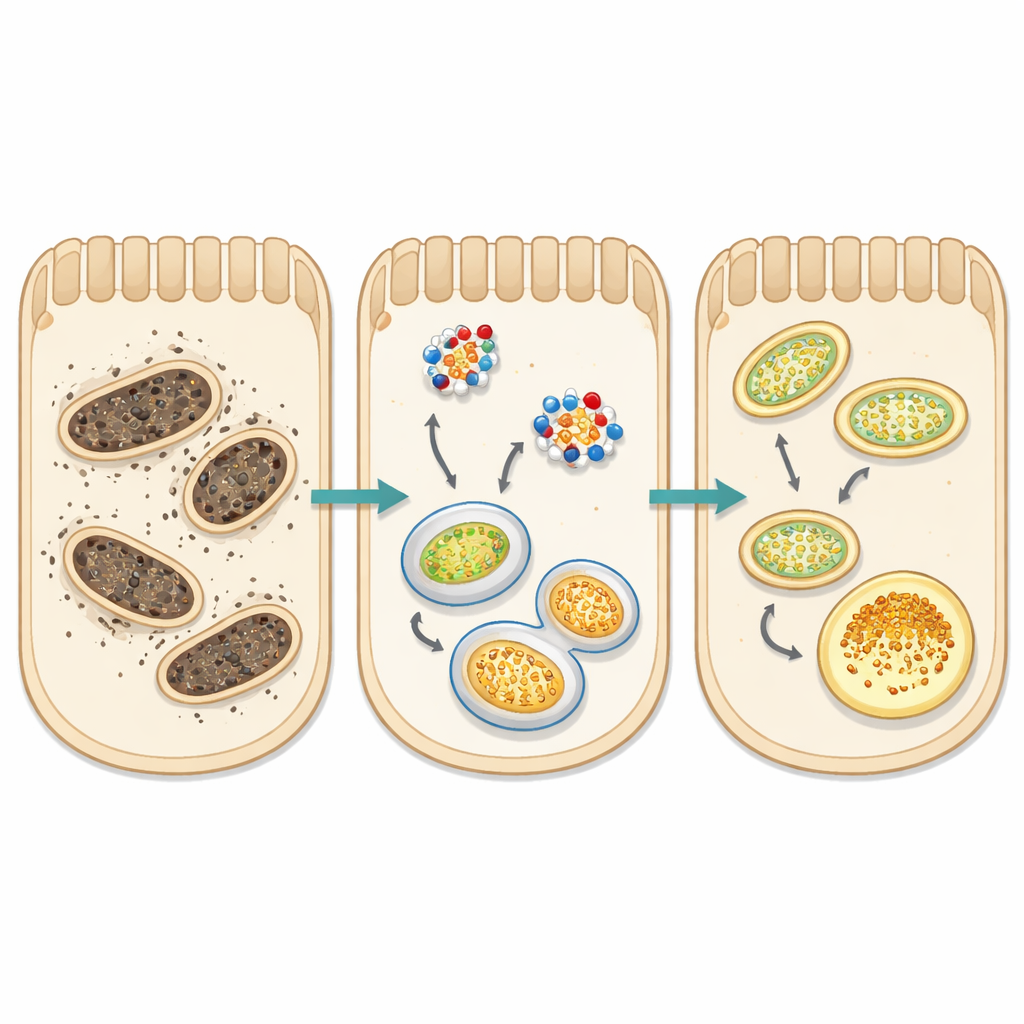
Het blussen van oxidatief vuur in niercellen
Zowel glycerol als straling overspoelden niercellen met reactieve zuurstofsoorten — zeer reactieve moleculen die vetten, eiwitten en DNA beschadigen. Het team mat verschillende sporen van dit oxidatieve vuur: malondialdehyde en lipofuscine (afbraakproducten van beschadigde vetten), proteïnecarbonyls (aangetaste eiwitten) en een belangrijk reparatie-enzym genaamd MSRA. Gewonde ratten vertoonden hogere niveaus van schade-indicatoren en uitgeputte antioxidantverdedigingen. Behandeling met natriumpropionaat keerde dit patroon grotendeels om. Schademarkers daalden, terwijl beschermende moleculen zoals glutathion en MSRA herstelden, wat aangeeft dat de interne chemie van de nieren weer naar balans verschuift. Onder de microscoop toonden nieren van behandelde ratten minder dode tubulaire cellen, minder vervorming van de filtratiestructuren en veel minder congestie en littekenvorming.
Helpen cellen hun energiecentrales recyclen
Een centraal aandachtspunt van de studie was mitofagie — het selectieve recyclesysteem van de cel voor versleten mitochondriën, de energieproducerende “krachtcentrales”. In gezonde cellen worden beschadigde mitochondriën gemarkeerd door eiwitten zoals PINK1, ingepakt in membranen gemarkeerd met LC3 en afgeleverd bij cellulaire recyclagecentra. In beide verwondingsmodellen was dit proces verstoord: PINK1-niveaus daalden, de LC3-balans suggereerde vastgelopen autofagie, en een adaptor-eiwit genaamd p62 stapelde zich op in plaats van te worden verwijderd. Tegelijkertijd stegen de niveaus van ATF5, een stresssignaal gekoppeld aan overbelaste mitochondriën, sterk. Natriumpropionaat bracht deze signalen grotendeels weer in balans: het verhoogde PINK1, herstelde de LC3-balans, verminderde p62-opstapeling en verlaagde ATF5. Samen met de vermindering van oxidatieve stress wijzen deze veranderingen op een hernieuwd kwaliteitssysteem voor mitochondriën, waardoor niercellen beschadigde krachtcentrales kunnen verwijderen voordat ze verdere schade veroorzaken.
Wat dit voor patiënten zou kunnen betekenen
Voor niet-specialisten is de kernboodschap dat een klein, van nature voorkomend molecuul gerelateerd aan vezelvertering de nieren van ratten hielp twee zeer verschillende typen acute aanvallen te weerstaan. Door zowel oxidatieve stress te verminderen als het interne recyclesysteem van de cel voor beschadigde mitochondriën te herstarten, behield natriumpropionaat de nierstructuur en -functie in situaties die toxine-geïnduceerde spierafbraak en bestraling nabootsen. Hoewel deze resultaten nog in dieren en in een vroeg stadium zijn, bieden ze een mechanismenkaart voor het verkennen van natriumpropionaat, of soortgelijke korteketenvetzuren, als ondersteunende therapieën om nierschade te verminderen in hoog-risico klinische situaties zoals intensivecare, zwaar trauma of kankerbestraling.
Bronvermelding: Habieb, M.E., Ali, M.M., Abd-ElRaouf, A. et al. Protective role of sodium propionate against glycerol or fractionated doses of gamma rays-induced acute kidney injury via ATF5-induced mitophagy in rats. Sci Rep 16, 12073 (2026). https://doi.org/10.1038/s41598-026-46553-3
Trefwoorden: acute nierschade, natriumpropionaat, oxidatieve stress, mitofagie, gamma-straling