Clear Sky Science · de
Schützende Rolle von Natriumpropionat gegen durch Glycerin oder fraktionierte Dosen von Gammastrahlen induzierte akute Nierenschädigung über ATF5-induzierte Mitophagie bei Ratten
Warum Nierenschäden wichtig sind
Akute Nierenschädigung ist ein plötzlicher Zusammenbruch des Filtersystems des Körpers und kann nach Exposition gegenüber bestimmten Medikamenten, schwerer Muskelschädigung oder medizinischer Strahlung auftreten. Wenn die Nieren versagen, sammeln sich innerhalb von Stunden bis Tagen Abfallprodukte im Blut an, was Patienten häufig auf die Intensivstation bringt. Diese Studie untersucht, ob eine einfache, aus dem Darm stammende Chemikalie — Natriumpropionat, eine kurzkettige Fettsäure, die bei der Fermentation von Ballaststoffen entsteht — die Nieren vor zwei sehr unterschiedlichen, klinisch relevanten Schadensarten bei Ratten schützen kann: einerseits ausgelöst durch ein muskelauflösendes Toxin (Glycerin), andererseits durch wiederholte Dosen von Gammastrahlung.
Zwei Wege, dasselbe Organ zu schädigen
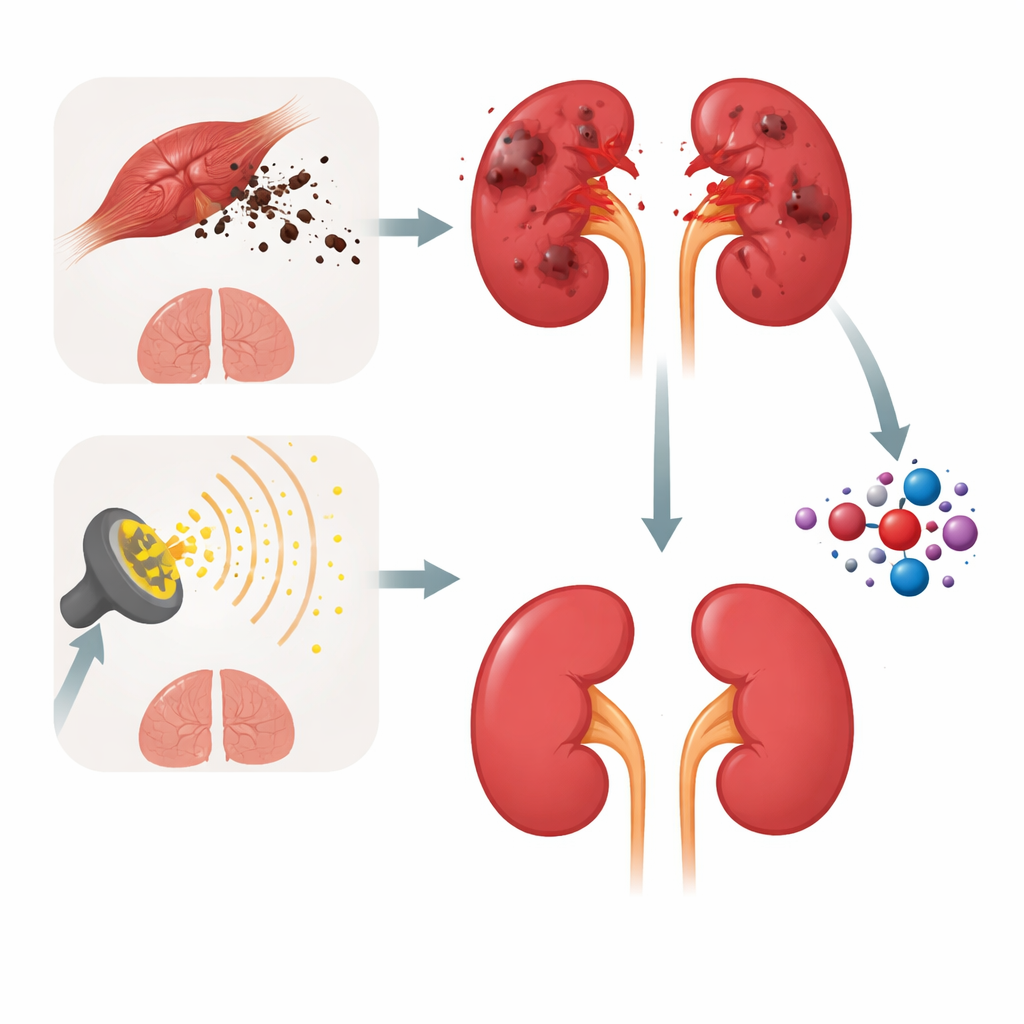
Die Forschenden nutzten zwei etablierte experimentelle Wege, um Rattennieren zu schädigen. In einem Modell führte eine starke Dosis Glycerin zu schwerem Muskelabbau, wodurch Muskelpigmente und andere Verbindungen ins Blut gelangten, die die feinen Tubuli der Niere verstopfen und vergiften. Im anderen Modell erhielten die Tiere mehrere kleinere Ganzkörperdosen von Gammastrahlung, was fraktionierte Expositionen widerspiegelt, wie sie in der Strahlentherapie verwendet werden. Obwohl diese Schäden an sehr unterschiedlichen Orten entstehen — Skelettmuskel versus Strahlenbelastung — konvergieren sie im selben Ergebnis: entzündete, schlecht funktionierende Nieren mit steigenden Harnstoff- und Kreatininwerten im Blut und klaren Anzeichen struktureller Schäden unter dem Mikroskop.
Ein einfaches Molekül aus dem Darm
Natriumpropionat wird normalerweise von Darmbakterien bei der Verdauung von Ballaststoffen produziert. Es wird mit geringerer Entzündung und besseren antioxidativen Abwehrmechanismen in verschiedenen Geweben in Verbindung gebracht, doch seine Rolle beim Nierenschutz und speziell bei der Beseitigung beschädigter Mitochondrien war in diesen akuten Schadensmodellen noch nicht untersucht. In der Studie erhielten Ratten Natriumpropionat oral, entweder während oder nach der Exposition gegenüber Glycerin oder Gammastrahlen. Die Behandlungsdosis war moderat und über zwei Wochen verabreicht, was einem praktischen Supplementierungszeitraum eher entspricht als einer einmaligen experimentellen Injektion.
Den oxidativen Brand in Nierenzellen dämpfen
Sowohl Glycerin als auch Strahlung überschwemmten Nierenzellen mit reaktiven Sauerstoffspezies — hochreaktiven Molekülen, die Fette, Proteine und DNA schädigen. Das Team bestimmte mehrere Spuren dieses oxidativen Schadens: Malondialdehyd und Lipofuszin (Produkte geschädigter Fette), Proteincarbonyle (veränderte Proteine) und ein wichtiges Reparaturenzym namens MSRA. Bei geschädigten Ratten waren die Schadensmarker erhöht und die antioxidativen Abwehrmechanismen erschöpft. Die Behandlung mit Natriumpropionat kehrte viele dieser Veränderungen um. Schadensmarker sanken, während schützende Moleküle wie Glutathion und MSRA sich erholten, was darauf hindeutet, dass die innere Chemie der Niere wieder ins Gleichgewicht zurückkehrte. Unter dem Mikroskop zeigten die Nieren der behandelten Tiere weniger abgestorbene Tubuluszellen, weniger Verzerrung der Filterstrukturen und deutlich weniger Stauungen und Narbenbildung.
Zellen helfen, ihre Kraftwerke zu recyceln
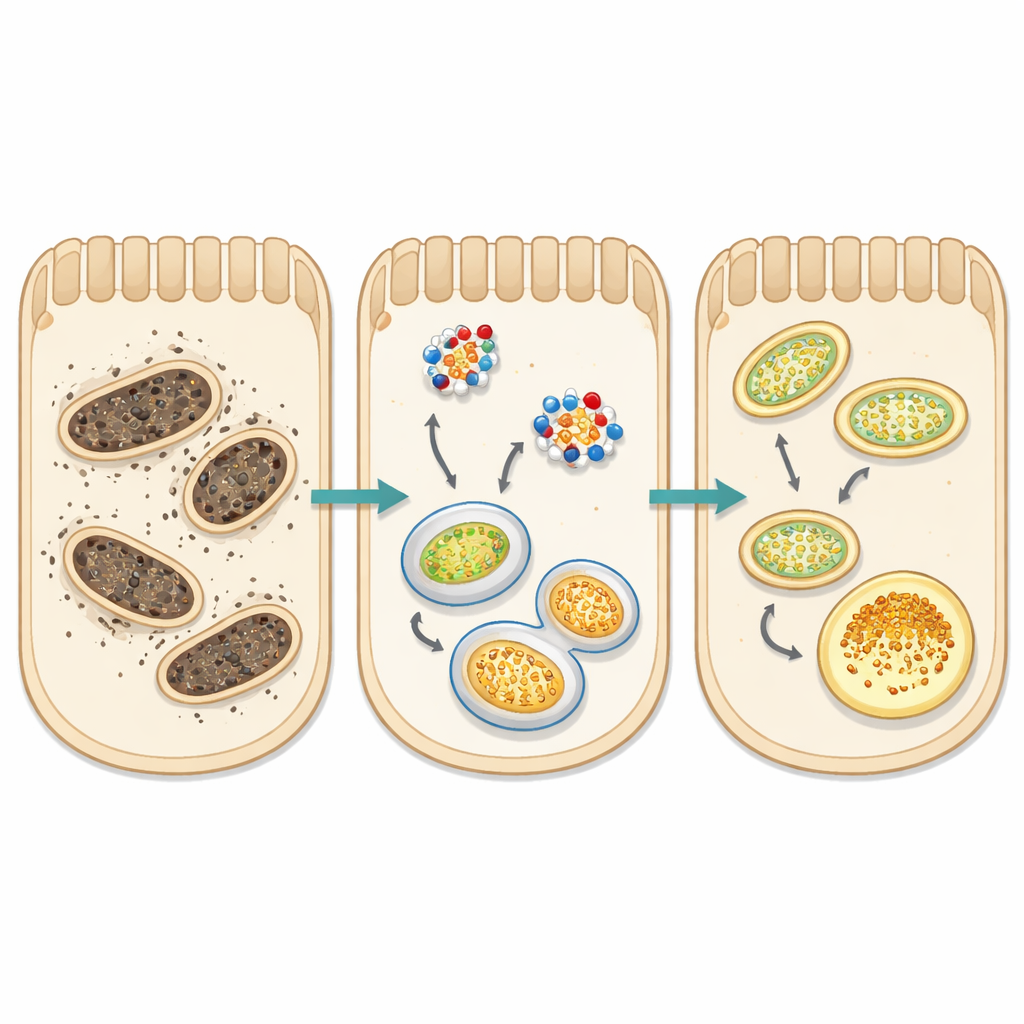
Ein zentraler Fokus der Studie war die Mitophagie — das selektive Recycling-System der Zelle für verschlissene Mitochondrien, die energieliefernden „Kraftwerke“. In gesunden Zellen werden beschädigte Mitochondrien durch Proteine wie PINK1 markiert, in Membranen mit LC3 eingebettet und zu zellulären Recyclingzentren transportiert. In beiden Schadensmodellen war dieser Prozess gestört: PINK1-Spiegel fielen, das Verhältnis der LC3-Formen deutete auf gestörte Autophagie hin, und ein Adapterprotein namens p62 häufte sich an, anstatt abgebaut zu werden. Gleichzeitig stiegen die Werte von ATF5, einem Stresssignal, das mit überlasteten Mitochondrien in Verbindung steht, stark an. Natriumpropionat normalisierte diese Signale weitgehend: Es erhöhte PINK1, stellte das LC3-Gleichgewicht wieder her, verringerte die Akkumulation von p62 und senkte ATF5. Zusammen mit reduziertem oxidativem Stress deuten diese Veränderungen auf ein wiederbelebtes Qualitätskontrollsystem der Mitochondrien hin, das es Nierenzellen ermöglicht, beschädigte Kraftwerke zu entfernen, bevor sie weiteren Schaden auslösen.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nichtfachleute ist die Kernbotschaft, dass ein kleines, natürlich vorkommendes Molekül aus der Ballaststoffverdauung den Rattennieren half, zwei sehr unterschiedliche akute Angriffe zu überstehen. Durch das Abkühlen des oxidativen Stresses und das Wiederanlaufen des zellulären Recyclings beschädigter Mitochondrien bewahrte Natriumpropionat Struktur und Funktion der Niere in Modellen, die Toxin-induzierten Muskelabbau und Strahlenexposition nachahmen. Obwohl diese Ergebnisse noch an Tieren und in einem frühen Stadium sind, liefern sie eine mechanistische Grundlage, um Natriumpropionat oder ähnliche kurzkettige Fettsäuren als unterstützende Therapien zur Verringerung von Nierenschäden in Hochrisiko-Kliniksituationen wie Intensivmedizin, schweren Traumata oder Krebs-Strahlentherapie weiter zu erforschen.
Zitation: Habieb, M.E., Ali, M.M., Abd-ElRaouf, A. et al. Protective role of sodium propionate against glycerol or fractionated doses of gamma rays-induced acute kidney injury via ATF5-induced mitophagy in rats. Sci Rep 16, 12073 (2026). https://doi.org/10.1038/s41598-026-46553-3
Schlüsselwörter: akute Nierenschädigung, Natriumpropionat, oxidativer Stress, Mitophagie, Gamma-Strahlung