Clear Sky Science · es
Papel protector del propionato de sodio frente a la lesión renal aguda inducida por glicerol o por dosis fraccionadas de rayos gamma mediante la mitofagia inducida por ATF5 en ratas
Por qué importa el daño renal
La lesión renal aguda es un fallo súbito del sistema de filtración del organismo y puede aparecer tras la exposición a ciertos fármacos, un daño muscular severo o radiación médica. Cuando los riñones fallan, los productos de desecho se acumulan en la sangre en cuestión de horas o días, lo que a menudo conduce a la necesidad de cuidados intensivos. Este estudio investiga si una molécula sencilla de origen intestinal, el propionato de sodio —un ácido graso de cadena corta asociado a la fermentación de la fibra dietética— puede proteger los riñones frente a dos tipos de lesión en ratas que son muy diferentes entre sí pero clínicamente relevantes: una desencadenada por una toxina que provoca descomposición muscular (glicerol) y otra por dosis repetidas de radiación gamma.
Dos maneras de dañar el mismo órgano
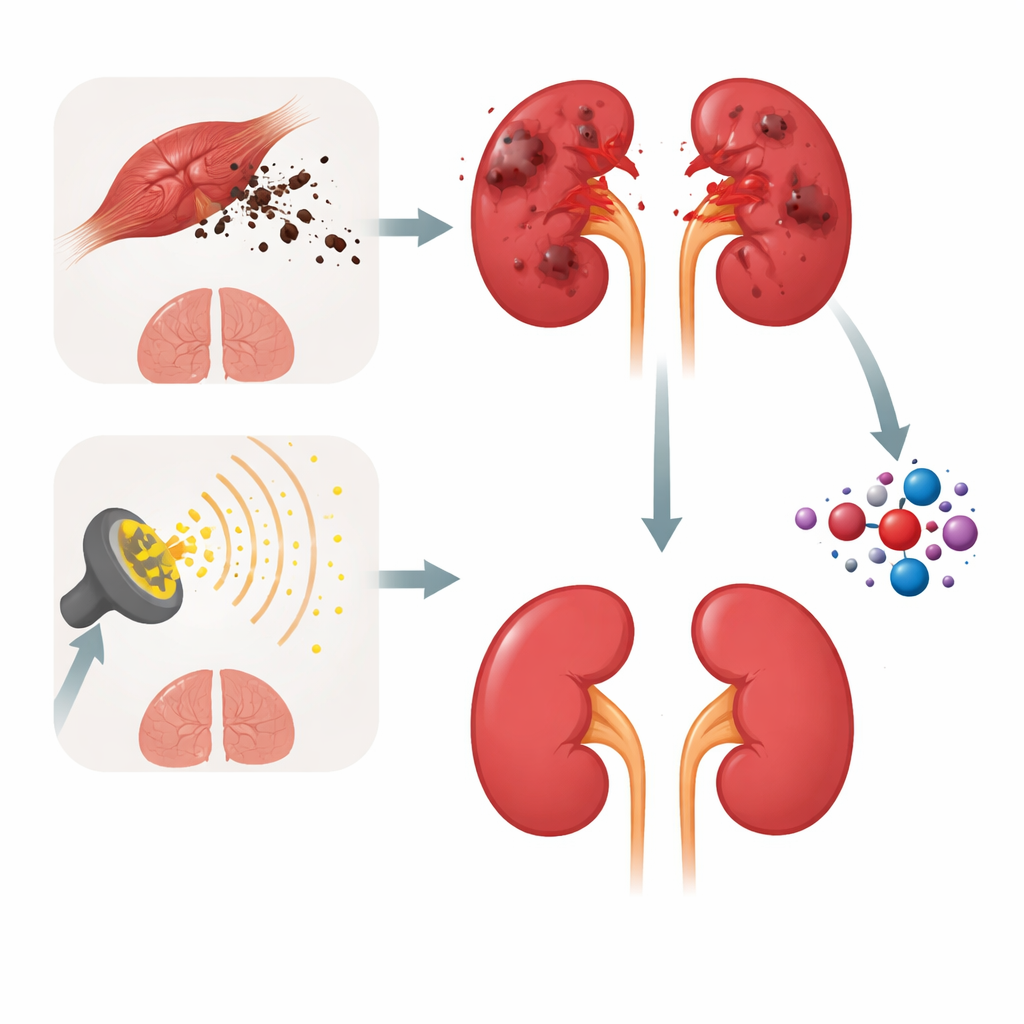
Los investigadores emplearon dos vías experimentales consolidadas para dañar los riñones de las ratas. En una, una dosis alta de glicerol provocó una descomposición muscular severa, inundando el torrente sanguíneo con pigmentos musculares y otros compuestos que obstruyen y envenenan los finos túbulos renales. En la otra, los animales recibieron varias dosis más pequeñas de radiación gamma corporal total, imitando las exposiciones fraccionadas utilizadas en la radioterapia. Aunque estas lesiones se originan en lugares muy distintos —músculo esquelético frente a haces de radiación— convergen en el mismo resultado: riñones inflamados y con bajo rendimiento, con aumento de la urea y creatinina sanguíneas y signos claros de daño estructural al microscopio.
Una molécula simple procedente del intestino
El propionato de sodio se produce normalmente por bacterias intestinales cuando digieren la fibra dietética. Se ha relacionado con una menor inflamación y mejores defensas antioxidantes en diversos tejidos, pero su papel en la protección renal y, en particular, en la limpieza de mitocondrias dañadas no se había probado en estos tipos de lesión aguda. Aquí, las ratas recibieron propionato de sodio por vía oral durante o después de la exposición a glicerol o rayos gamma. La dosis del tratamiento fue modesta y administrada durante dos semanas, imitando un calendario de suplementación práctico en lugar de una inyección experimental única.
Apagar el fuego oxidativo en las células renales
Tanto el glicerol como la radiación inundaron las células renales con especies reactivas de oxígeno: moléculas muy reactivas que dañan lípidos, proteínas y ADN. El equipo midió varias huellas de este fuego oxidativo: malondialdehído y lipofuscina (productos de lípidos dañados), carbonilos proteicos (proteínas lesionadas) y una enzima reparadora clave llamada MSRA. Las ratas lesionadas mostraron niveles más altos de marcadores de daño y defensas antioxidantes agotadas. El tratamiento con propionato de sodio revirtió gran parte de este patrón. Los marcadores de daño descendieron, mientras que moléculas protectoras como el glutatión y la MSRA se recuperaron, indicando que la química interna del riñón volvía hacia el equilibrio. Al microscopio, los riñones de las ratas tratadas mostraron menos células tubulares muertas, menos distorsión de las estructuras de filtrado y mucha menos congestión y cicatrización.
Ayudar a las células a reciclar sus centrales energéticas
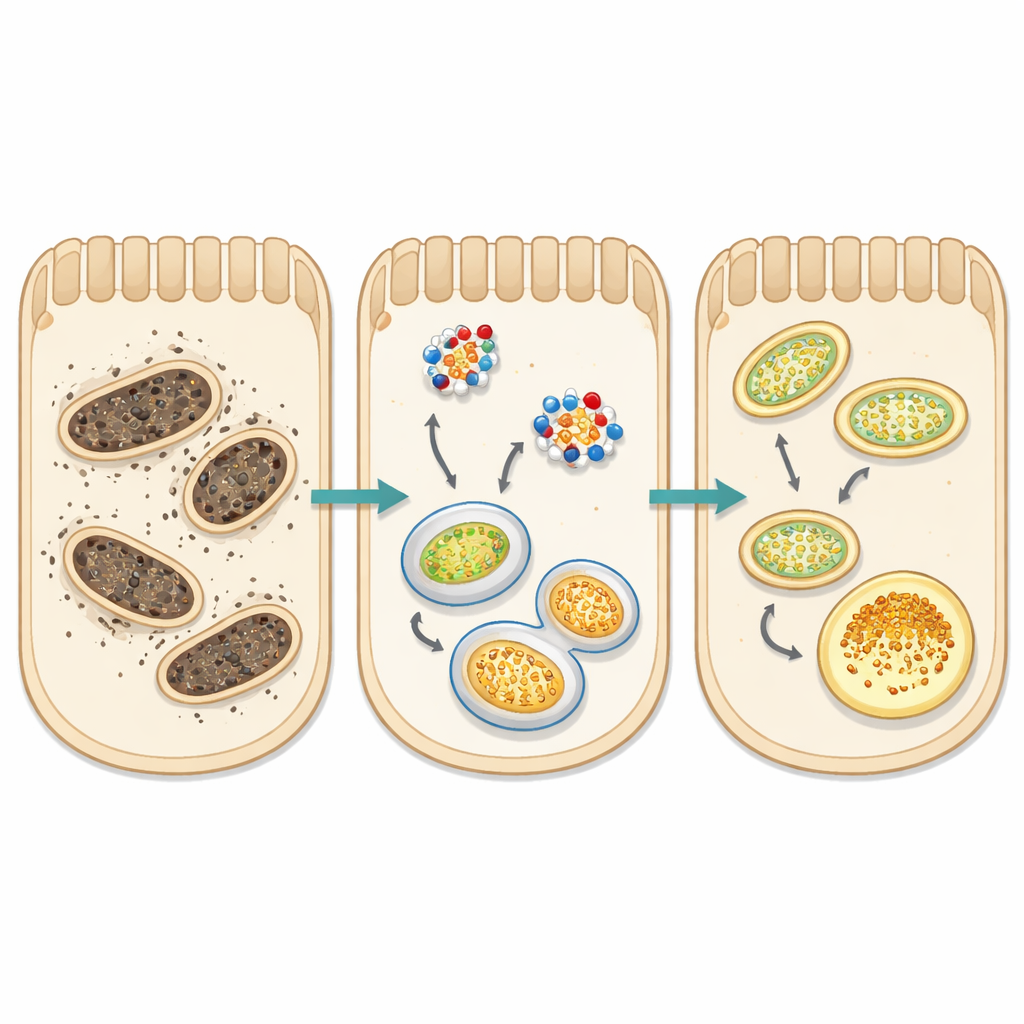
Un foco central del estudio fue la mitofagia: el sistema selectivo de reciclaje celular para mitocondrias envejecidas, las “centrales energéticas” productoras de energía. En células sanas, las mitocondrias dañadas son etiquetadas por proteínas como PINK1, envueltas en membranas marcadas por LC3 y entregadas a los centros de reciclaje celular. En ambos modelos de lesión, este proceso se vio alterado: los niveles de PINK1 disminuyeron, el equilibrio de LC3 sugirió una autophagia bloqueada, y una proteína adaptadora llamada p62 se acumuló en lugar de ser eliminada. Al mismo tiempo, los niveles de ATF5, una señal de estrés ligada a mitocondrias sobrecargadas, aumentaron de forma marcada. El propionato de sodio normalizó en gran medida estas señales: aumentó PINK1, restauró el equilibrio de LC3, redujo la acumulación de p62 y disminuyó ATF5. Junto con la reducción del estrés oxidativo, estos cambios apuntan a un sistema de control de calidad mitocondrial reactivado, que permite a las células renales eliminar las centrales dañadas antes de que causen más daño.
Qué podría significar esto para los pacientes
Para un público no especialista, el mensaje clave es que una pequeña molécula de origen natural relacionada con la digestión de la fibra ayudó a los riñones de ratas a resistir dos tipos muy distintos de ataque agudo. Al enfriar tanto el estrés oxidativo como reactivar el reciclaje interno de mitocondrias dañadas, el propionato de sodio preservó la estructura y la función renal en escenarios que imitan la descomposición muscular inducida por toxinas y la exposición a radiación. Aunque estos resultados aún proceden de estudios en animales y se encuentran en una fase inicial, proporcionan una hoja de ruta mecanística para explorar el propionato de sodio, o ácidos grasos de cadena corta similares, como terapias de apoyo para reducir el daño renal en situaciones clínicas de alto riesgo, como cuidados intensivos, traumatismos graves o radioterapia contra el cáncer.
Cita: Habieb, M.E., Ali, M.M., Abd-ElRaouf, A. et al. Protective role of sodium propionate against glycerol or fractionated doses of gamma rays-induced acute kidney injury via ATF5-induced mitophagy in rats. Sci Rep 16, 12073 (2026). https://doi.org/10.1038/s41598-026-46553-3
Palabras clave: lesión renal aguda, propionato de sodio, estrés oxidativo, mitofagia, radiación gamma