Clear Sky Science · ar
الدور الوقائي لبروبونات الصوديوم ضد الفشل الكلوي الحاد الناتج عن الغليسرول أو جرعات مقسمة من أشعة جاما عبر التحلل البِطَانِي المحدث بواسطة ATF5 في الجرذان
لماذا يهم تلف الكِلية
الفشل الكلوي الحاد هو انهيار مفاجئ في نظام التصفية بالجسم، ويمكن أن يحدث بعد التعرض لبعض الأدوية أو تلف العضلات الشديد أو الإشعاع الطبي. عند فشل الكليتين، تتراكم نفايات الجسم في الدم خلال ساعات إلى أيام، ما يُسفر غالبًا عن إدخال المرضى إلى وحدات العناية المركزة. تستكشف هذه الدراسة ما إذا كانت مادة بسيطة منتجة في الأمعاء، بروبونات الصوديوم — وهي حمض دهني قصير السلسلة مرتبط بتخمّر الألياف الغذائية — يمكن أن تحمي الكليتين من نوعين مختلفين لكن ذوي صلة سريرية من الإصابات في الجرذان: واحد ناتج عن سم يسبب تكسير العضلات (الغليسرول) والآخر ناتج عن جرعات متكررة من أشعة غاما.
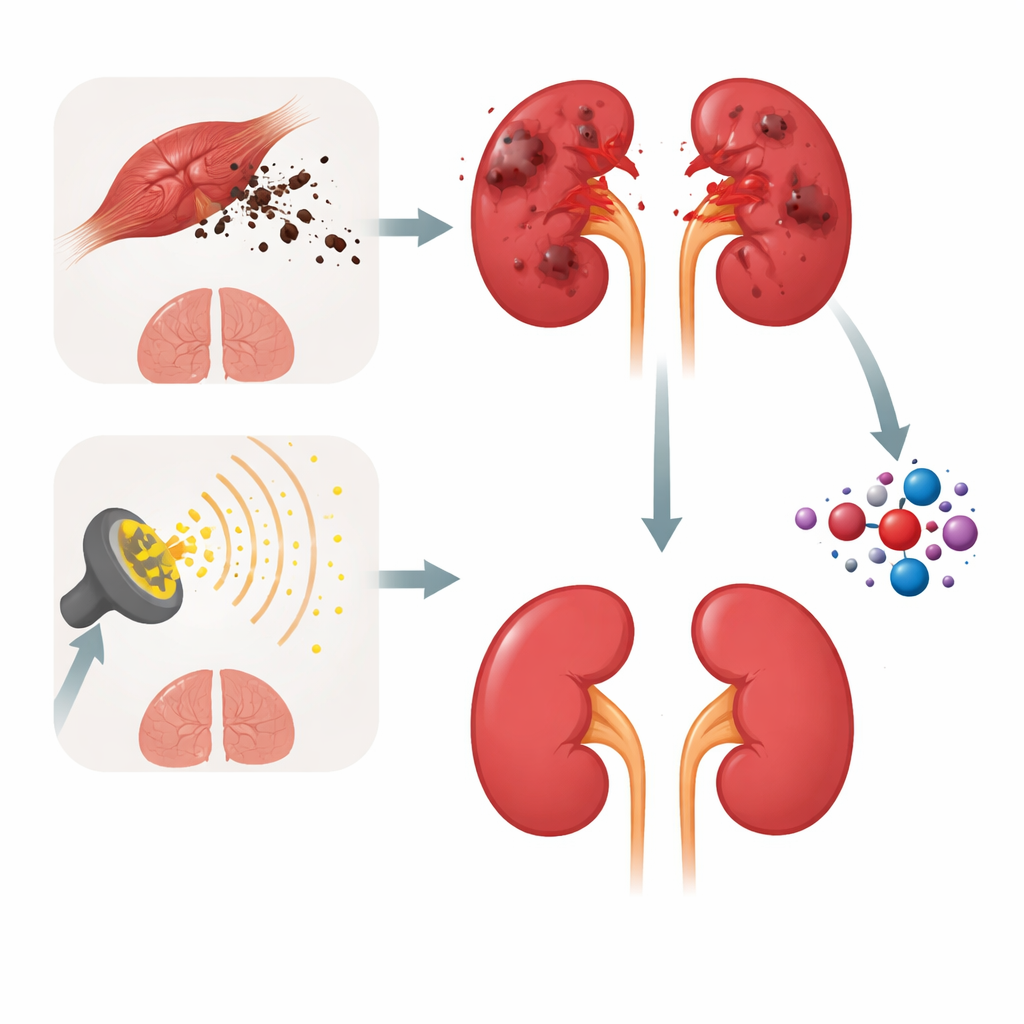
طريقتان لإصابة نفس العضو
استخدم الباحثون مسارين تجريبيين معتمدين لإحداث تلف في كلى الجرذان. في أحدهما، تسببت جرعة قوية من الغليسرول في تكسير شديد للعضلات، مما أغرق مجرى الدم بصبغات ونواتج عضلية أخرى تسد وتسمم الأنابيب الدقيقة للكلية. في الآخر، تلقى الحيوان عدة جرعات أصغر من إشعاع غاما للجسم كله، محاكاة للتعرض المقسّم المستخدم في العلاج الإشعاعي. على الرغم من أن هذه الإصابات تنشأ من مصادر مختلفة — العضلات الهيكلية مقابل حزم الإشعاع — فإنها تتقاطع في نتيجة واحدة: كليتان ملتهبتان ذات أداء ضعيف، مع ارتفاع مستويات اليوريا والكرياتينين في الدم وعلامات واضحة لتلف بنيوي تحت المجهر.
جزيء بسيط من الأمعاء
يُنتَج بروبونات الصوديوم عادة بواسطة بكتيريا الأمعاء عند هضم الألياف الغذائية. رُبطَ بتقليل الالتهاب وتحسين الدفاعات المضادة للأكسدة في أنسجة متعددة، لكن دوره في حماية الكلى وخاصة في تنظيف الميتوكوندريا التالفة لم يُختبر في هذه الأنواع من الإصابات الحادة. هنا، تلقى الجرذان بروبونات الصوديوم عن طريق الفم إما أثناء أو بعد التعرض للغليسرول أو أشعة غاما. كانت جرعة العلاج معتدلة وأعطيت لمدة أسبوعين، محاكاةً لجدول تكميلي عملي بدلاً من حقنة تجريبية لمرة واحدة.
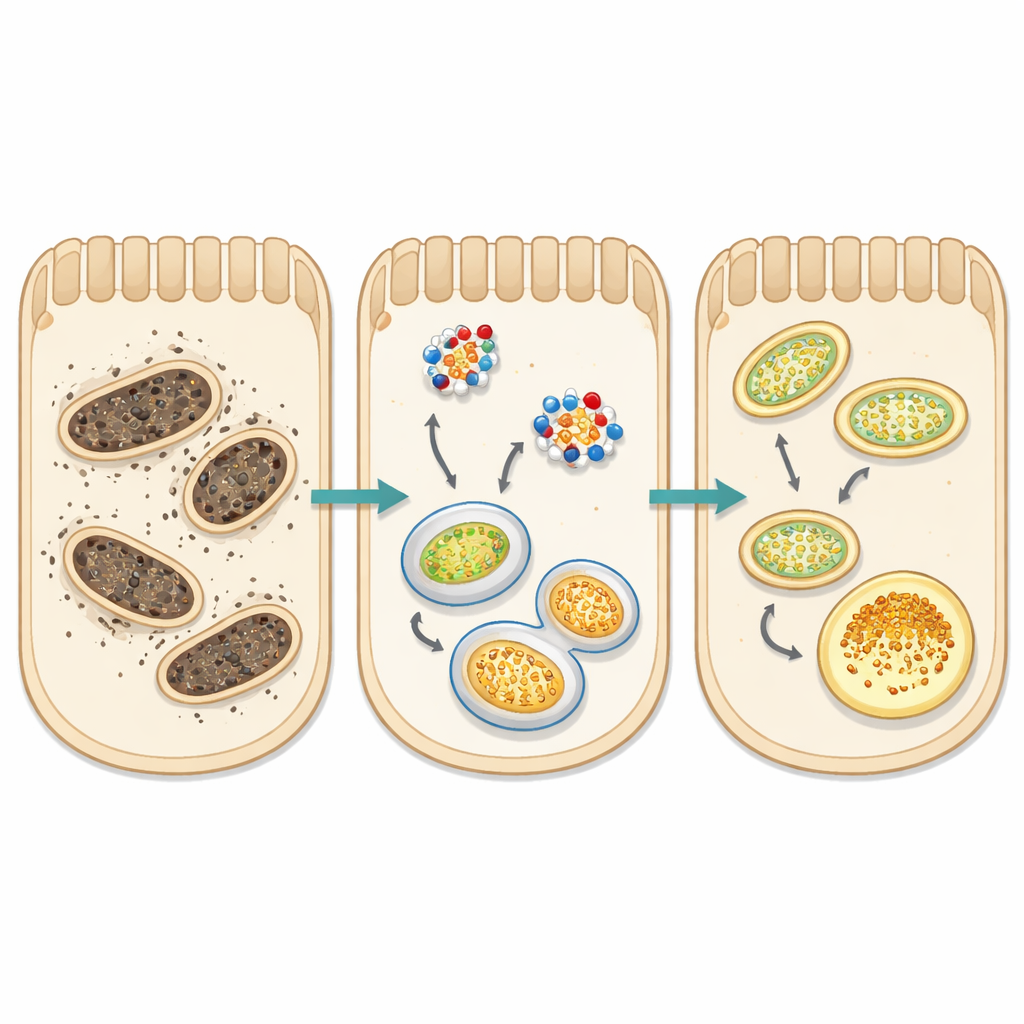
تهدئة الحريق التأكسدي في خلايا الكلى
أغرق كل من الغليسرول والإشعاع خلايا الكلى بجذور الأكسجين التفاعلية — جزيئات شديدة التفاعل تتلف الدهون والبروتينات والحمض النووي. قاس الفريق عدة بصمات لهذا الحريق التأكسدي: المالونالديهيد والليبوفسين (نواتج تلف الدهون)، كربونيلات البروتين (بروتينات متندبة)، وإنزيم إصلاحي رئيسي يدعى MSRA. أظهرت الجرذان المصابة مستويات أعلى من علامات الضرر وضعفًا في دفاعات مضادات الأكسدة. أعاد علاج بروبونات الصوديوم الكثير من هذا النمط إلى الخلف: انخفضت علامات الضرر، بينما تعافىت الجزيئات الوقائية مثل الجلوتاثيون وMSRA، مما يشير إلى أن الكيمياء الداخلية للكلى كانت تعود نحو التوازن. وتحت المجهر، أظهرت كلى الحيوانات المعالجة خلايا أنبوبية ميتة أقل وتشوهًا أقل للهياكل الفلترية وازدحامًا وتليفًا أقل بكثير.
مساعدة الخلايا على إعادة تدوير محركاتها
كان التركيز المركزي للدراسة على التحلل الميتوكوندري — نظام الخلية الانتقائي لإعادة تدوير الميتوكوندريا البالية، «محركات» إنتاج الطاقة. في الخلايا السليمة، تُوسم الميتوكوندريا التالفة بواسطة بروتينات مثل PINK1، وتُحاط بأغشية معنونة بـ LC3، وتُسلم إلى مراكز إعادة التدوير الخلوية. في كلا نموذجَي الإصابة، تعطّل هذا المسار: انخفضت مستويات PINK1، وأشار توازن LC3 إلى توقف السَّلوك الاِبتِلاعي، وتراكم بروتين مستقبل يسمى p62 بدلًا من أن يُزال. وفي الوقت نفسه، ارتفعت مستويات ATF5، إشارة إجهاد مرتبطة بتحميل الميتوكوندريا. أعاد بروبونات الصوديوم هذه الإشارات إلى حد كبير: عزز PINK1، واستعاد توازن LC3، وخفف تراكم p62، وخفض ATF5. جنبًا إلى جنب مع تقلص الإجهاد التأكسدي، تشير هذه التغيرات إلى إحياء نظام نوعية الميتوكوندريا، مما يتيح لخلايا الكلى إزالة المحركات التالفة قبل أن تُحدث أذى إضافيًا.
ما قد يعنيه هذا للمرضى
لغير المتخصصين، الرسالة الأساسية هي أن جزيئًا صغيرًا يحدث طبيعيًا ومرتبط بهضم الألياف ساعد كلى الجرذان على الصمود أمام نوعين مختلفين جدًا من الهجوم الحاد. من خلال كل من تهدئة الإجهاد التأكسدي وإعادة تشغيل آلية إعادة تدوير الميتوكوندريا داخل الخلية، حافظ بروبونات الصوديوم على بنية ووظيفة الكلى في ظروف تحاكي تكسير العضلات الناتج عن السم والتعرض للإشعاع. وعلى الرغم من أن هذه النتائج لا تزال في الحيوانات وفي مرحلة مبكرة، فإنها تقدّم خارطة آلية لاستكشاف بروبونات الصوديوم أو الأحماض الدهنية القصيرة المشابهة كعلاجات داعمة لتقليل تلف الكلى في حالات سريرية عالية المخاطر، مثل العناية المركزة أو الإصابات الكبرى أو العلاج الإشعاعي للسرطان.
الاستشهاد: Habieb, M.E., Ali, M.M., Abd-ElRaouf, A. et al. Protective role of sodium propionate against glycerol or fractionated doses of gamma rays-induced acute kidney injury via ATF5-induced mitophagy in rats. Sci Rep 16, 12073 (2026). https://doi.org/10.1038/s41598-026-46553-3
الكلمات المفتاحية: الفشل الكلوي الحاد, بروبونات الصوديوم, الإجهاد التأكسدي, التحلل المِيتَوُنْدِرِي, الإشعاع الغاما