Clear Sky Science · nl
Een robuust muislever-organoïdeplatform maakt blijvende multicellulaire rijping en fibrosemodellering mogelijk vanaf een enkel weefselmonster
Waarom het kweken van mini-levers ertoe doet
Chronische leverziekte neemt wereldwijd toe, terwijl behandelopties beperkt blijven en donorgewervelde organen voor transplantatie schaars zijn. Wetenschappers wenden zich tot kleine driedimensionale “mini-organen”, of organoïden, die in het laboratorium worden gekweekt om leverziekten beter te begrijpen, nieuwe geneesmiddelen te testen en toekomstige regeneratieve therapieën te verkennen. Deze studie beschrijft een nieuw muislever-organoïde systeem dat, uit één klein stukje leverweefsel, betrouwbaar meerdere belangrijke leverceltypen samen kan laten groeien en zelfs het littekenvormingsproces dat fibrose heet kan nabootsen. 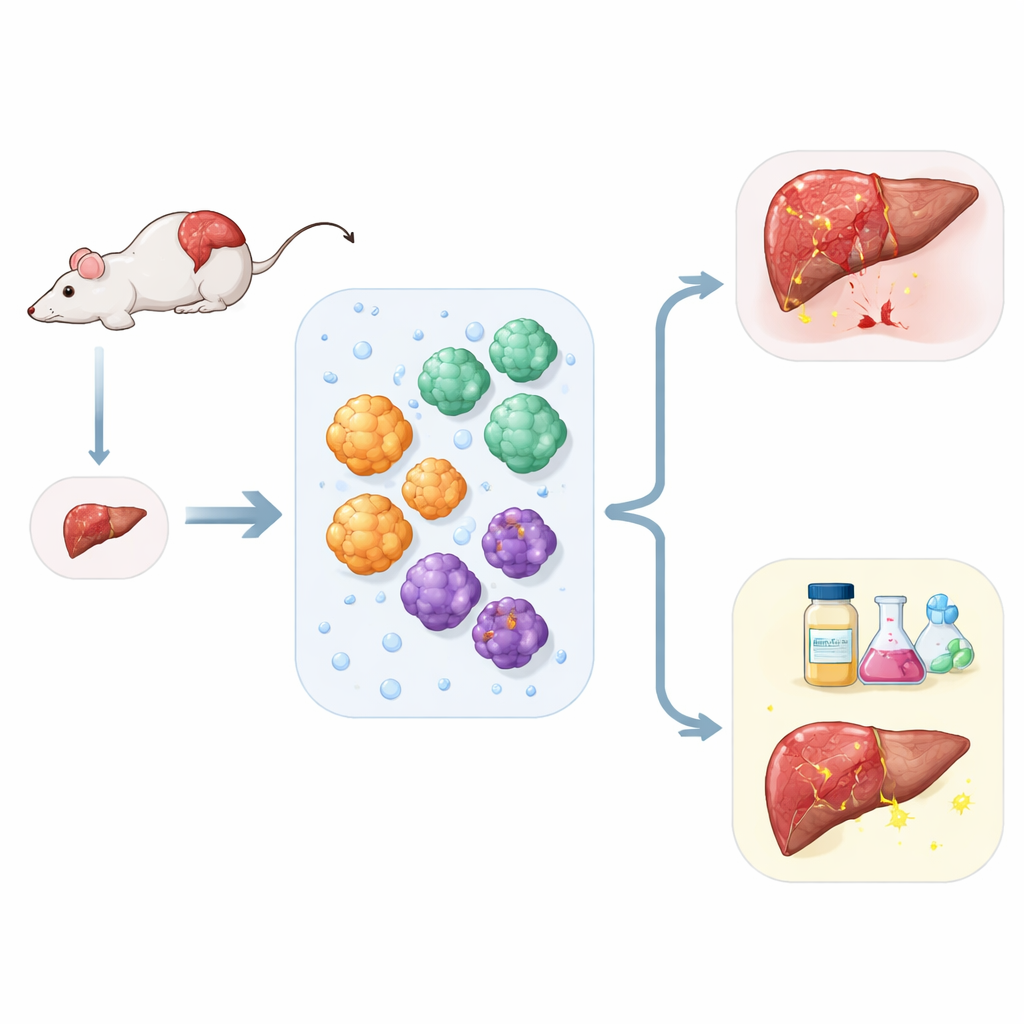
Kleine levers bouwen uit een klein monster
De onderzoekers wilden een praktisch probleem oplossen: hoe haal je de meeste informatie uit heel weinig leverweefsel. Met een vereenvoudigde preparatiemethode splitsten ze muislever in individuele cellen en scheidden die op basis van eenvoudige fysieke en oppervlakte-eigenschappen. Uit één weefselmonster konden ze drie belangrijke spelers van de lever isoleren: functionele levercellen die het metabolisme verzorgen, galgangcellen die spijsverteringsvloeistoffen verplaatsen, en ondersteunende cellen genaamd stercellen die de littekenvorming aansturen. Elk celtype werd gekweekt in een gelachtige matrix, waar het zichzelf organiseerde tot bolvormige organoïden die deden denken aan verkleinde stukjes leverweefsel.
Levercellen rijp en actief houden
Een langdurige uitdaging in leveronderzoek is dat levercellen snel hun gespecialiseerde functies verliezen zodra ze uit het lichaam worden gehaald. Om dit aan te pakken fijntunen de onderzoekers het chemische recept van het kweekmedium voor hepatocyt-organoïden. Door een remmer van het Notch-pad toe te voegen (wat cellen wegduwt van een stamcelachtige status) en het steroïde geneesmiddel dexamethason, stimuleerden ze de organoïden om functioneel “volwassen” te blijven. Over vele groeicycli bleven deze organoïden albumine produceren, suikers opslaan, vetten verwerken en enzymen voor medicijnafbraak uitvoeren op manieren die nauw overeenkomen met vers geïsoleerde levercellen. Belangrijk is dat de cellen niet terugzakten naar een minder volwassen of verkeerde identiteit, wat een veelvoorkomend probleem is in oudere organoïde systemen.
Galgang- en ondersteunende cellen vastleggen
Uit dezelfde leverfragmenten ontstonden ook robuuste galgangorganoïden. Deze structuren vormden holle bollen bekleed met een enkele cellaag die leek op kleine buisjes. Ze vertoonden stabiele expressie van markers die typisch zijn voor galkanaalweefsel en toonden een actief transportpompsysteem dat verbindingen naar de centrale holte kan verplaatsen, een belangrijke eigenschap voor de verwerking van gal en geneesmiddelen. Tegelijkertijd zuiverde het team stercellen tot zeer hoge zuiverheid door gebruik te maken van hun natuurlijke opslag van vitamine A–rijke druppels. In hun rusttoestand slaakten deze stercellen rustig lipiden op, maar wanneer ze werden blootgesteld aan een signaalmolecuul dat met beschadiging wordt geassocieerd, transformeerden ze in een actievere, vezelproducerende vorm, wat overeenkomt met wat er gebeurt tijdens littekenvorming in echte leveren.
Leverlittekens modelleren in een schaaltje
Om te onderzoeken of deze componenten vroege leverschade konden nabootsen, brachten de wetenschappers de organoïden en stercellen samen in een gedeelde cultuur. Toen stercellen in hun geactiveerde, littekenvormende staat werden gezet, gaven ze oplosbare factoren af die de nabijgelegen hepatocyt- en galgangorganoïden bereikten. De ooit gezonde organoïden vertraagden hun groei, verloren enkele van hun kenmerkende leverfuncties en begonnen tekenen te vertonen van een cellulaire identiteitsverandering die wordt gekoppeld aan weefselverharding en functieverlies. Deze veranderingen weerspiegelen hoe littekenvorming bij chronische leverziekte geleidelijk het vermogen van het orgaan om te regenereren en het lichaam te ontgiften ondermijnt. 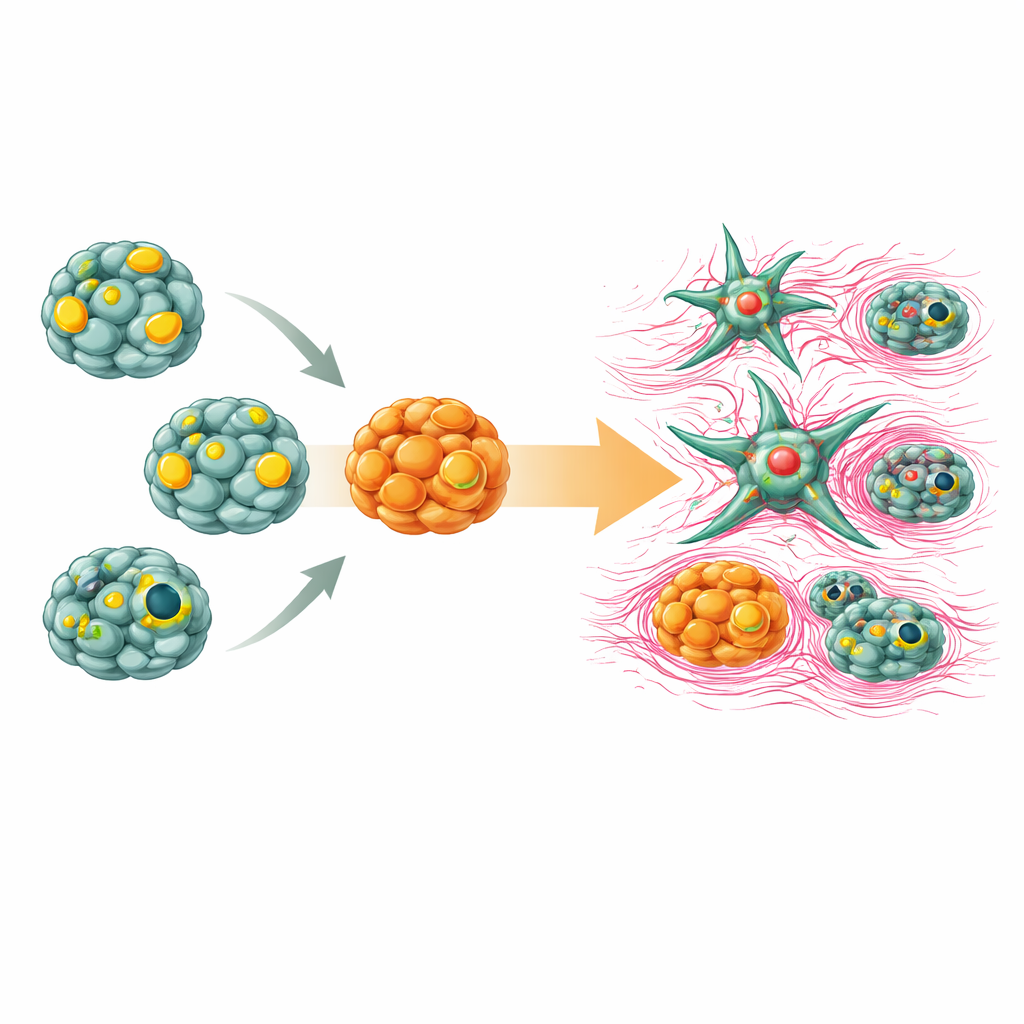
Wat dit betekent voor toekomstige leverzorg
Door een stabiel, multicellulair mini-leversysteem op te bouwen uit slechts één klein weefselstuk, biedt deze studie een krachtig nieuw hulpmiddel voor leveronderzoek. Het platform behoudt trouw het gedrag van meerdere leverceltypen en kan sleutelfasen van fibrose reproduceren, alles in een gecontroleerd schaaltje. Voor niet-specialisten is de kernboodschap dat wetenschappers nu leverschade, herstel en medicijnreacties op een veel realistischer maar schaalbaarere manier kunnen bestuderen, zonder uitsluitend te vertrouwen op diermodellen of schaars menselijk weefsel. Op de lange termijn zouden dergelijke systemen het ontdekken van anti-fibrotische geneesmiddelen kunnen versnellen en helpen behandelingen te personaliseren, waardoor we dichterbij therapieën komen die chronische leverschade stoppen of zelfs omkeren.
Bronvermelding: Liang, Y., Ye, Y., Xie, H. et al. A robust mouse liver organoid platform enables sustained multicellular maturation and fibrosis modeling from a single tissue sample. Sci Rep 16, 14137 (2026). https://doi.org/10.1038/s41598-026-42990-2
Trefwoorden: leverorganoïden, fibrosemodellering, hepatische stercellen, regeneratieve geneeskunde, medicijnscreening