Clear Sky Science · he
פלטפורמת אורגנואידים לכבד עכבר עמידה מאפשרת הבשלה רב-תאית ממושכת ודימוי צלקתיות מדגימה מדגם רקמה יחיד
מדוע גידול ״כבדונים״ זעירים חשוב
מחלות כבד כרוניות נמצאות בעלייה ברחבי העולם, אך אפשרויות הטיפול מוגבלות ושתלים מתורמים נדירים. מדענים פונים לכ־״איברים זעירים״ תלת־ממדיים, או אורגנואידים, שגודלו במעבדה על מנת להבין טוב יותר מחלות כבד, לבדוק תרופות חדשות ולחקור טיפולים רגנרטיביים עתידיים. המחקר המתואר כאן מציג מערכת חדשה של אורגנואידים לכבד עכבר, שמאפשרת מתוך חתיכת רקמה קטנה לגדל באמינות מספר סוגי תאים מרכזיים בכבד ואף לחקות את תהליך הצלקתיות המכונה פיברוזיס.
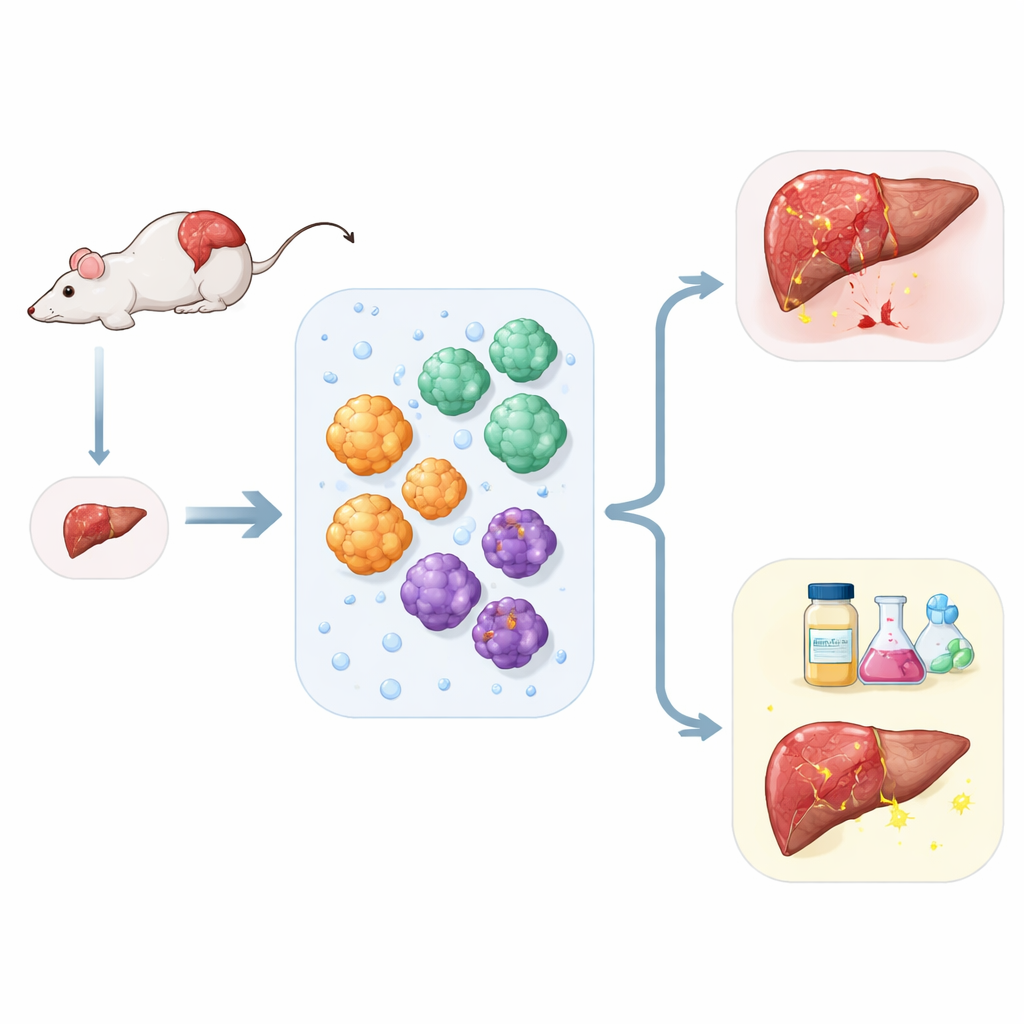
בניית כבדונים זעירים מדגימה קטנה
החוקרים שאפו לפתור בעיה פרקטית: כיצד להפיק את מירב המידע ממעטה רקמת כבד. באמצעות שיטת הכנה פשוטה ומדויקת הם פירקו את כבד העכבר לתאים בודדים ואז הפרידו אותם לפי מאפיינים פיזיים ומשטחיים פשוטים. מתוך דגימה אחת יכלו לבודד שלוש שחקניות מרכזיות בכבד: תאי הכבד העובדים המטפלים בחילוף החומרים, תאי צינור המרה שמנהלים את הנוזלים העיכוליים ותאי תמיכה הקרויים תאי סטלייט שמניעים את הצלקתיות. כל סוג תא גדל בסקרופ כמו ג'ל, שבו הוא התארגן בעצמו לאורגנואידים כדוריים הדומים לחתיכות כבד ממוקטנות.
שמירה על בגרות ותפקוד של תאי כבד
אתגר ותיק במחקר כבד הוא שתאי כבד מאבדים במהירות את היכולות המיוחדות שלהם לאחר הוצאתם מן הגוף. כדי להתמודד עם זאת הקבוצה לכיוון את המתכון הכימי של מדיום הגידול לאורגנואידי ההפטוציטים. על־ידי הוספת מעכב מסלול Notch (המכוון תאים להתרחק ממצב דמוי־גזע) והסטרואיד דקסמתאזון, עודדו את האורגנואידים להישאר באופן פונקציונלי ״בוגרים״. במשך מחזורים מרובים של גידול, האורגנואידים המשיכו לייצר אלבומין, לאגור סוכרים, לעבד שומנים ולהפעיל אנזימי פירוק־תרופות באופן שתאם במידה רבה תאים שנחקרו זהרם. באופן חשוב, התאים לא חזרו למצב פחות בוגר או לזהות שגויה — בעיה שכיחה במערכות אורגנואידים ישנות יותר.
שימור תאי צינור המרה ותאי תמיכה
אותם רסיסי כבד גם הניבו אורגנואידים יציבים של צינור המרה. מבנים אלה התארגנו לכדורים חלולים שמרופדים בשכבה יחידה של תאים שהזכירו צינורות זעירים. הם הראו ביטוי יציב של סימני רקמה טיפוסיים לצינור המרה וגילו משאבת טרנספורט פעילה שיכולה להעביר תרכובות למרכז החלל — תכונה מרכזית לטיפול במרה ובתרופות. במקביל, הצוות טיהר תאי סטלייט להיקף טהרה מאוד גבוה באמצעות ניצול מאגרי הטיפות העשירות בוויטמין A הטבעיות שלהם. במצבם הרדום, תאי הסטלייט הללו אחסנו שומנים בשקט, אך כאשר נחשפו למולקולה מסנג'ר הקשורה לפגיעה, הם השתנו לצורה אקטיבית יותר המייצרת סיבים, המשקפת את מה שקורה במהלך הצלקת בכבד אמיתי.
דימוי צלקתיות כבד על צלחת
כדי לבדוק האם הרכיבים הללו יכולים לשחזר נזק ראשוני לכבד, המדענים הביאו את האורגנואידים ותאי הסטלייט יחד לתרבית משותפת. כאשר תאי הסטלייט עברו להפוך למצבם המופעל המייצר צלקת, הם שחררו גורמים מסיסים שהשפיעו על אורגנואידי ההפטוציטים וצינור המרה הסמוכים. האורגנואידים שפעם היו בריאים האטו את קצב הגידול שלהם, איבדו חלק מתכונות הכבד האופייניות והחלו להראות סימני שינוי זהות תאי הקשורים להקשחת הרקמה ולאובדן תפקוד. השינויים האלה משקפים את האופן שבו הצלקת במחלות כבד כרוניות מחלישה בהדרגה את יכולת האיבר להתחדש ולפנות רעלים מהגוף.
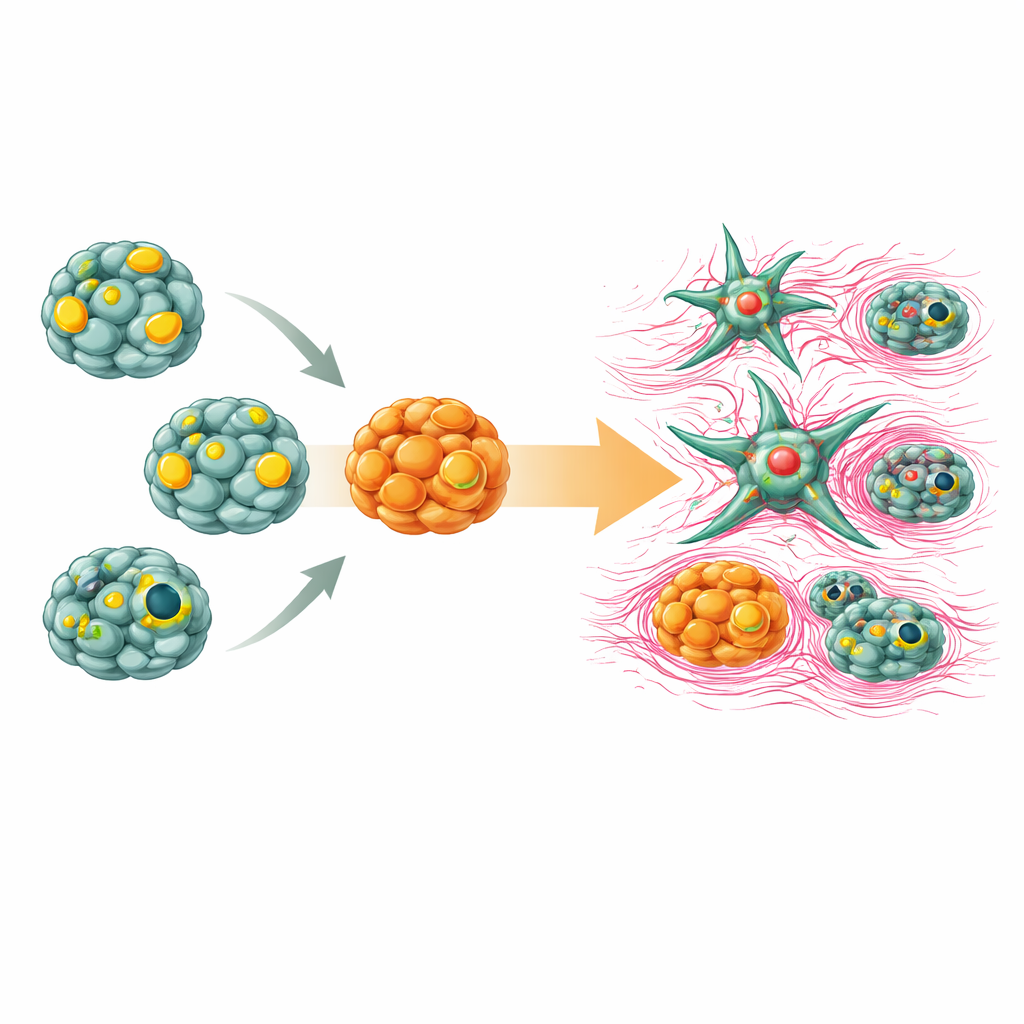
מה משמעות הדבר עבור טיפול עתידי בכבד
על־ידי בניית מערכת כבד זעירה רב־תאית יציבה מחתיכת רקמה קטנה בלבד, המחקר מציע כלי חדש וחזק למחקר כבד. הפלטפורמה שומרת בנאמנות על ההתנהגות של מספר סוגי תאים בכבד ויכולה לשחזר צעדים מרכזיים של פיברוזיס — הכל בתנאי תרבית מבוקרים. לקורא שאינו מומחה, המסקנה היא שמדענים יכולים כעת לחקור פגיעה בכבד, התאוששות ותגובות לתרופות בצורה ריאליסטית הרבה יותר אך בסקאלה ניתנת להרחבה, מבלי להסתמך רק על דגמי חיה או על איברים אנושיים נדירים. בטווח הארוך, מערכות כאלה יכולות לזרז גילוי תרופות אנטי־פיברוטיות ולעזור להתאמת טיפולים אישית, מה שיכול לקרב אותנו אל טיפולים המעכבים או אפילו הופכים נזק כבד כרוני.
ציטוט: Liang, Y., Ye, Y., Xie, H. et al. A robust mouse liver organoid platform enables sustained multicellular maturation and fibrosis modeling from a single tissue sample. Sci Rep 16, 14137 (2026). https://doi.org/10.1038/s41598-026-42990-2
מילות מפתח: אורגנואידים של הכבד, דימוי צלקתיות (פיברוזיס), תאי סטלייט כבדיים, רפואה רגנרטיבית, סינון תרופות