Clear Sky Science · it
Una solida piattaforma di organoidi epatici di topo permette una maturazione multicellulare sostenuta e la modellazione della fibrosi a partire da un singolo campione di tessuto
Perché coltivare mini-fegati è importante
Le malattie croniche del fegato sono in aumento a livello globale, ma le opzioni terapeutiche restano limitate e gli organi donatori per il trapianto scarseggiano. I ricercatori si rivolgono a piccoli “mini-organi” tridimensionali, o organoidi, coltivati in laboratorio per comprendere meglio le patologie epatiche, testare nuovi farmaci ed esplorare future terapie rigenerative. Questo studio descrive un nuovo sistema di organoidi epatici di topo che, a partire da un singolo piccolo frammento di fegato, è in grado di far crescere in modo affidabile diversi tipi cellulari chiave e persino di mimare il processo di cicatrizzazione noto come fibrosi. 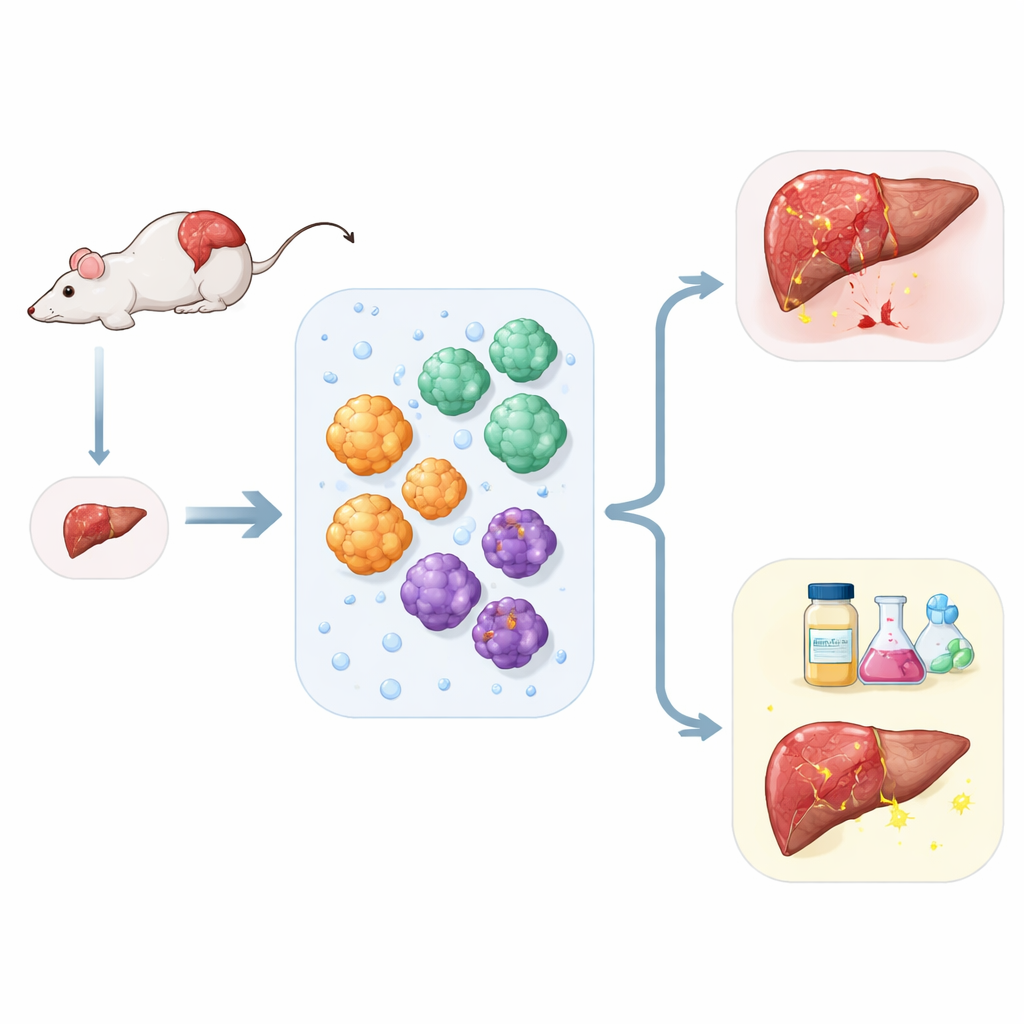
Costruire mini-fegati da un piccolo campione
Gli autori hanno affrontato un problema pratico: come ottenere il massimo delle informazioni da una quantità minima di tessuto epatico. Utilizzando un metodo di preparazione snello, hanno digerito il fegato di topo in cellule singole e poi le hanno separate in base a semplici proprietà fisiche e di superficie. Da un campione di tessuto è stato possibile isolare tre attori principali del fegato: gli epatociti, che gestiscono il metabolismo; le cellule dei dotti biliari, che convogliano i fluidi digestivi; e le cellule di supporto chiamate stellate, responsabili della cicatrizzazione. Ogni tipo cellulare è stato coltivato in un impalcatura simile a un gel, dove si è auto-organizzato in organoidi sferici somiglianti a porzioni miniaturizzate di tessuto epatico.
Mantenere gli epatociti maturi e attivi
Una sfida di lunga data nella ricerca sul fegato è che gli epatociti perdono rapidamente le loro capacità specializzate una volta isolati dall’organismo. Per affrontare questo problema, il gruppo ha messo a punto la ricetta chimica del mezzo di coltura per gli organoidi di epatociti. Aggiungendo un inibitore della via Notch (che spinge le cellule lontano da uno stato simile a quello staminale) e il farmaco steroideo desametasone, hanno incoraggiato gli organoidi a mantenersi funzionalmente “adulti”. Dopo numerosi cicli di crescita, questi organoidi hanno continuato a produrre albumina, immagazzinare zuccheri, metabolizzare i grassi e attivare enzimi deputati alla degradazione dei farmaci in modi molto simili a quelli degli epatociti appena isolati. È importante notare che le cellule non sono tornate verso uno stato meno maturo o verso identità sbagliate, un problema frequente nei sistemi di organoidi più vecchi.
Catturare i dotti biliari e le cellule di supporto
Gli stessi frammenti di fegato hanno anche fornito organoidi dei dotti biliari robusti. Queste strutture hanno formato sfere cave rivestite da un singolo strato cellulare che ricordava piccoli tubi. Hanno mostrato l’espressione stabile di marcatori tipici del tessuto dei dotti biliari e hanno dimostrato un trasporto attivo in grado di spostare composti nella cavità centrale, caratteristica fondamentale per la gestione della bile e dei farmaci. Parallelamente, il gruppo ha purificato le cellule stellate con elevata purezza sfruttando le loro naturali riserve di gocce ricche di vitamina A. In stato di riposo, queste cellule stellate immagazzinavano lipidi in modo silenzioso, ma quando sono state esposte a una molecola segnale associata a lesione, si sono trasformate in una forma più attiva e produttrice di fibre, rispecchiando quanto avviene durante la cicatrizzazione nei fegati reali.
Modellare la cicatrizzazione epatica in provetta
Per verificare se questi componenti potevano ricreare il danno epatico iniziale, gli scienziati hanno messo insieme organoidi e cellule stellate in una coltura condivisa. Quando le cellule stellate sono state attivate nello stato produttivo di cicatrice, hanno rilasciato fattori solubili che hanno raggiunto i vicini organoidi di epatociti e dotti biliari. Gli organoidi, prima sani, hanno rallentato la crescita, perso alcune delle loro caratteristiche tipiche e cominciato a mostrare segni di uno spostamento dell’identità cellulare legato all’irrigidimento del tessuto e alla perdita di funzione. Questi cambiamenti rispecchiano il modo in cui la cicatrizzazione nelle malattie epatiche croniche compromette gradualmente la capacità dell’organo di rigenerarsi e di detossificare l’organismo. 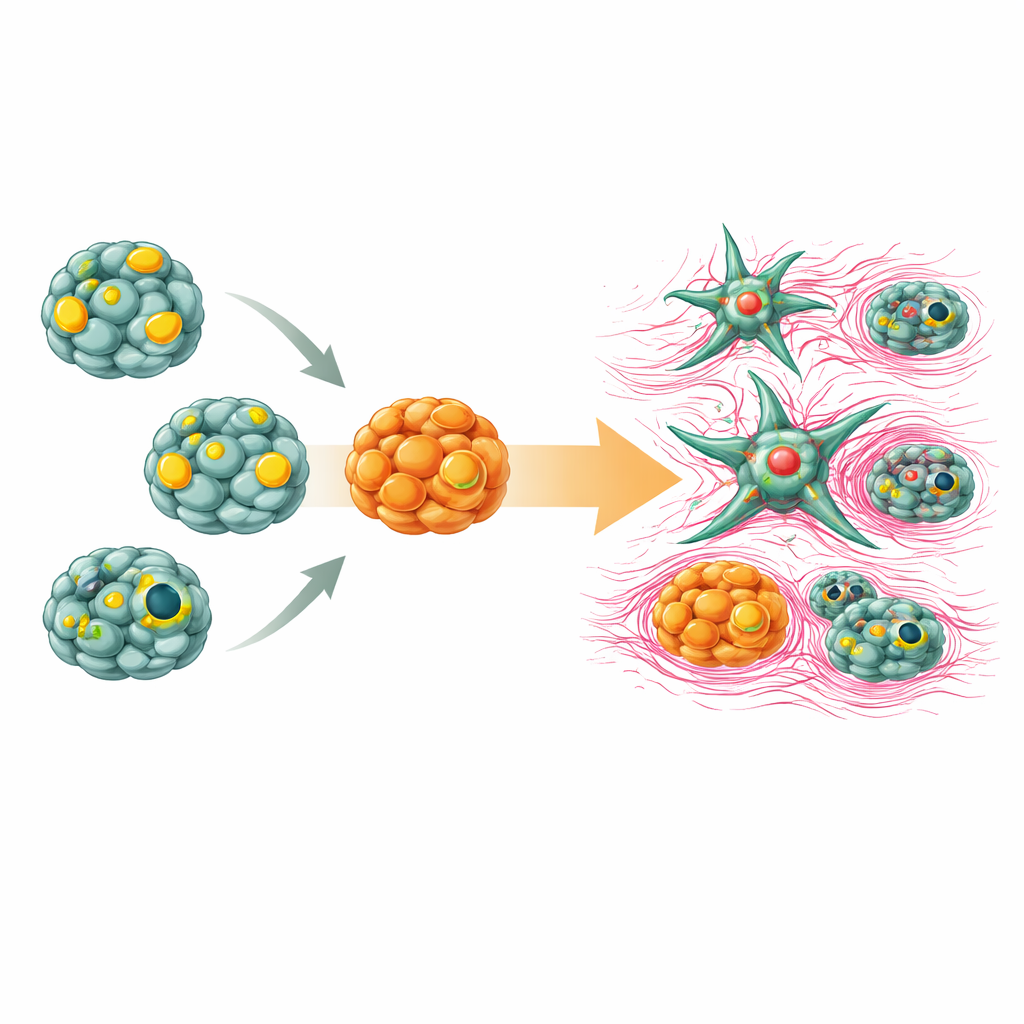
Cosa significa per la cura futura del fegato
Costruendo un sistema di mini-fegato stabile e multicellulare a partire da un unico piccolo frammento di tessuto, questo studio offre un nuovo strumento potente per la ricerca epatica. La piattaforma mantiene fedelmente il comportamento di diversi tipi cellulari epatici e può riprodurre i passaggi chiave della fibrosi, tutto in una piastra di coltura controllata. Per i non specialisti, il messaggio è che ora gli scienziati possono studiare danno epatico, recupero e risposte farmacologiche in modo molto più realistico e scalabile, senza dipendere esclusivamente da modelli animali o da organi umani scarsi. Sul lungo periodo, tali sistemi potrebbero accelerare la scoperta di farmaci anti-fibrotici e aiutare a personalizzare i trattamenti, avvicinandoci a terapie in grado di fermare o persino invertire il danno epatico cronico.
Citazione: Liang, Y., Ye, Y., Xie, H. et al. A robust mouse liver organoid platform enables sustained multicellular maturation and fibrosis modeling from a single tissue sample. Sci Rep 16, 14137 (2026). https://doi.org/10.1038/s41598-026-42990-2
Parole chiave: organoidi epatici, modellazione della fibrosi, cellule stellate epatiche, medicina rigenerativa, screening farmacologico