Clear Sky Science · nl
Een multitask deep learning- en radiomics-framework voor detectie en classificatie van foetale anatomische structuren in echografie
Waarom vroege hersenscans van de baby ertoe doen
Toekomstige ouders en clinici willen al vroeg duidelijke antwoorden over de gezondheid van een baby. Echografische onderzoeken in de eerste drie maanden van de zwangerschap bieden al een inkijk in de zich ontwikkelende hersenen en het gezicht, waar subtiele veranderingen kunnen wijzen op latere problemen. Maar het interpreteren van deze korrelige beelden is lastig en hangt sterk af van de vaardigheid van degene die de probe vasthoudt. Deze studie onderzoekt hoe moderne kunstmatige intelligentie kan fungeren als een extra paar deskundige ogen, automatisch kleine structuren in het hoofd van de foetus kan detecteren en classificeren om vroege, consistentere screening te ondersteunen.
Meer zien dan het menselijk oog
De onderzoekers concentreerden zich op negen belangrijke hersen- en gelaatskenmerken die artsen routinematig controleren tussen 11 en 14 weken zwangerschap, waaronder delen van de hersenen, de vloeistofruimtes eromheen en gelaatsmarkeurs zoals het neusbottinkje en het gehemelte. Veranderingen in deze kenmerken kunnen wijzen op genetische of structurele aandoeningen. Traditioneel kunnen zelfs ervaren specialisten van mening verschillen over wat zij op echografie zien, en de beeldkwaliteit varieert per kliniek. Om dit aan te pakken verzamelde het team een grote, diverse set van 4.532 echo-onderzoeken uit negen medische centra, waarmee een breed scala aan apparatuur, beeldstijlen en foetale posities werd vastgelegd. Deze diversiteit stelde hen in staat een geautomatiseerd systeem te bouwen en te testen dat minder gebonden is aan één ziekenhuis of apparaat.
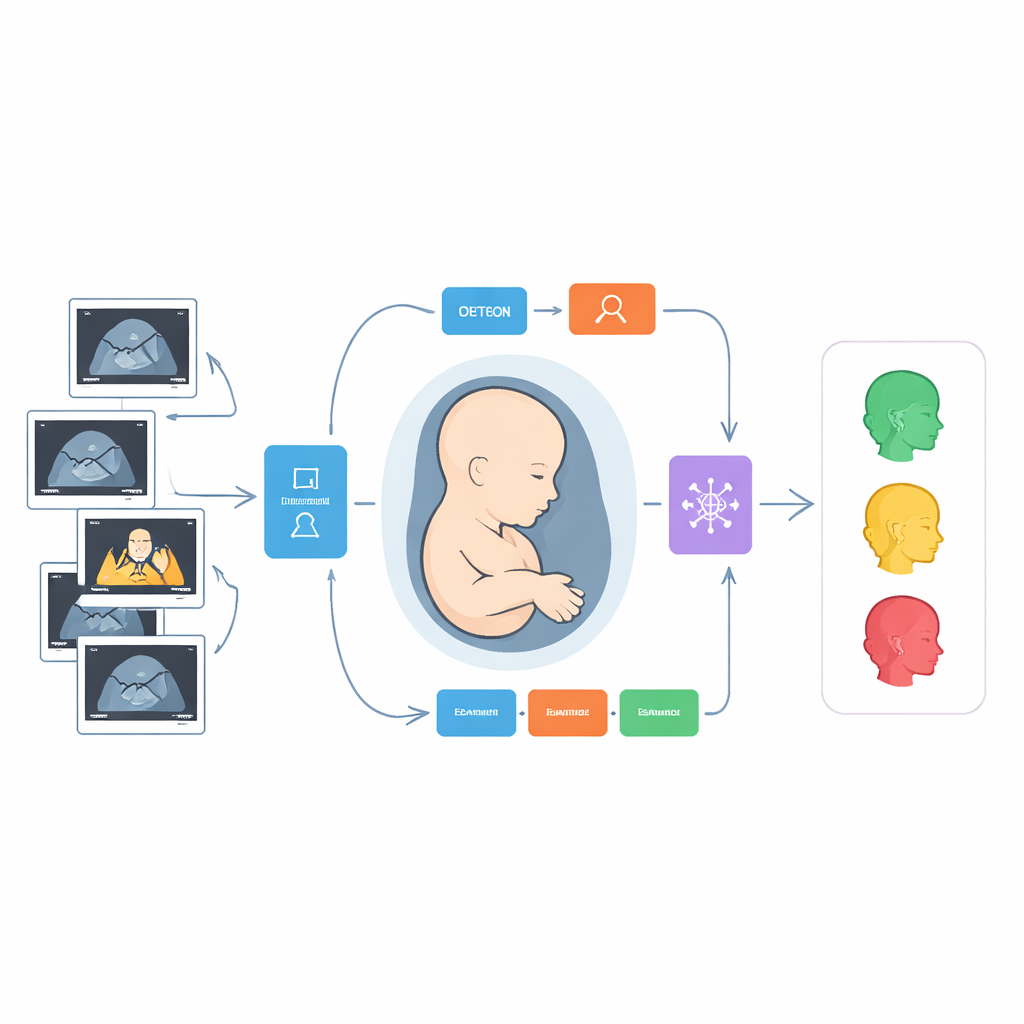
Hoe de slimme pijplijn werkt
De kern van de studie is een stapsgewijze digitale pijplijn die het werkproces van een menselijke onderzoeker nabootst en vervolgens uitbreidt. Eerst scannen twee geavanceerde beeldanalysemethoden elk echoframe en trekken ze boxen om de negen doelstructuren, zoals het middenbrein of het neusbottinkje. Het ene model is een snelle detector die ontworpen is om snel kleine objecten te vinden, terwijl het andere een transformer-achtige architectuur gebruikt die het beeld in overlappende vensters bekijkt om zowel lokale details als bredere context vast te leggen. Zodra de regio’s zijn gelokaliseerd, bestudeert het systeem de inhoud van elke box op twee aanvullende manieren: het berekent honderden handgemaakte “radiomische” metingen die textuur, helderheid en vorm beschrijven, en het laat een diep neuraal netwerk direct uit de pixels eigen patronen leren.
Ruwe kenmerken omzetten in duidelijke beslissingen
Het verzamelen van duizenden numerieke metingen is alleen zinvol als ze betrouwbaar en niet redundant zijn. De auteurs pasten daarom een driestaps filter toe. Ze hielden eerst alleen die kenmerken over die stabiel bleken over verschillende centra en beoordelaars, verwijderden vervolgens sterk overlappende metingen en gebruikten tenslotte een sparsity-bevorderende methode om de meest informatieve subset te kiezen. Deze verfijnde kenmerken, afkomstig uit zowel radiomics als deep learning, werden daarna ingevoerd in een gespecialiseerd model dat ontworpen is voor het verwerken van tabelachtige data. Dit model leert hoe verschillende kenmerken samenhangen, waardoor het elke structuur kan indelen in klinisch betekenisvolle categorieën, zoals normaal, twijfelachtig of duidelijk afwijkend, op basis van hoe deze in de scan verschijnt.
Hoe goed het systeem presteerde
Om te testen of de aanpak ook buiten de trainingsdata standhield, evalueerde het team de prestaties op interne testbeelden en op een aparte set van bijna 500 scans uit een ander centrum. De transformer-gebaseerde detector bleek bijzonder nauwkeurig in het vinden van de juiste anatomische regio’s en kwam vaak met zeer grote overlap overeen met door experts gelabelde boxen. Bij het beoordelen of een structuur normaal was of niet, versloegen de gecombineerde feature-modellen — die zowel radiomische als deep-learned patronen gebruikten — consequent modellen die op één bron vertrouwden. Op de moeilijkste externe testset classificeerden de beste gecombineerde modellen structuren in ongeveer 96% van de gevallen correct, met sterke capaciteit om subtiele afwijkingen te detecteren zoals een verkort neusbottinkje of vernauwde vloeistofruimtes achter de hersenstam.
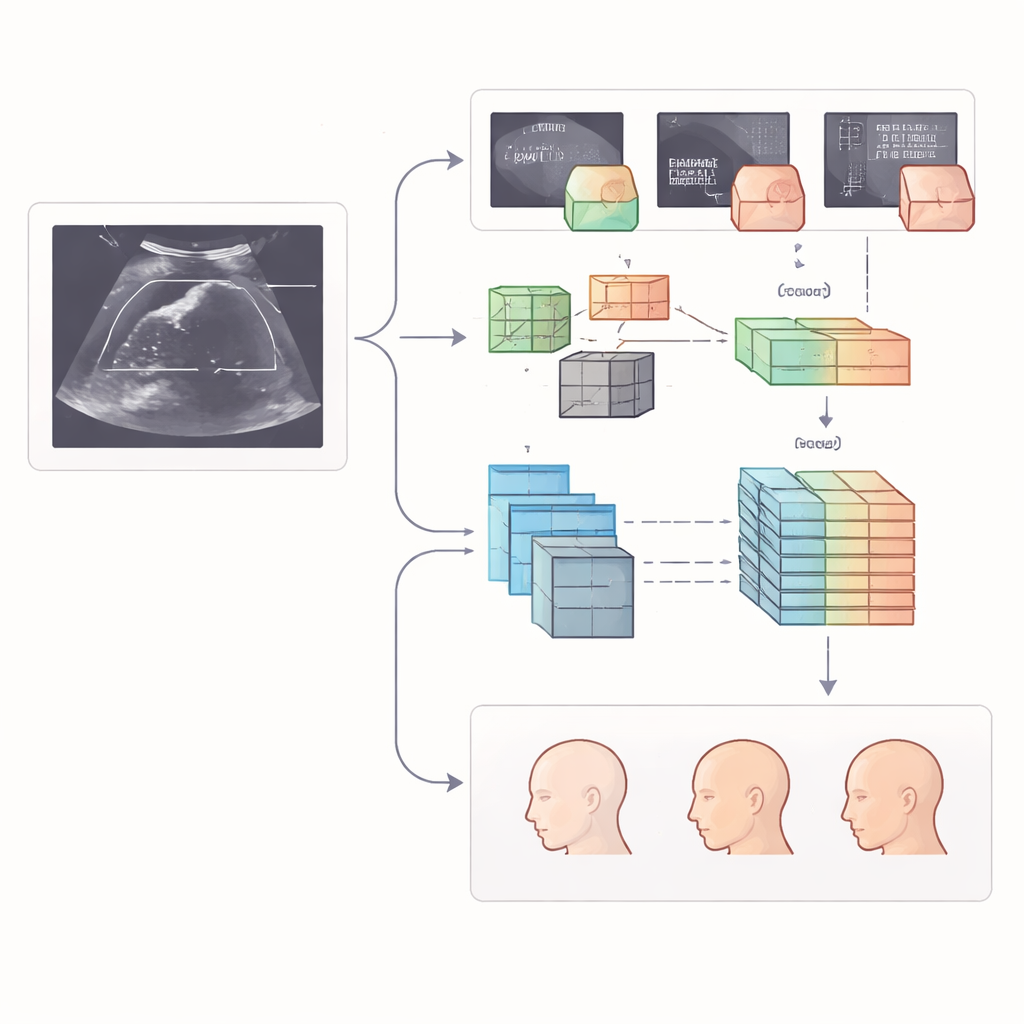
Wat dit kan betekenen voor prenatale zorg
Voor leken komt de boodschap erop neer dat computers nu kunnen helpen om vroege zwangerschapsmetingen consistenter te maken en minder afhankelijk van het oordeel van één enkel expert. Door automatisch delicate structuren in de foetale hersenen en het gezicht te vinden en te beoordelen, zou dit stapsgewijze systeem vroege, objectievere detectie van mogelijke problemen kunnen ondersteunen, zelfs in drukke klinieken met verschillende apparatuur. Hoewel de auteurs opmerken dat zeldzame en ongewone aandoeningen nog steeds een uitdaging vormen en dat verdere tests in de praktijk nodig zijn, suggereren hun resultaten dat zorgvuldig ontworpen AI-hulpmiddelen, getraind op meerdere centra, op een dag routinematige partners in eerstetrimester screening kunnen worden en ouders duidelijkere informatie en clinici sterkere besluitvormingsondersteuning kunnen bieden in een kritisch vroeg stadium.
Bronvermelding: Zhou, X., Wan, J., Sun, F. et al. A multi-task deep learning and radiomics framework for fetal anatomical structure detection and classification in ultrasound imaging. Sci Rep 16, 11586 (2026). https://doi.org/10.1038/s41598-026-41635-8
Trefwoorden: foetale echografie, prenatale screening, deep learning, radiomics, hersenen en gezichtsontwikkeling