Clear Sky Science · nl
Een computationele analyse van biofysische en geometrische beperkingen weerlegt bestaande hypothesen over kruis-excitatie in dorsale rootganglia
Waarom naburige zenuwcellen ertoe doen
Elke aanraking, pijn of temperatuurverandering die je voelt begint in kleine clusters zenuwcellen die dorsale rootganglia worden genoemd, net buiten het ruggenmerg. Al decennia zien wetenschappers daar een merkwaardig verschijnsel: wanneer één van deze cellen vuurt, worden zijn buren vaak gemakkelijker te prikkelen, alsof het signaal zijwaarts doorloopt. Deze "kruis-excitatie" zou onze kijk op pijn en sensatie kunnen veranderen. De nieuwe studie gebruikt gedetailleerde computermodellen om een eenvoudige maar ongemakkelijke vraag te stellen: werken onze huidige verklaringen voor dit zijwaartse gekeuvel daadwerkelijk?
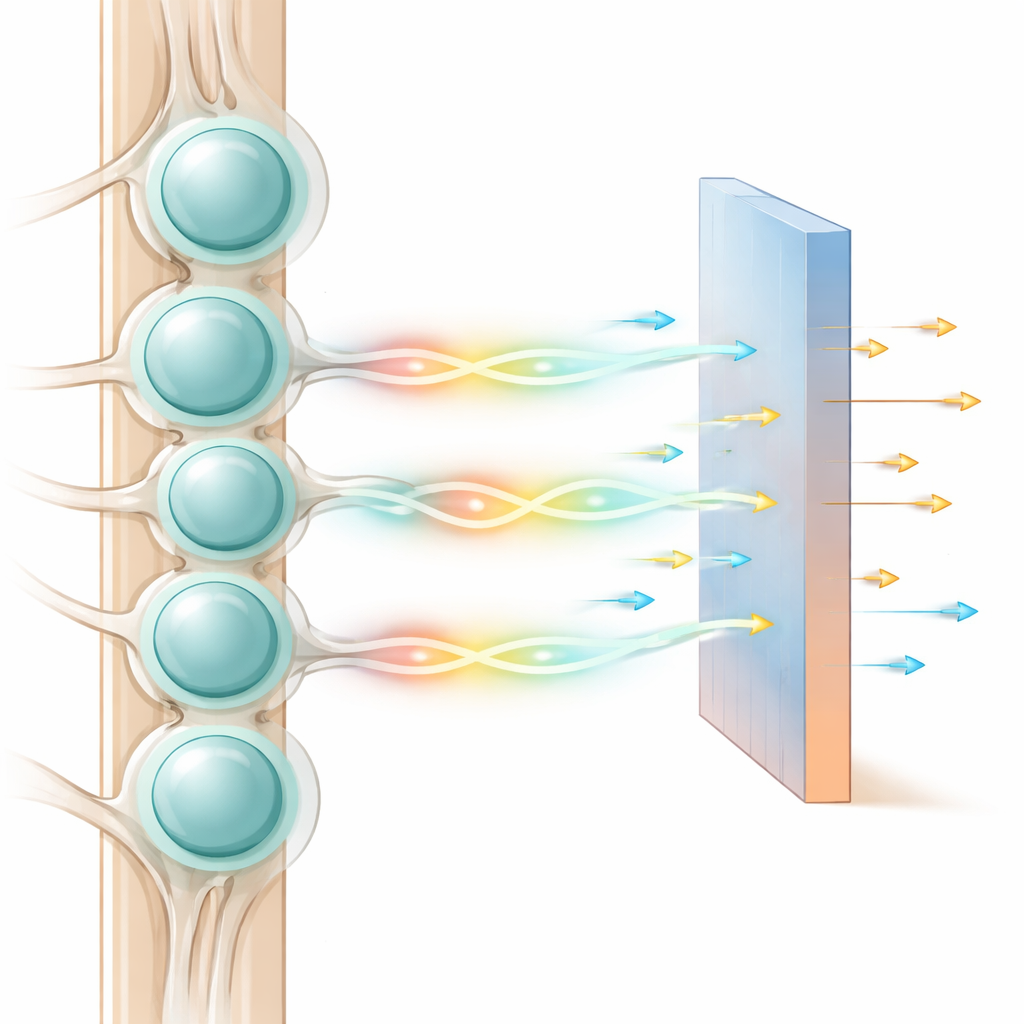
Een druk buurtnetwerk van zenuwcellen
Dorsale rootganglia zijn dicht opeengepakte buurten van sensorische neuronen. Het cellichaam van elke neuron is omhuld door een dun laagje ondersteunende cellen, satellietglia genoemd, die een kapsel vormen en de ene neuron grotendeels van de andere isoleren. Klassieke leerboeken beschrijven deze neuronen als eenvoudige relais die signalen alleen doorgeven aan het ruggenmerg als de input sterk genoeg is. Toch laten experimenten zien dat wanneer één neuron wordt gestimuleerd, veel buren binnen ongeveer een halve tot een seconde prikkelbaarder worden. Deze langzame, vertraagde versterking wijst op een chemisch of diffusie-gebaseerd proces in plaats van een snel elektrisch mechanisme, en het verschijnt in de meeste grote, aanraking-gerelateerde vezels, wat wijst op een fundamentele rol in sensoriële verwerking.
De hypothese van lekkende ionen testen
Een leidende verklaring is dat wanneer een neuron herhaaldelijk vuurt, het kaliumionen vrijgeeft in de smalle vloeistofruimte tussen zijn membraan en de omringende glia-schede. Als genoeg kalium zich ophoopt en door het omliggende weefsel sijpelt, zou dat nabijgelegen neuronen dichter bij activering kunnen duwen. De auteurs bouwden een zeer gedetailleerd model van een sensorische neuron en zijn glia-kapsel na, inclusief tientallen ionkanalen en pompen, en simuleerden toen kaliumwaarden die stegen van normaal naar niveaus gemeten in experimenten. Terwijl een eenvoudige tekstboekformule suggereerde dat de membraanpotentiaal met enkele millivolts zou kunnen verschuiven—dicht bij wat experimenten rapporteren—vertelde het volledige biofysische model een ander verhaal. Zodra realistische ionregulatie door zowel neuron als glia werd meegenomen, was de spanningsverschuiving minder dan één millivolt, veel te klein om de waargenomen kruis-excitatie te verklaren.
Het spoor volgen door kleine tussenruimtes
Het team vroeg zich vervolgens af of kalium eenvoudigweg van een vurende neuron naar zijn buren kon diffunderen door het doolhofachtige bindweefsel tussen kapsels. Ze verbonden twee gemodelleerde neuron–glia-eenheden met een gesimuleerde extracellulaire corridor en dreven één neuron aan met snelle elektrische pulsen, ter imitatie van eerdere experimenten. De spanningsverandering in de stille buur was verwaarloosbaar klein—orde van tien-miljoensten van een millivolt. Zelfs wanneer ze neuronen onrealistisch dicht bij elkaar plaatsten of de beschikbare ruimte reduceerden tot een nauwe labyrinthachtige structuur, produceerde diffusie alleen merkbare effecten wanneer twee cellichamen bijna een gemeenschappelijke omhulling deelden, een zeldzaam verschijnsel onder gezonde omstandigheden. Vanuit fysisch oogpunt kon diffusie gewoon geen sterk genoeg signaal over de typische afstanden dragen.
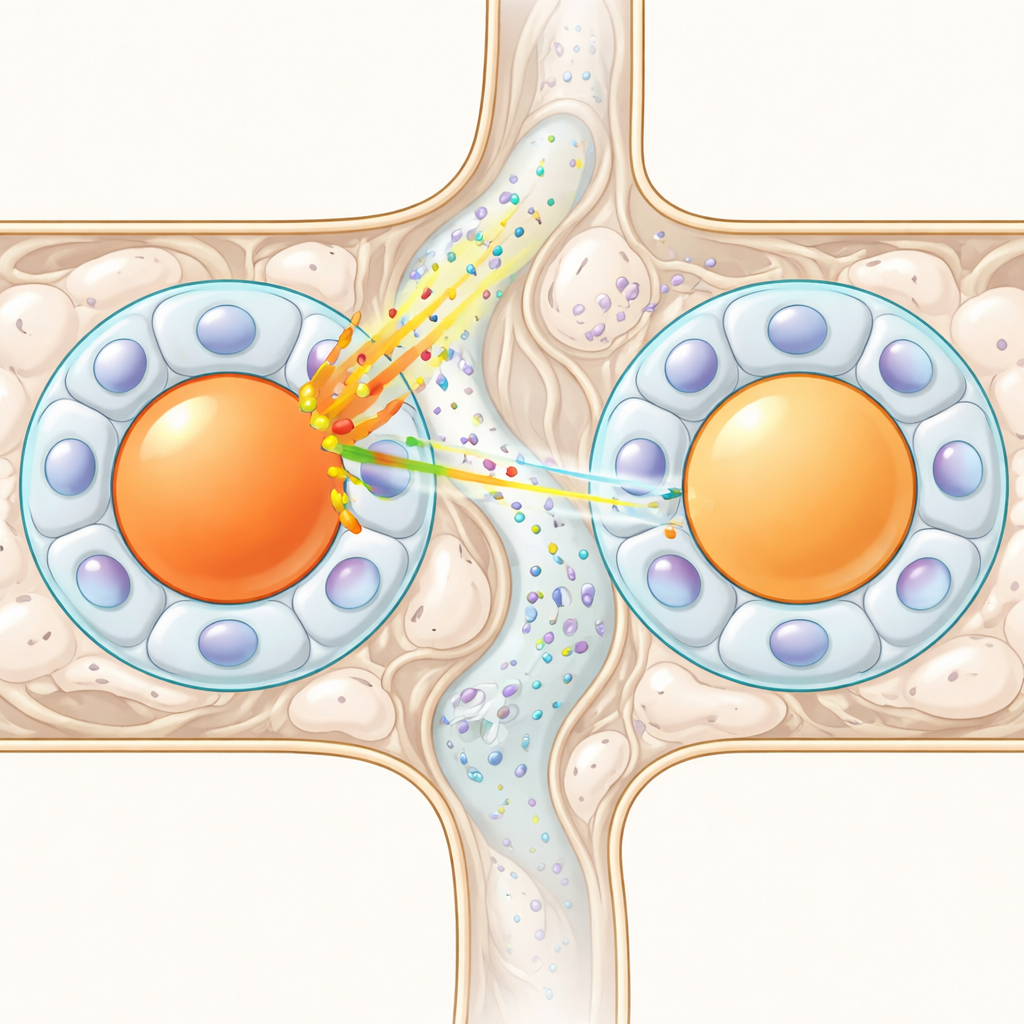
Wanneer structuur verbinding onwaarschijnlijk maakt
Een andere reeks hypothesen vertrouwt op fysieke bruggen tussen cellen. Sommige satellietglia vormen directe verbindingen, zogenaamde gap junctions, of speciale "sandwich"-arrangementen waarbij één glia-cel tussen twee neuronlichamen zit en chemische signalen kan doorgeven. Als zulke verbindingen veel voorkwamen, zouden ze een netwerk kunnen vormen dat excitatie verspreidt. Om dit te testen bouwden de onderzoekers een 3D-statistisch model van hoe neuron–glia-modules van verschillende grootte in een ganglion verpakt kunnen worden, en legden daar bekende waarschijnlijkheden voor deze verbindingen overheen. Experimenten suggereren dat gap junctions tussen aparte kapsels zeldzaam zijn—typisch een paar procent—en sandwich-achtige arrangementen komen voor in slechts ongeveer één op de tien neuronen. De simulaties toonden aan dat, gegeven deze lage kansen en het beperkte aantal fysieke buren (gewoonlijk ongeveer zeven per neuron), je de zeer hoge frequenties van kruis-excitatie die in experimenten worden gezien niet kunt bereiken. Zelfs door alle bekende structurele mechanismen te combineren blijf je vertekend tekortschieten.
Wat dit betekent voor voelen en behandelen van pijn
Door zowel de natuurkunde als de anatomie tot hun ruimste grenzen op te rekken—ionlekken te maximaliseren, cellen zo dicht mogelijk te verpakken en uit te gaan van beste-gevallen configuraties—probeerden de auteurs bestaande theorieën elke kans te geven te werken. Toch konden diffusie van ionen, zeldzame gap junctions en sandwich-achtige contacten samen nog steeds niet de sterkte en prevalentie van kruis-excitatie reproduceren die in echt weefsel wordt waargenomen. Voor de niet-specialist is de conclusie helder: de zijwaartse "echo" van zenuwactiviteit in deze ganglia is reëel en veelvoorkomend, maar onze huidige verklaringen zijn onvolledig. Er ontbreekt iets belangrijks over hoe sensorische neuronen met elkaar communiceren voordat signalen het ruggenmerg bereiken. Het begrijpen van deze verborgen verwerkingslaag kan onze ideeën over normale sensatie hervormen en nieuwe wegen openen voor pijntherapieën, vooral nu artsen steeds vaker elektrische stimulatie nabij deze ganglia gebruiken om chronische pijn te behandelen en het herstel na een ruggenmergletsel te ondersteunen.
Bronvermelding: Perevozniuk, D., Gorskii, O., Musienko, P. et al. A computational analysis of biophysical and geometric constraints refutes existing hypotheses of cross-excitation in dorsal root ganglia. Sci Rep 16, 14306 (2026). https://doi.org/10.1038/s41598-026-40355-3
Trefwoorden: dorsale rootganglion, kruis-excitatie, sensorische neuronen, neuropathische pijn, computationele modellering