Clear Sky Science · es
Un análisis computacional de las limitaciones biofísicas y geométricas refuta las hipótesis existentes sobre la excitación cruzada en los ganglios de la raíz dorsal
Por qué importan las células nerviosas vecinas
Cada toque, dolor o cambio de temperatura que percibes inicia su viaje en pequeños racimos de células nerviosas llamados ganglios de la raíz dorsal, situados justo fuera de la médula espinal. Durante décadas, los científicos han observado un comportamiento curioso allí: cuando una de estas células dispara, sus vecinas a menudo se vuelven más fáciles de excitar, como si la señal se propagara lateralmente de forma silenciosa. Esta “excitación cruzada” podría cambiar nuestra manera de entender el dolor y la sensación. El nuevo estudio utiliza modelos computacionales detallados para plantear una pregunta simple pero incómoda: ¿funcionan realmente nuestras explicaciones actuales para este rumor lateral?
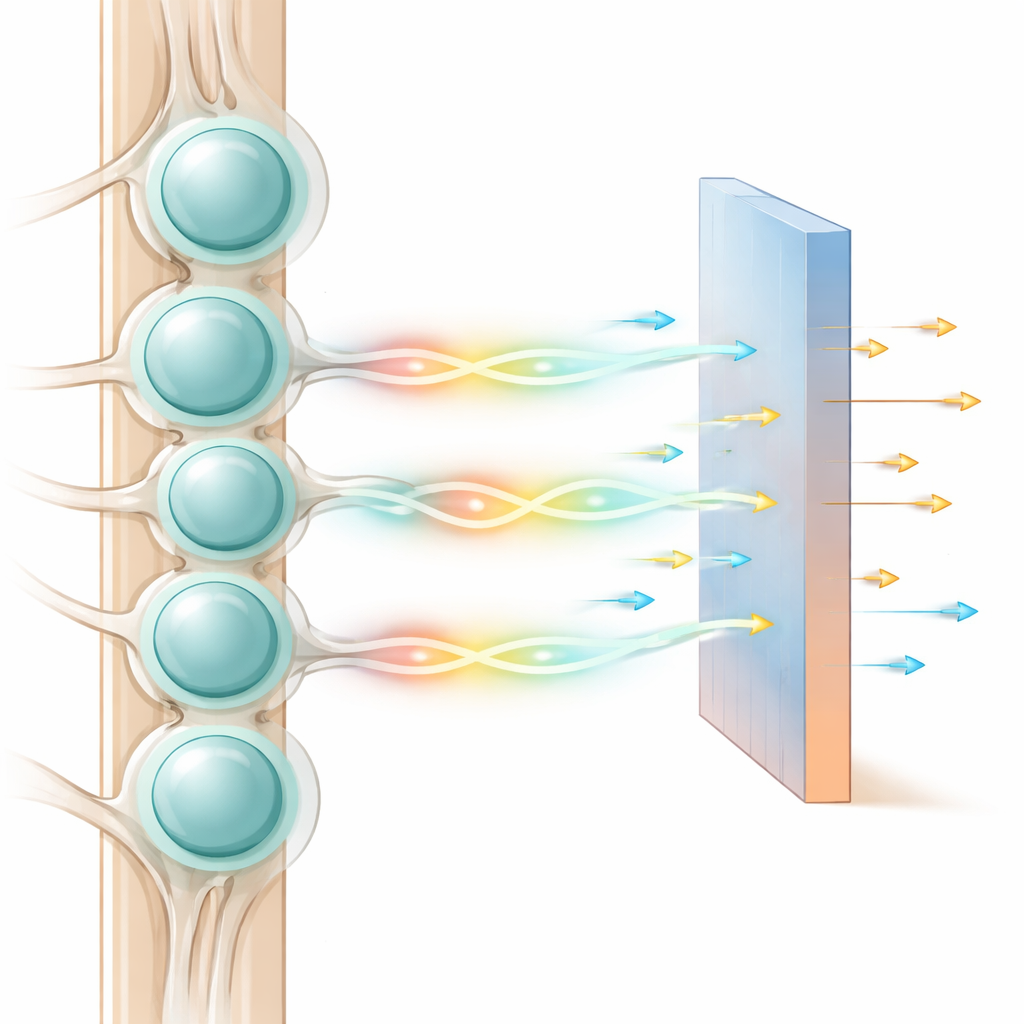
Un vecindario de células nerviosas muy concurrido
Los ganglios de la raíz dorsal son vecindarios densamente empaquetados de neuronas sensoriales. El soma de cada neurona está envuelto por una delgada capa de células de sostén llamadas células gliales satélite, formando una cápsula que aísla en gran medida una neurona de otra. Los manuales clásicos describen a estas neuronas como simples relés, que transmiten señales a la médula espinal solo cuando las entradas son lo bastante fuertes. Sin embargo, los experimentos han mostrado que cuando se estimula una neurona, muchas vecinas se vuelven más excitables en un lapso de alrededor de medio segundo a un segundo. Este aumento lento y demorado sugiere un proceso químico o basado en difusión más que uno eléctrico rápido, y aparece en la mayoría de las fibras grandes relacionadas con el tacto, lo que apunta a un papel fundamental en el procesamiento sensorial.
Probando la idea de fugas de iones
Una explicación principal es que cuando una neurona dispara repetidamente, libera iones de potasio al pequeño espacio de fluido entre su superficie y la cápsula glial circundante. Si suficiente potasio se acumula y se filtra a través del tejido circundante, podría empujar a las neuronas vecinas más cerca de disparar. Los autores reconstruyeron un modelo muy detallado de una neurona sensorial y su cápsula glial, incluyendo docenas de canales iónicos y bombas, y luego simularon niveles de potasio elevándose desde valores normales hasta los medidos en experimentos. Mientras que una fórmula sencilla de libro de texto sugería que el voltaje de la neurona podría desplazarse unos pocos milivoltios —cerca de lo que reportan los experimentos—, el modelo biofísico completo contó una historia diferente. Una vez incluida la regulación realista de iones por parte de la neurona y la glía, el cambio de voltaje fue menor de un milivoltio, mucho demasiado pequeño para explicar la excitación cruzada observada.
Siguiendo la pista a través de espacios diminutos
El equipo preguntó entonces si el potasio podría simplemente difundirse desde una neurona que dispara hacia sus vecinas a través del laberinto de tejido conectivo entre las cápsulas. Conectaron dos unidades modelo neurona–glía con un corredor extracelular simulado y estimularon una neurona con pulsos eléctricos rápidos, imitando experimentos previos. El cambio de voltaje en la vecina silenciosa fue insignificante —del orden de diez millonésimas de milivoltio. Incluso cuando empacaron neuronas de manera irrealmente cercana o redujeron el espacio disponible a un laberinto estrecho, la difusión solo produjo efectos notables cuando dos somas casi compartían una envoltura común, una ocurrencia rara en condiciones de salud. Desde un punto de vista físico, la difusión simplemente no podía transportar una señal lo bastante fuerte a través de las distancias típicas.
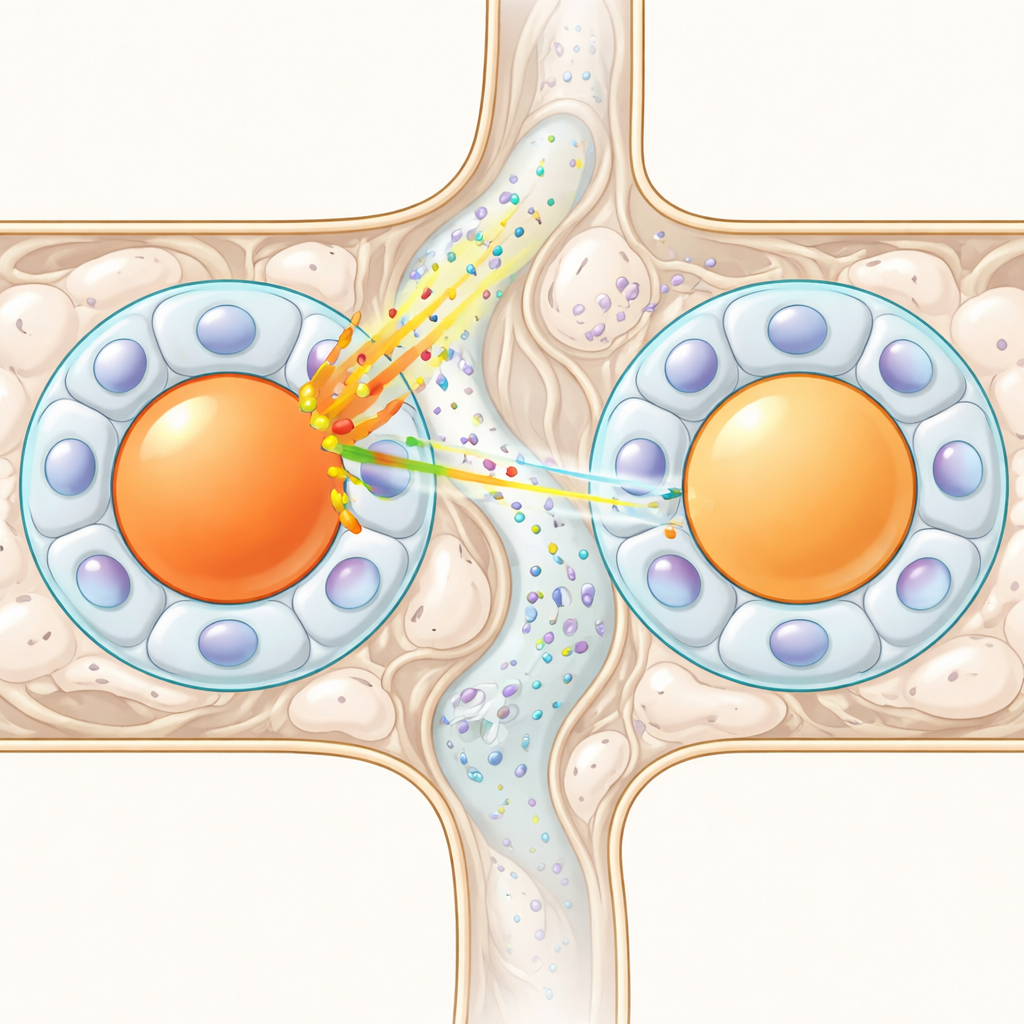
Cuando la estructura hace improbable la conexión
Otro conjunto de hipótesis se basa en puentes físicos entre células. Algunas células gliales satélite forman conexiones directas llamadas uniones gap, o arreglos especiales tipo “sandwich” donde una célula glial se sitúa entre dos cuerpos neuronales y puede transmitir señales químicas. Si tales vínculos fuesen comunes, podrían formar una red que difunda la excitación. Para probar esto, los investigadores construyeron un modelo estadístico 3D de cómo se pueden empaquetar módulos neurona–glía de distintos tamaños dentro de un ganglio, y superpusieron probabilidades conocidas para estas conexiones. Los experimentos sugieren que las uniones gap entre cápsulas distintas son raras —típicamente unos pocos por ciento— y las disposiciones tipo sandwich ocurren en solo alrededor de una de cada diez neuronas. Las simulaciones mostraron que, dadas estas bajas probabilidades y el número limitado de vecinos físicos (típicamente alrededor de siete por neurona), no se pueden alcanzar las tasas muy altas de excitación cruzada observadas experimentalmente. Incluso combinando todos los mecanismos estructurales conocidos, el resultado queda muy por debajo.
Qué significa esto para la percepción y el tratamiento del dolor
Llevando tanto la física como la anatomía a sus límites más generosos —maximizando las fugas iónicas, empaquetando las células lo más posible y asumiendo configuraciones favorables— los autores intentaron dar a las teorías existentes todas las oportunidades para funcionar. Aun así, la difusión de iones, las raras uniones gap y los contactos tipo sandwich juntos no pudieron reproducir la intensidad y la prevalencia de la excitación cruzada observada en tejido real. Para un lector no especialista, la conclusión es clara: el “eco” lateral de la actividad nerviosa en estos ganglios es real y común, pero nuestras explicaciones actuales son incompletas. Falta algo importante sobre cómo las neuronas sensoriales se comunican entre sí antes de que las señales lleguen a la médula espinal. Comprender esta capa oculta de procesamiento podría reformular las ideas sobre la sensación normal y abrir nuevas vías para terapias del dolor, especialmente a medida que los médicos usan cada vez más estimulación eléctrica cerca de estos ganglios para tratar el dolor crónico y ayudar a la recuperación tras lesiones de la médula espinal.
Cita: Perevozniuk, D., Gorskii, O., Musienko, P. et al. A computational analysis of biophysical and geometric constraints refutes existing hypotheses of cross-excitation in dorsal root ganglia. Sci Rep 16, 14306 (2026). https://doi.org/10.1038/s41598-026-40355-3
Palabras clave: ganglio de la raíz dorsal, excitación cruzada, neuronas sensoriales, dolor neuropático, modelado computacional