Clear Sky Science · it
Un’analisi computazionale dei vincoli biofisici e geometrici confuta le ipotesi esistenti di eccitazione incrociata nei gangli delle radici dorsali
Perché le cellule nervose vicine contano
Ogni tocco, dolore o variazione di temperatura che senti ha inizio in piccole aggregazioni di cellule nervose chiamate gangli delle radici dorsali, situati appena fuori dal midollo spinale. Per decenni gli scienziati hanno osservato lì un comportamento curioso: quando una di queste cellule si attiva, i suoi vicini spesso diventano più facili da eccitare, come se il segnale si propagasse silenziosamente di lato. Questa “eccitazione incrociata” potrebbe ristrutturare il nostro modo di pensare al dolore e alla sensazione. Il nuovo studio usa modelli computazionali dettagliati per porre una domanda semplice ma scomoda: le nostre attuali spiegazioni per questo dialogo laterale funzionano davvero?
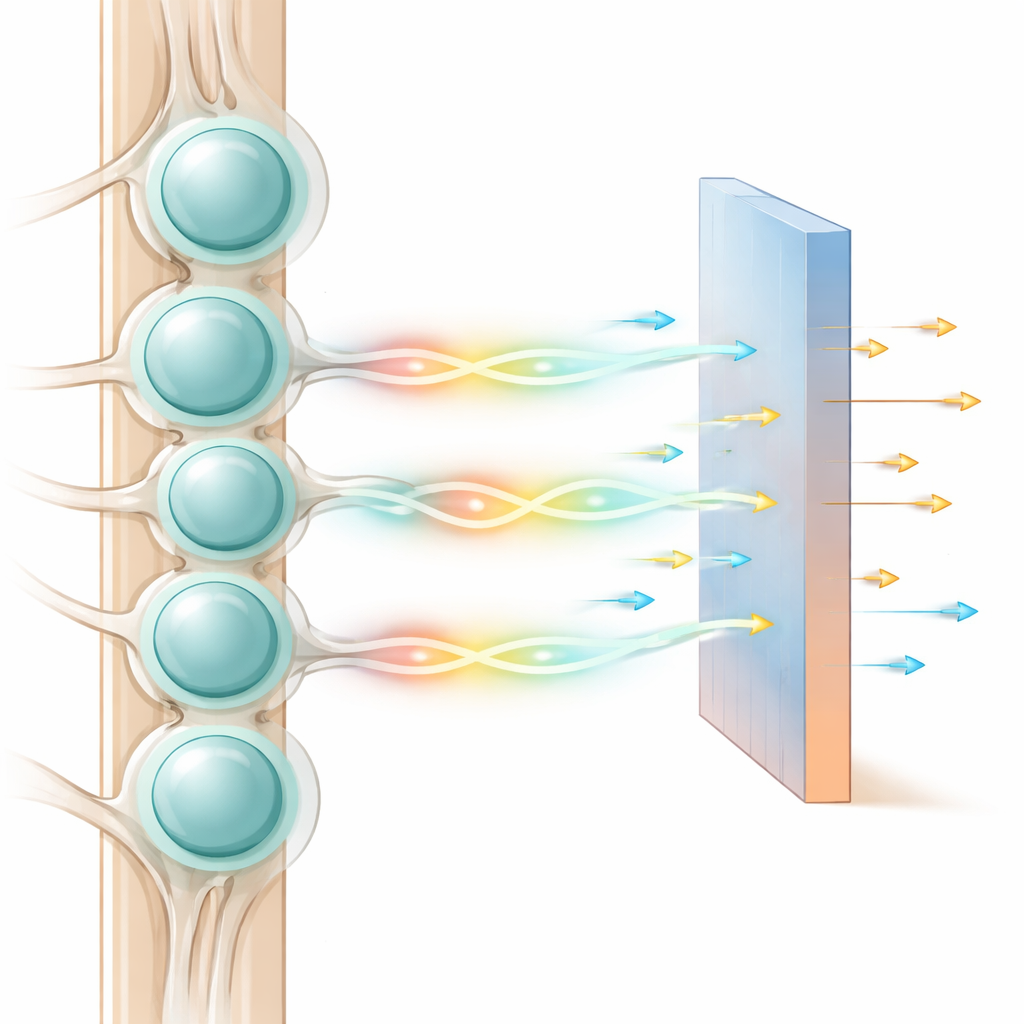
Un quartiere affollato di cellule nervose
I gangli delle radici dorsali sono quartieri densamente popolati di neuroni sensoriali. Il corpo cellulare di ciascun neurone è avvolto da un sottile involucro di cellule di supporto chiamate cellule gliali satelliti, formando una capsula che in gran parte isola un neurone dall’altro. I manuali classici descrivono questi neuroni come semplici relè, che trasmettono segnali al midollo spinale solo quando gli input sono sufficientemente forti. Eppure gli esperimenti hanno mostrato che quando un neurone viene stimolato, molti vicini diventano più eccitabili entro circa mezzo secondo o un secondo. Questo potenziamento lento e ritardato suggerisce un processo chimico o basato sulla diffusione piuttosto che uno elettrico veloce, e appare nella maggior parte delle grandi fibre legate al tatto, indicando un ruolo fondamentale nell’elaborazione sensoriale.
Mettere alla prova l’ipotesi delle perdite di ioni
Una spiegazione principale è che quando un neurone scarica ripetutamente, rilascia ioni potassio nello stretto spazio fluido tra la sua superficie e l’involucro gliale circostante. Se abbastanza potassio si accumulasse e filtrasse attraverso i tessuti circostanti, potrebbe spingere i neuroni vicini più vicini alla soglia di scarica. Gli autori hanno ricostruito un modello molto dettagliato di un neurone sensoriale e della sua capsula gliale, includendo dozzine di canali ionici e pompe, e hanno poi simulato l’aumento dei livelli di potassio dai valori normali a quelli misurati negli esperimenti. Mentre una semplice formula da manuale suggeriva che la tensione del neurone potesse spostarsi di alcuni millivolt—vicino a quanto riportato sperimentalmente—il modello biofisico completo raccontava una storia diversa. Una volta inclusa la regolazione realistica degli ioni da parte sia del neurone sia della glia, lo spostamento di tensione era inferiore a un millivolt, molto troppo piccolo per spiegare l’eccitazione incrociata osservata.
Seguire la traccia attraverso spazi minuscoli
Il gruppo si è quindi chiesto se il potassio potesse semplicemente diffondere da un neurone attivo ai suoi vicini attraverso il labirinto di tessuto connettivo tra le capsule. Hanno collegato due unità neurone–glia modellate con un corridoio extracellulare simulato e hanno eccitato un neurone con impulsi elettrici rapidi, imitando esperimenti passati. Il cambiamento di potenziale nel vicino silente era infinitesimale—dell’ordine di dieci-milionesimi di millivolt. Anche quando hanno compattato i neuroni in modo irrealistico o ridotto lo spazio disponibile a un labirinto stretto, la diffusione produceva effetti notabili solo quando due corpi cellulari erano quasi condivisione di un involucro comune, un’occorrenza rara in condizioni di salute. Dal punto di vista fisico, la diffusione semplicemente non poteva trasportare un segnale abbastanza forte su distanze tipiche.
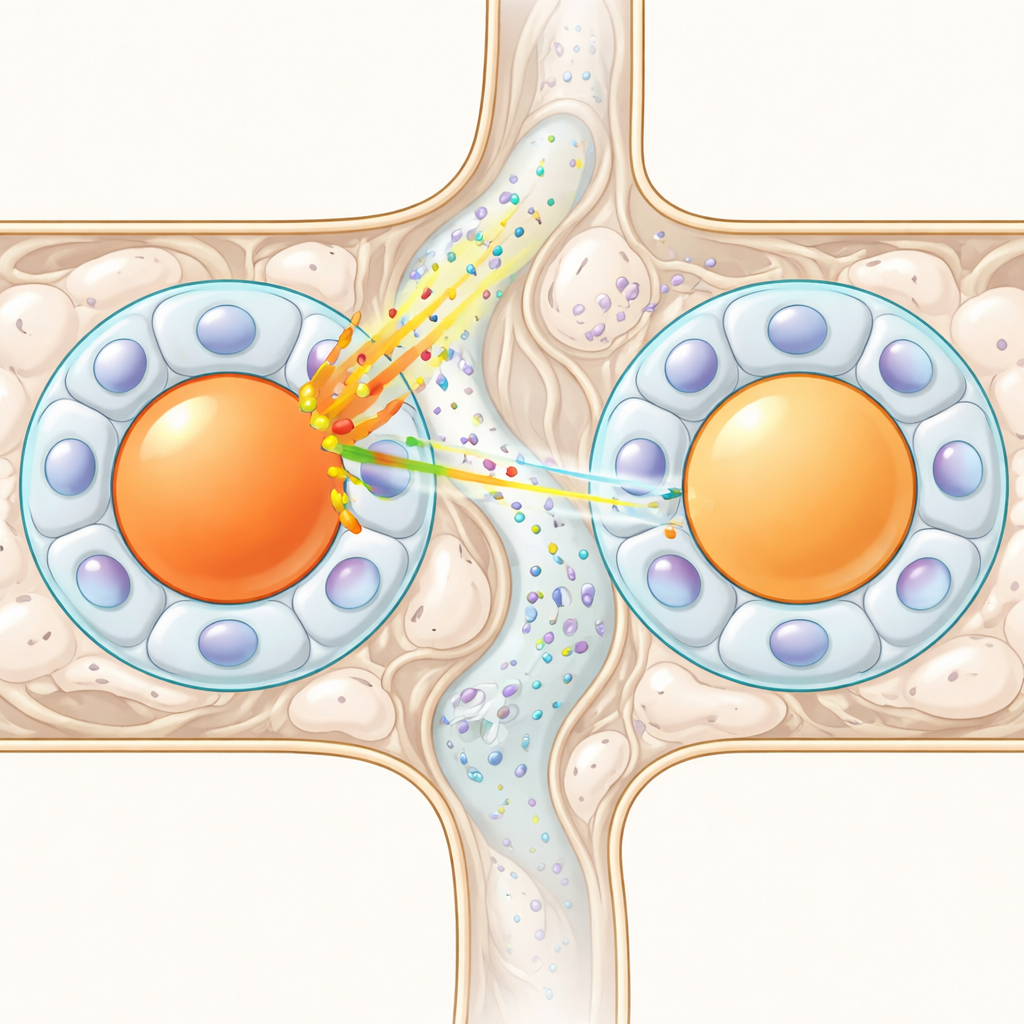
Quando la struttura rende la connessione improbabile
Un altro insieme di ipotesi si basa su ponti fisici tra le cellule. Alcune cellule gliali satelliti formano connessioni dirette chiamate giunzioni gap, o particolari disposizioni a “sandwich” in cui una cellula gliale si interpone tra due corpi neuronali e può trasmettere segnali chimici. Se tali collegamenti fossero comuni, potrebbero creare una rete che diffonde l’eccitazione. Per verificarlo, i ricercatori hanno costruito un modello statistico 3D di come moduli neurone–glia di dimensioni diverse possano essere impacchettati all’interno di un ganglio, quindi hanno sovrapposto le probabilità note per queste connessioni. Gli esperimenti suggeriscono che le giunzioni gap tra capsule distinte sono rare—tipicamente pochi percento—e le disposizioni a sandwich si verificano solo in circa uno ogni dieci neuroni. Le simulazioni hanno mostrato che, date queste basse probabilità e il numero limitato di vicini fisici (di solito circa sette per neurone), non si può raggiungere l’altissima frequenza di eccitazione incrociata osservata sperimentalmente. Anche combinando tutti i meccanismi strutturali noti si resta ben al di sotto dei valori osservati.
Cosa significa per la percezione e il trattamento del dolore
Spingendo sia la fisica sia l’anatomia ai loro limiti più generosi—massimizzando le perdite di ioni, impacchettando le cellule il più possibile e assumendo configurazioni al miglior caso—gli autori hanno cercato di dare alle teorie esistenti ogni possibilità di funzionare. Eppure la diffusione di ioni, le rare giunzioni gap e i contatti a sandwich messi insieme non riuscivano a riprodurre la forza e la prevalenza dell’eccitazione incrociata osservata nei tessuti reali. Per il lettore non specialista, la conclusione è semplice: l’“eco” laterale dell’attività neuronale in questi gangli è reale e comune, ma le nostre spiegazioni attuali sono incomplete. Qualcosa di importante su come i neuroni sensoriali comunicano tra loro prima che i segnali raggiungano il midollo spinale manca ancora. Comprendere questo livello nascosto di elaborazione potrebbe rivedere le idee sulla sensazione normale e aprire nuove strade per le terapie del dolore, specialmente ora che i medici usano sempre più spesso la stimolazione elettrica nei pressi di questi gangli per trattare il dolore cronico e favorire il recupero dopo lesioni del midollo spinale.
Citazione: Perevozniuk, D., Gorskii, O., Musienko, P. et al. A computational analysis of biophysical and geometric constraints refutes existing hypotheses of cross-excitation in dorsal root ganglia. Sci Rep 16, 14306 (2026). https://doi.org/10.1038/s41598-026-40355-3
Parole chiave: ganglio della radice dorsale, eccitazione incrociata, neuroni sensoriali, dolore neuropatico, modellizzazione computazionale