Clear Sky Science · de
Eine rechnergestützte Analyse biophysikalischer und geometrischer Beschränkungen widerlegt bestehende Hypothesen zur Kreuzerregung in dorsalen Wurzelganglien
Warum benachbarte Nervenzellen wichtig sind
Jeder Berührungseindruck, jeder Schmerz und jede Temperaturveränderung beginnt in winzigen Ansammlungen von Nervenzellen, den dorsalen Wurzelganglien, die direkt außerhalb des Rückenmarks liegen. Seit Jahrzehnten beobachten Forscher dort ein seltsames Verhalten: Wenn eine dieser Zellen feuert, lassen sich die Nachbarn oft leichter erregen, als würde das Signal leise seitwärts weitergegeben. Diese „Kreuzerregung“ könnte unser Verständnis von Schmerz und Wahrnehmung verändern. Die neue Studie nutzt detaillierte Computermodelle, um eine einfache, aber unbequeme Frage zu stellen: Funktionieren unsere bisherigen Erklärungen für dieses seitliche Geplapper tatsächlich?
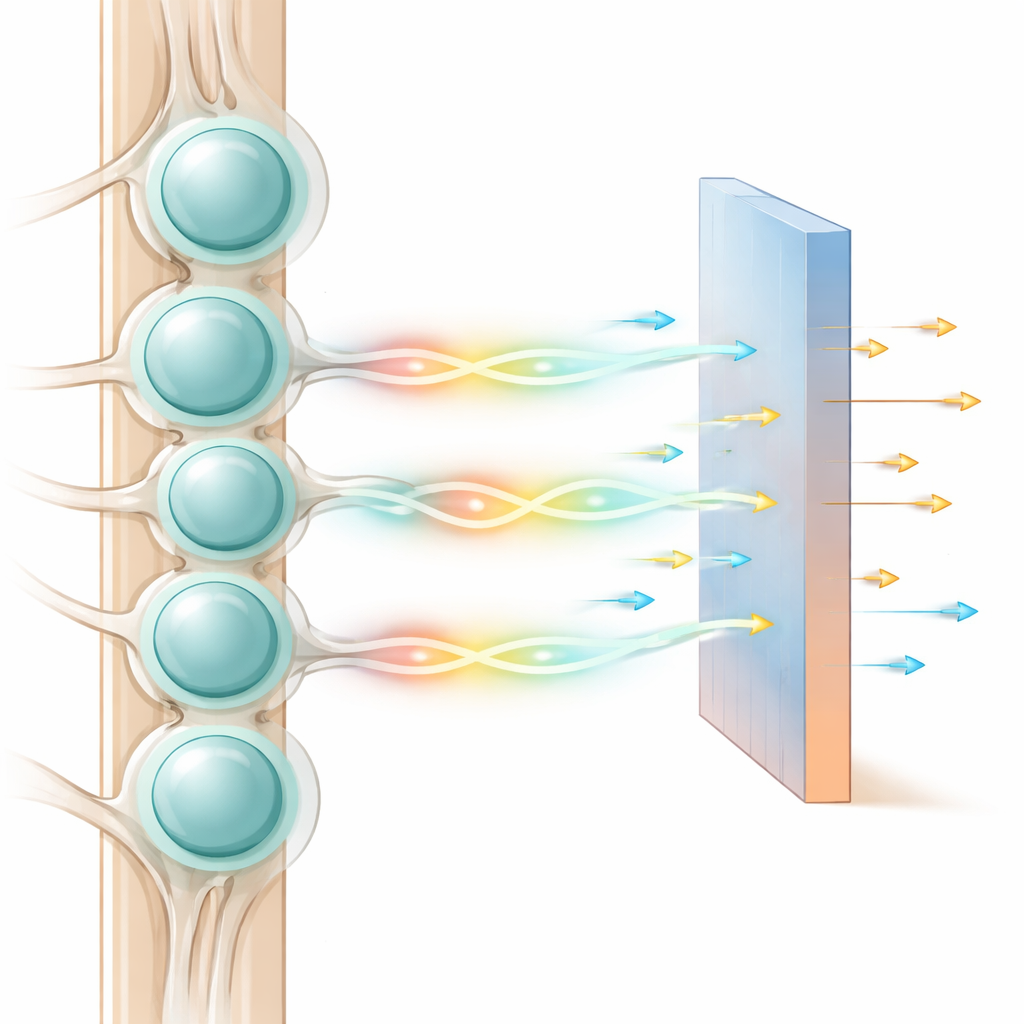
Eine dicht besiedelte Nachbarschaft von Nervenzellen
Dorsale Wurzelganglien sind eng gepackte Nachbarschaften sensorischer Neuronen. Der Zellkörper jedes Neurons ist von einer dünnen Hülle aus Stützzellen, den Satelliten-Gliazellen, umgeben und bildet eine Kapsel, die ein Neuron weitgehend von seinem Nachbarn isoliert. Klassische Lehrbücher beschreiben diese Neuronen als einfache Relais, die Signale nur dann an das Rückenmark weitergeben, wenn die Eingänge stark genug sind. Dennoch zeigen Experimente, dass nach Stimulation einer Zelle viele Nachbarn innerhalb von etwa einer halben bis einer Sekunde erregbarer werden. Dieser langsame, verzögerte Anstieg deutet eher auf einen chemischen oder diffusionsbasierten Prozess als auf einen schnellen elektrischen Mechanismus hin und tritt bei den meisten großen, berührungsrelevanten Fasern auf, was auf eine grundlegende Rolle in der sensorischen Verarbeitung hindeutet.
Die Idee auslaufender Ionen testen
Eine führende Erklärung lautet, dass ein wiederholt feuertes Neuron Kaliumionen in den winzigen Flüssigkeitsraum zwischen seiner Oberfläche und der umgebenden Gliahülle freisetzt. Wenn sich ausreichend Kalium ansammelt und durch das umliegende Gewebe sickert, könnte es benachbarte Neuronen näher an ihre Feuerschwelle bringen. Die Autoren bauten ein sehr detailliertes Modell eines sensorischen Neurons und seiner Glia‑Kapsel nach, inklusive Dutzender Ionenkanäle und Pumpen, und simulierten dann Kaliumspiegel, die von normal bis zu in Experimenten gemessenen Werten anstiegen. Während eine einfache Lehrbuchformel eine Verschiebung der Membranspannung um einige Millivolt nahelegte — in etwa im Bereich dessen, was Experimente berichten — ergab das vollständige biophysikalische Modell ein anderes Bild. Sobald realistische Ionengleichgewichte von sowohl Neuron als auch Glia berücksichtigt wurden, betrug die Spannungsverschiebung weniger als ein Millivolt, also bei weitem zu klein, um die beobachtete Kreuzerregung zu erklären.
Der Spur durch winzige Räume folgen
Das Team fragte anschließend, ob Kalium einfach von einem feuernden Neuron zu seinen Nachbarn diffundieren könnte, durch das labyrinthartige Bindegewebe zwischen den Kapseln. Sie verbanden zwei modellierte Neuron‑Glia‑Einheiten mit einem simulierten extrazellulären Korridor und trieben ein Neuron mit schnellen elektrischen Impulsen, um frühere Experimente zu imitieren. Die Spannungsänderung im stillen Nachbarn war verschwindend klein — in der Größenordnung von zehnmillionstel Millivolt. Selbst wenn sie die Neuronen unrealistisch dicht zusammenpackten oder den verfügbaren Raum zu einem engen Labyrinth reduzierten, erzeugte die Diffusion nur dann spürbare Effekte, wenn zwei Zellkörper nahezu dieselbe Hülle teilten, ein seltener Befund unter gesunden Bedingungen. Aus physikalischer Sicht konnte die Diffusion einfach kein starkes Signal über typische Entfernungen übertragen.
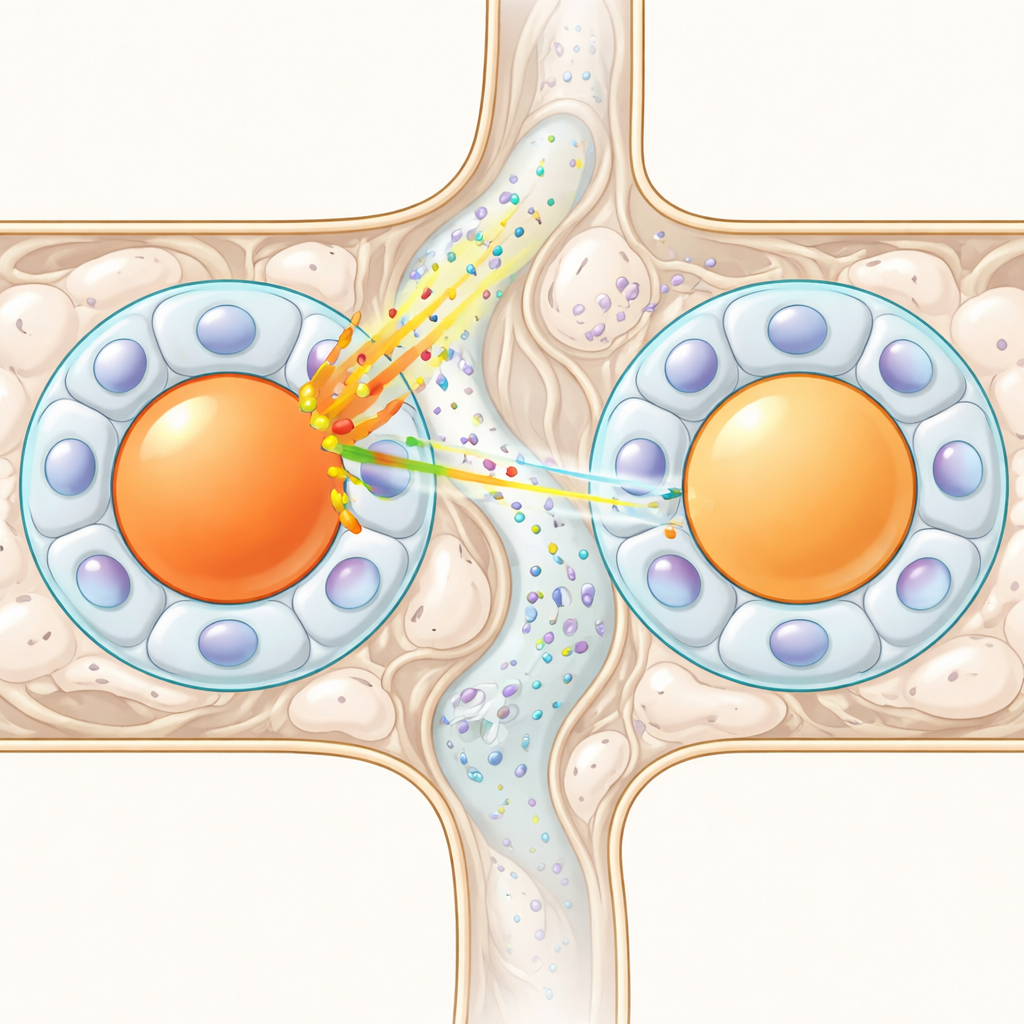
Wenn die Struktur Verbindungen unwahrscheinlich macht
Eine andere Gruppe von Hypothesen stützt sich auf physische Brücken zwischen Zellen. Manche Satelliten‑Gliazellen bilden direkte Verbindungen, sogenannte Gap‑Junctions, oder spezielle „Sandwich“-Anordnungen, bei denen eine Gliazelle zwischen zwei Zellkörpern sitzt und chemische Signale weitergeben kann. Wenn solche Verbindungen häufig wären, könnten sie ein Netzwerk bilden, das Erregung verbreitet. Um das zu testen, erstellten die Forschenden ein 3D‑statistisches Modell, wie Neuron‑Glia‑Module verschiedener Größe in einem Ganglion gepackt sein können, und legten bekannte Wahrscheinlichkeiten für diese Verbindungen darüber. Experimente deuten darauf hin, dass Gap‑Junctions zwischen unterschiedlichen Kapseln selten sind — typischerweise ein paar Prozent — und Sandwich‑Anordnungen bei nur etwa einem von zehn Neuronen vorkommen. Die Simulationen zeigten, dass man bei diesen geringen Wahrscheinlichkeiten und der begrenzten Zahl physischer Nachbarn (typischerweise etwa sieben pro Neuron) nicht die sehr hohen Raten von Kreuzerregung erreichen kann, die experimentell beobachtet werden. Selbst die Kombination aller bekannten strukturellen Mechanismen reicht bei weitem nicht aus.
Was das für Wahrnehmung und Schmerzbehandlung bedeutet
Indem die Autoren sowohl die Physik als auch die Anatomie bis an die großzügigsten Grenzen trieben — maximales Ionenauslaufen, engste Packung der Zellen und Annahme bestmöglicher Konfigurationen — versuchten sie, den bestehenden Theorien jede Chance zu geben. Dennoch konnten Diffusion von Ionen, seltene Gap‑Junctions und Sandwich‑Kontaktierungen zusammen weder die Stärke noch die Häufigkeit der in realem Gewebe beobachteten Kreuzerregung reproduzieren. Für eine allgemein verständliche Aussage heißt das: Das seitliche „Echo“ neuronaler Aktivität in diesen Ganglien ist real und weit verbreitet, aber unsere derzeitigen Erklärungen sind unvollständig. Etwas Wesentliches darüber, wie sensorische Neuronen miteinander kommunizieren, bevor Signale das Rückenmark erreichen, fehlt noch. Das Verständnis dieser verborgenen Verarbeitungsebene könnte Vorstellungen von normaler Empfindung umkrempeln und neue Wege für Schmerztherapien eröffnen — besonders da Ärzte zunehmend elektrische Stimulation in der Nähe dieser Ganglien zur Behandlung chronischer Schmerzen und zur Unterstützung der Erholung nach Rückenmarksverletzungen einsetzen.
Zitation: Perevozniuk, D., Gorskii, O., Musienko, P. et al. A computational analysis of biophysical and geometric constraints refutes existing hypotheses of cross-excitation in dorsal root ganglia. Sci Rep 16, 14306 (2026). https://doi.org/10.1038/s41598-026-40355-3
Schlüsselwörter: dorsaler Wurzelganglion, Kruzzerregung, sensorische Neuronen, neuropathischer Schmerz, computergestütztes Modellieren