Clear Sky Science · nl
Instelbare hydrogel-micropilaararrays voor myelinisatiestudies
Waarom kleine pilaren beschadigde zenuwen kunnen helpen herstellen
Aandoeningen zoals multiple sclerose beschadigen de isolerende laag rond zenuwvezels, waardoor signalen in de hersenen vertragen en problemen ontstaan met bewegen, gezichtsvermogen en denken. Het lichaam heeft cellen die deze isolatie kunnen herbouwen, maar wetenschappers hebben nog steeds moeite om te voorspellen welke geneesmiddelen hen daadwerkelijk zullen helpen hun werk te doen. Dit artikel beschrijft een slimme in het lab gemaakte omgeving van kleine, zachte pilaren die zenuwvezels imiteren, en die onderzoekers een veel realistischere manier biedt om te observeren en te meten hoe hersencellen isolatie herstellen — en om toekomstige behandelingen veilig en efficiënt te testen.
Een kunstmatig bos van zenuwachtige paaltjes bouwen
Het team creëerde een platform van een waterig gelmateriaal, een beetje zoals zeer stevige Jell‑O, bezaaid met duizenden rechtopstaande microscopische pilaren. Deze pilaren fungeren als vervanging voor zenuwvezels in de hersenen. Met standaard chipfabricagetechnieken konden de onderzoekers nauwkeurig instellen hoe breed elke pilaar was, hoe ver pilaren uit elkaar stonden en hoe stijf of zacht ze waren. Het bereik loopt van hersenachtige zachtheid tot veel stijvere omstandigheden, vergelijkbaar met ander weefsel in het lichaam, terwijl de vormen in maten blijven die overeenkomen met echte zenuwvezels. Dit raster van uniforme pilaren staat in een kleine put, zodat slechts bescheiden aantallen cellen en weinig vloeistof nodig zijn voor experimenten.
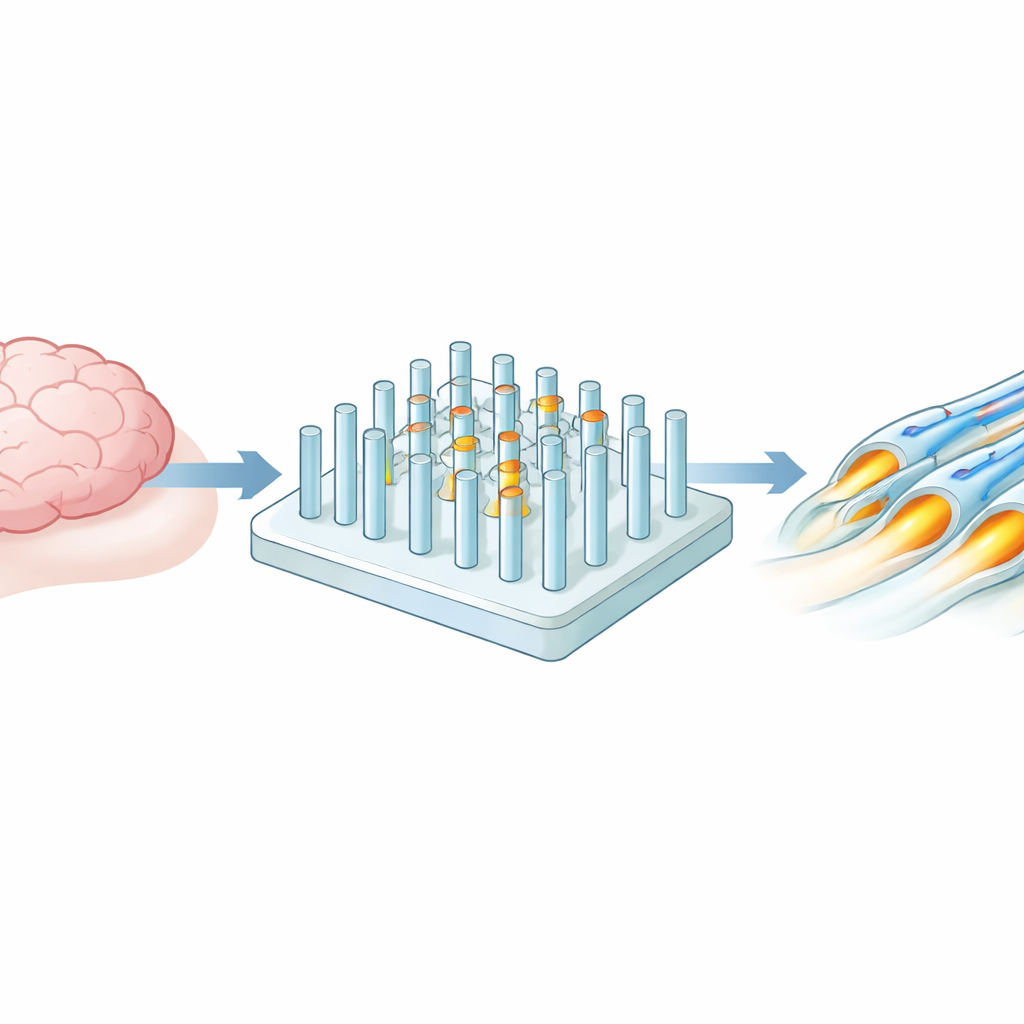
Hersencellen overtuigen de pilaren te omwikkelen
Vervolgens plaatsten de onderzoekers oligodendrocyten — gespecialiseerde hersencellen die normaal zenuwvezels in myeline wikkelen — op deze pilaararrays. Gedurende twee weken volgden ze hoe de cellen groeiden, veranderden en uiteindelijk lange uitlopers uitstuurden die zich om de pilaren kronkelden. Met geavanceerde microscopen, waaronder 3D-confocale beeldvorming en elektronenmicroscopie, zagen ze meerdere compacte lagen isolatie ontstaan rond veel van de gelpaaltjes, zeer vergelijkbaar met natuurlijke myeline in de hersenen. Meer dan de helft van de pilaren droeg meervoudige wikkelingen, en de dikte van de isolatielaag kwam nauw overeen met het aantal windingen dat de cel had gemaakt, wat bevestigde dat een eenvoudige fluorescentiekleuring betrouwbaar kon optreden in plaats van arbeidsintensievere ultrastructuurcontroles.
Hoe vorm, afstand en zachtheid de isolatie sturen
Omdat het platform zo instelbaar is, kon het team systematisch onderzoeken welke fysieke eigenschappen het belangrijkst zijn. Ze varieerden pilaarbreedte en -afstand om de diversiteit aan zenuwvezelgroottes in echt hersenweefsel na te bootsen. Dikkere pilaren werden vaker en vollediger omwikkeld, wat het spiegelbeeld is van hoe grotere zenuwvezels in levende hersenen de voorkeur krijgen bij isolatie. Wanneer pilaren zeer dun waren maar te dicht opeengepakt, had elke cel meer potentiële doelen dan ze aankon, en daalde de efficiëntie van het omwikkelen. De verhouding van pilaarmaat tot coatingsdikte — de zogenaamde g-ratio die neurowetenschappers gebruiken — viel binnen het bereik dat in gezond centraal zenuwstelselweefsel wordt gezien, wat suggereert dat het kunstmatige systeem kernaspecten van het natuurlijke ontwerp vangt.
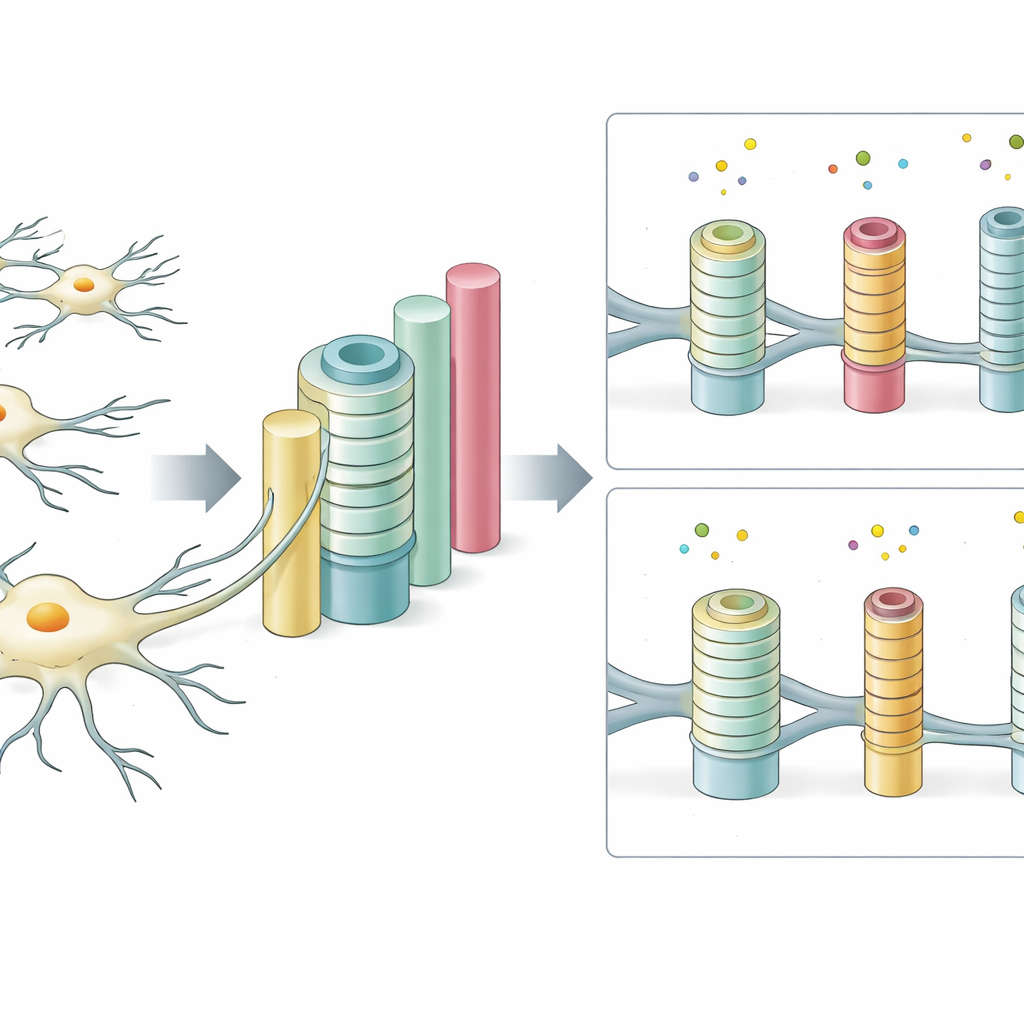
Het gevoel en het oppervlak van het landschap veranderen het celgedrag
Buiten de geometrie beïnvloedde ook de ‘gevoel’ van de omgeving sterk hoe goed cellen isolatie vormden. Op zeer zachte pilaren die sponsachtig hersenweefsel nabootsten, trad enige wikkeling op, maar die was verminderd voor bepaalde pilaarmaten. Naarmate pilaren steviger werden, nam het omwikkelen over het algemeen toe, vooral op grotere paaltjes. De onderzoekers veranderden ook de moleculen die het pilaaroppervlak bekleden. Bekleden met laminine, een natuurlijk onderdeel van het ondersteunende netwerk in de hersenen, bevorderde omwikkeling, terwijl fibronectine veranderde hoeveel pilaren elke cel volledig kon omringen. Toen ze veranderingen in zachtheid en oppervlaktechemie combineerden, zagen ze dat beide factoren gezamenlijk bepaalden hoeveel pilaren volledig geïsoleerd werden, wat benadrukt hoe gevoelig deze cellen zijn voor subtiele fysieke en chemische signalen.
Medicijneffecten blootleggen — en valse beloften
Het team veranderde het systeem vervolgens in een testplatform voor potentiële geneesmiddelen. Ze brachten verschillende verbindingen aan die eerder waren voorgesteld om myelineherstel te bevorderen, samen met één stof waarvan bekend is dat deze het proces belemmert. Het platform pikte duidelijke verhogingen in omwikkeling op voor kandidaat ‘pro-myelinerende’ geneesmiddelen en dosisafhankelijke afnames voor de remmer. Cruciaal was dat de schijnbare sterkte van sommige geneesmiddelen afhing van hoe stijf de pilaren waren. Op stijvere paaltjes leken middelen krachtiger; op zachtere, hersenachtige pilaren waren hun voordelen kleiner. Dit suggereert dat oudere, te stijve labmodellen de belofte van bepaalde verbindingen hebben kunnen overschatten, wat helpt verklaren waarom sommige faalden in klinische proeven ondanks veelbelovende vroege gegevens.
Menselijke biologie in beeld brengen
Om het systeem relevanter te maken voor patiënten toonden de onderzoekers aan dat het niet alleen werkt met knaagdiercellen maar ook met menselijke cellen afkomstig van foetaal weefsel en van menselijke stamcellen. Deze menselijke oligodendrocyten strekten lange, ingewikkelde uitlopers uit en omgorden de gelpilaren, en in het geval van stamcel-afgeleide cellen vormden ze zelfs compacte, meerlagige isolatie. Dat betekent dat het platform kan worden gecombineerd met moderne stamceltechnologieën, inclusief patiëntspecifieke lijnen, om menselijke ziekten die myeline aantasten te modelleren en om op maat gemaakte behandelingen te zoeken.
Wat dit betekent voor toekomstige behandelingen
In eenvoudige bewoordingen biedt dit werk een realistisch miniatuurspeelveld waar isolatievormende hersencellen kunnen interageren met levensechte ‘nepzenuwen’. Omdat de grootte, afstand, zachtheid en het oppervlak van de pilaren allemaal bestuurd kunnen worden, kunnen wetenschappers ontleden hoe elk kenmerk het myelineherstel vormt en hoe potentiële geneesmiddelen zich daadwerkelijk gedragen in een hersenachtige omgeving. Door misleidende resultaten van te stijve of platte labsystemen te verminderen en doordat het goed werkt met menselijke cellen, kan dit instelbare pilaarplatform de ontdekking van betrouwbaardere therapieën voor multiple sclerose en verwante aandoeningen versnellen, en de mogelijkheid om beschadigde zenuwisolatie te herstellen dichterbij brengen.
Bronvermelding: Lasli, S., Vinel, C., Agrawal, A. et al. Tunable hydrogel-based micropillar arrays for myelination studies. Nat Methods 23, 854–864 (2026). https://doi.org/10.1038/s41592-026-03048-3
Trefwoorden: myelinisatie, hydrogel-micropilaren, oligodendrocyten, mechanobiologie, multiple sclerose