Clear Sky Science · de
Abstimmbare Hydrogel‑Mikropfahl‑Arrays für Myelinisierungsstudien
Warum winzige Pfeiler geschädigte Nerven reparieren helfen könnten
Erkrankungen wie Multiple Sklerose schädigen die Isolierschicht um Nervenfasern, verlangsamen die Signale im Gehirn und verursachen Probleme mit Bewegung, Sehen und Denken. Der Körper besitzt Zellen, die diese Isolierung wieder aufbauen können, doch Wissenschaftler tun sich noch schwer damit, vorherzusagen, welche Wirkstoffe ihnen dabei tatsächlich helfen. Diese Arbeit beschreibt eine clevere, im Labor hergestellte Landschaft aus winzigen, weichen Pfeilern, die Nervenfasern nachahmen und Forschern eine wesentlich realistischere Möglichkeit bieten, zu beobachten und zu messen, wie Gehirnzellen die Isolierung wiederherstellen — und zukünftige Behandlungen sicher und effizient zu testen.
Ein künstlicher Wald aus nervenähnlichen Pfosten
Das Team entwickelte eine Plattform aus einem wasserreichen Gel, etwas wie sehr fester Götterspeise, durchsetzt mit Tausenden aufrechten mikroskopischen Pfeilern. Diese Pfeiler stehen für Nervenfasern im Gehirn. Mittels üblicher Chip‑Herstellungstechniken konnten die Forschenden präzise einstellen, wie breit jeder Pfeiler war, wie weit die Pfeiler voneinander entfernt standen und wie steif oder weich sie waren. Der Bereich reicht von gehirnähnlicher Weichheit bis zu deutlich festeren Bedingungen, vergleichbar mit anderem Körpergewebe, wobei die Formen in Größen gehalten werden, die echten Nervenfasern entsprechen. Dieses Gitter gleichförmiger Pfeiler liegt in einer kleinen Vertiefung, sodass für Experimente nur geringe Zellzahlen und wenig Flüssigkeit benötigt werden.
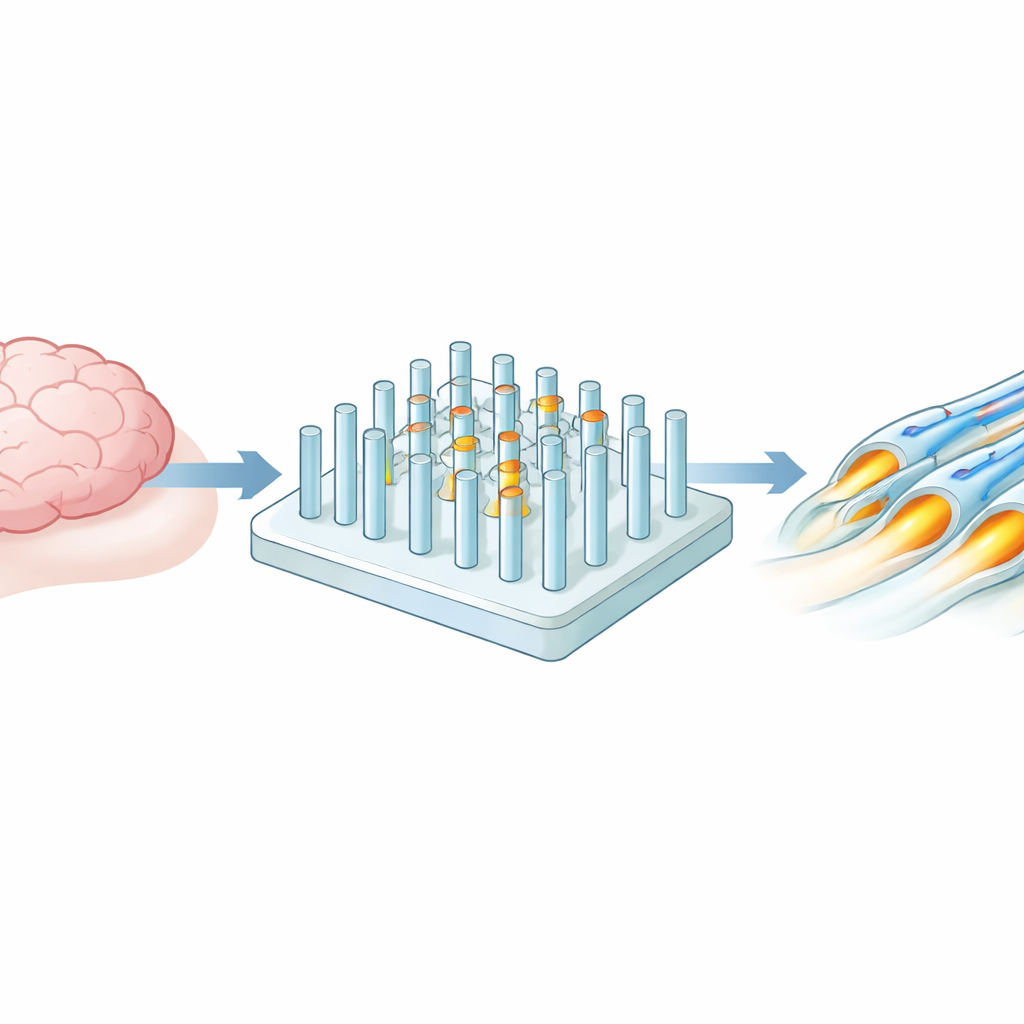
Gehirnzellen zum Umschlingen der Pfeiler bringen
Als Nächstes setzten die Forschenden Oligodendrozyten — spezialisierte Gehirnzellen, die normalerweise Nervenfasern mit Myelin umhüllen — auf diese Pfeiler‑Arrays. Über zwei Wochen beobachteten sie, wie die Zellen wuchsen, sich veränderten und schließlich lange Fortsätze ausbildeten, die sich um die Pfeiler wickelten. Mit fortgeschrittenen Mikroskopen, darunter 3D‑Konfokalmikroskopie und Elektronenmikroskopie, sahen sie an vielen Gelpfosten mehrere kompakte Isolationsschichten entstehen, sehr ähnlich zum natürlichen Myelin im Gehirn. Mehr als die Hälfte der Pfeiler war mehrfach umwickelt, und die Dicke der Isolierschicht stimmte eng mit der Anzahl der Wicklungen überein, was bestätigte, dass ein einfacher Fluoreszenzfarbstoff zuverlässig anstelle aufwändiger ultrastruktureller Untersuchungen verwendet werden kann.
Wie Form, Abstand und Weichheit die Isolierung steuern
Da die Plattform so gut einstellbar ist, konnte das Team systematisch untersuchen, welche physikalischen Eigenschaften am wichtigsten sind. Sie variierten Pfeilerbreite und Abstand, um die Vielfalt der Nervenfasergrößen im echten Gehirngewebe zu spiegeln. Dickere Pfeiler wurden häufiger und vollständiger umhüllt, was dem Phänomen entspricht, dass größere Nervenfasern im lebenden Gehirn bevorzugt isoliert werden. Waren die Pfeiler sehr dünn, aber zu dicht gepackt, hatte jede Zelle mehr potenzielle Ziele, als sie bearbeiten konnte, und die Effizienz der Umwicklung sank. Das Verhältnis von Pfeilergröße zur Beschichtungsdicke — das sogenannte g‑Ratio, das Neurowissenschaftler verwenden — lag im Bereich des gesunden zentralen Nervensystems, was darauf hinweist, dass das künstliche System zentrale Aspekte des natürlichen Aufbaus erfasst.
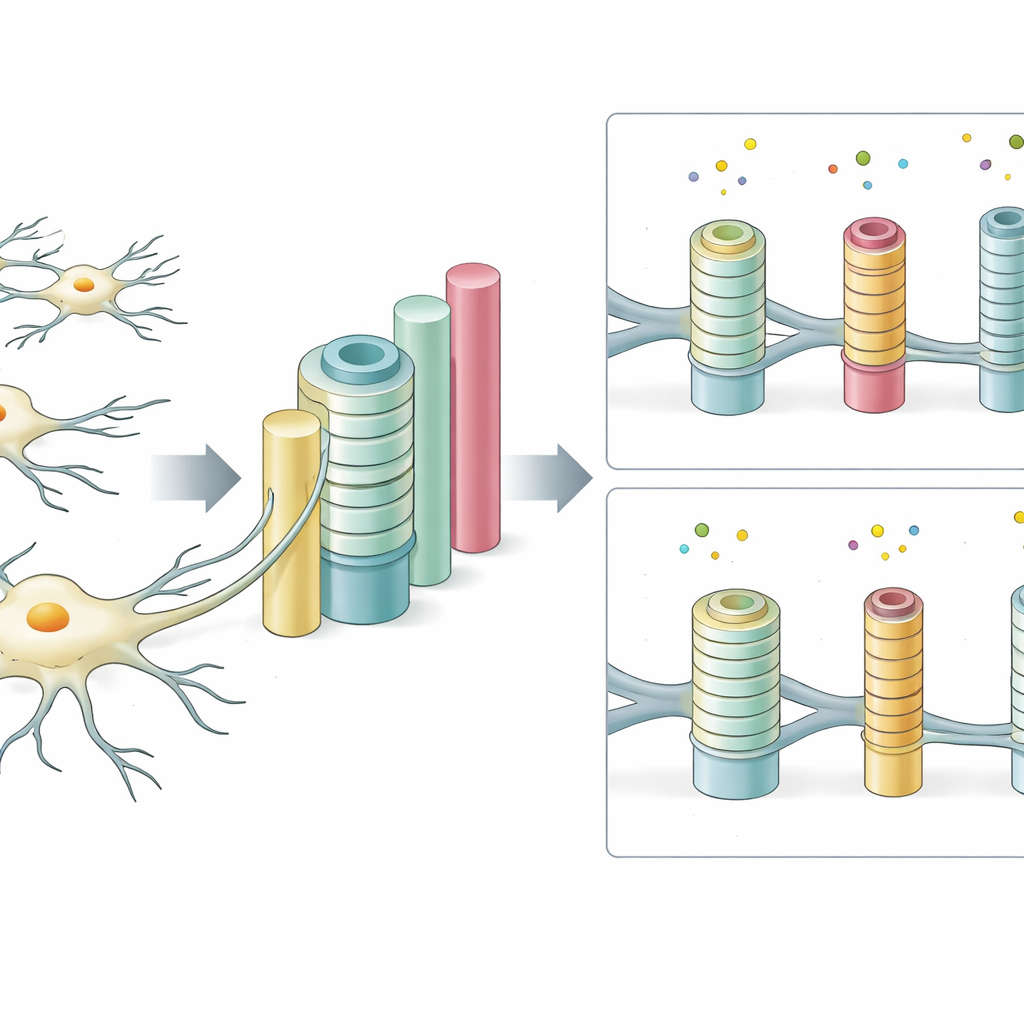
Die Haptik und Oberfläche der Landschaft verändern das Zellverhalten
Über die Geometrie hinaus beeinflusste auch die „Haptik“ der Umgebung stark, wie gut Zellen Isolierung bildeten. Auf sehr weichen Pfeilern, die schwammiges Gehirngewebe nachahmten, trat zwar eine gewisse Umwicklung auf, sie war aber für bestimmte Pfeilergrößen vermindert. Mit zunehmender Festigkeit nahm die Umwicklung allgemein zu, insbesondere an größeren Pfosten. Die Forschenden veränderten außerdem die Moleküle, die die Pfeileroberfläche schmückten. Eine Beschichtung mit Laminin, einem natürlichen Baustein des neuronalen Stützgewebes, förderte die Umwicklung, während Fibronectin beeinflusste, wie viele Pfeiler jede Zelle vollständig umschließen konnte. Kombinierten sie Änderungen in Weichheit und Oberflächenchemie, zeigte sich, dass beide Faktoren gemeinsam steuern, wie viele Pfeiler vollständig isoliert werden — ein Hinweis darauf, wie empfindlich diese Zellen auf subtile physikalische und chemische Signale reagieren.
Aufdecken von Arzneiwirkungen — und falschen Versprechungen
Das Team nutzte das System anschließend als Prüfstand für potenzielle Medikamente. Sie setzten mehrere Verbindungen ein, die zuvor als förderlich für Myelinreparatur vorgeschlagen wurden, sowie eine, die bekanntermaßen den Prozess stört. Die Plattform zeigte klare Zunahmen der Umwicklung für vielversprechende „pro‑myelinisierende“ Wirkstoffe und dosisabhängige Abnahmen für den Inhibitor. Entscheidenderweise hing die scheinbare Wirksamkeit mancher Wirkstoffe davon ab, wie steif die Pfeiler waren. An steiferen Pfosten wirkten die Medikamente potenter; an weicheren, gehirnähnlichen Pfeilern waren ihre Vorteile kleiner. Das legt nahe, dass ältere, zu starre Labor‑Modelle das Potenzial bestimmter Verbindungen überschätzt haben könnten und erklärt, warum einige in klinischen Studien trotz vielversprechender Vorbefunde versagten.
Menschliche Biologie ins Spiel bringen
Um das System patientenrelevanter zu machen, zeigten die Forschenden, dass es nicht nur mit Rodentenzellen funktioniert, sondern auch mit menschlichen Zellen aus fetalem Gewebe und mit humanen Stammzellen. Diese menschlichen Oligodendrozyten bildeten lange, verzweigte Fortsätze und umhüllten die Gelpfeiler; bei Stammzell‑abgeleiteten Zellen entstanden sogar kompakte, mehrschichtige Isolierungen. Das bedeutet, die Plattform lässt sich mit modernen Stammzelltechnologien koppeln, einschließlich patientenspezifischer Zelllinien, um menschliche Erkrankungen, die Myelin betreffen, zu modellieren und maßgeschneiderte Therapien zu suchen.
Was das für zukünftige Behandlungen bedeutet
Kurz gesagt bietet diese Arbeit einen realistischen Miniaturspielplatz, auf dem isolierungsbildende Gehirnzellen mit lebensnahen „künstlichen Nerven“ interagieren können. Da Größe, Abstand, Weichheit und Oberfläche der Pfeiler alle kontrollierbar sind, können Wissenschaftler untersuchen, wie jede Eigenschaft die Myelinreparatur beeinflusst und wie potenzielle Medikamente sich in einer gehirnähnlichen Umgebung tatsächlich verhalten. Indem irreführende Ergebnisse aus zu starren oder flachen Labormodellen reduziert werden und die Plattform gut mit menschlichen Zellen zusammenarbeitet, könnte dieses einstellbare Pfeiler‑System die Entdeckung verlässlicherer Therapien für Multiple Sklerose und verwandte Erkrankungen beschleunigen und die Aussicht, beschädigte Nervenisolierungen wiederherzustellen, näher rücken.
Zitation: Lasli, S., Vinel, C., Agrawal, A. et al. Tunable hydrogel-based micropillar arrays for myelination studies. Nat Methods 23, 854–864 (2026). https://doi.org/10.1038/s41592-026-03048-3
Schlüsselwörter: Myelinisierung, Hydrogel‑Mikropfähle, Oligodendrozyten, Mechanobiologie, Multiple Sklerose