Clear Sky Science · ja
ミエリン化研究のための可変性ハイドロゲル微小柱アレイ
なぜ小さな柱が損傷した神経を修復する手掛かりになるのか
多発性硬化症のような病気は、神経線維を取り巻く絶縁被膜(ミエリン)を損なわせ、脳からの信号伝達を遅らせ、運動や視覚、認知に問題を引き起こします。体内にはこの被膜を再生できる細胞が存在しますが、それらを本当に助ける薬を予測するのは依然として困難です。本論文は、神経線維を模した小さく柔らかな柱が規則的に並んだ巧妙な人工基盤を紹介しており、研究者が脳細胞のミエリン再構築をより現実的に観察・計測し、将来の治療法を安全かつ効率的に試験できる方法を提供します。
神経のような柱の“ミニ森林”を作る
研究チームは、水分を多く含むゲル、いわば非常に堅いゼリーのような素材に、何千もの直立した微小な柱を配置したプラットフォームを作成しました。これらの柱は脳内の神経線維を代替します。標準的なチップ製造技術を用いることで、柱の太さ、柱間の距離、そして剛性(硬さ)を正確に調整できるようにしました。その範囲は脳に近い柔らかさから、他の組織に似たはるかに硬い条件まで及び、形状は実際の神経線維に見合うサイズで保持されています。この均一な柱の格子は小さなウェルに収まるため、実験に必要な細胞数や液体量は控えめです。
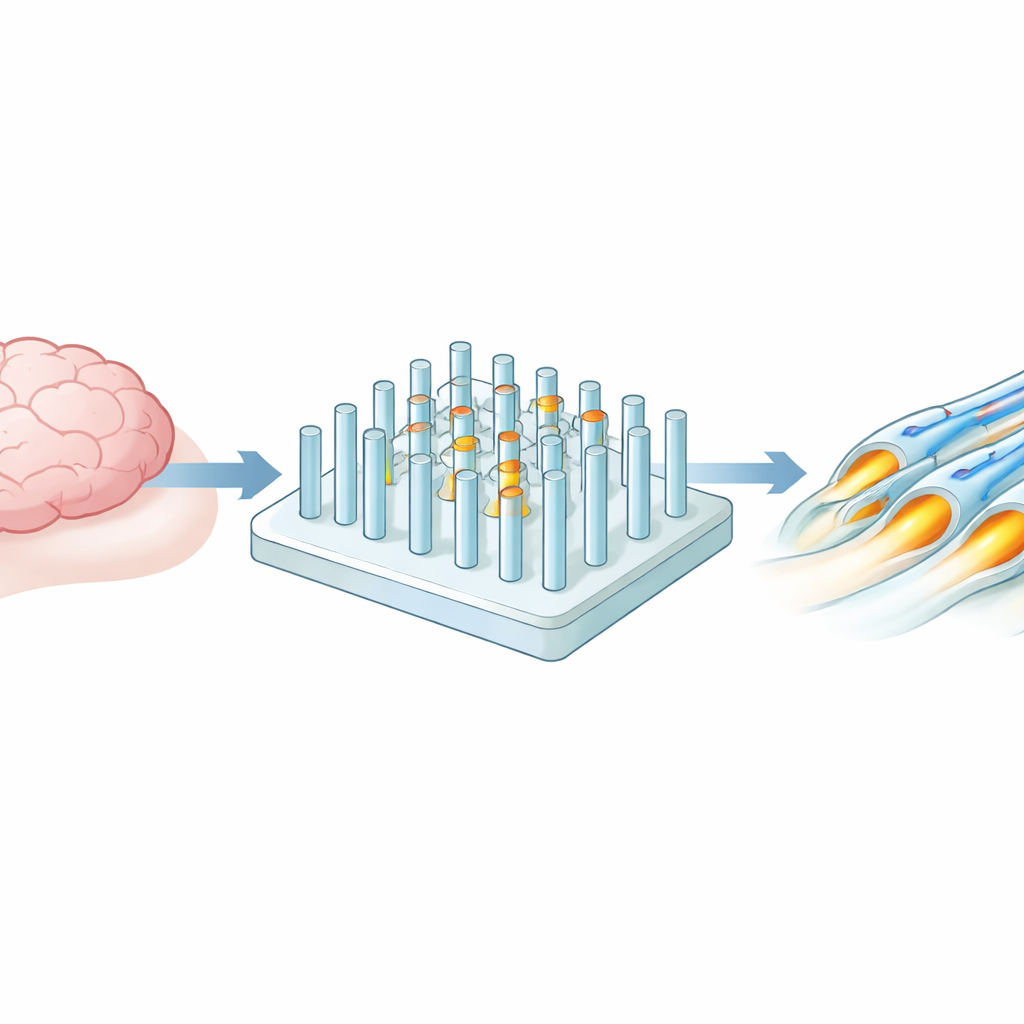
脳の細胞に柱を巻き付かせる
次に研究者は、通常ミエリンで神経線維を包むオリゴデンドロサイトをこれらの柱アレイに配置しました。2週間にわたり、細胞が成長・変化し、やがて長い突起を伸ばして柱を巻き付ける様子を観察しました。3D共焦点イメージングや電子顕微鏡などの高度な顕微鏡で、多くのゲル柱の周りに多重の緊密な絶縁層が形成されているのを確認し、これは脳内の天然ミエリンに非常によく似ていました。半数以上の柱に多層の巻き付きが見られ、絶縁層の厚さは細胞が何回巻いたかと密接に一致しており、単純な蛍光染色が手間のかかる超微細構造学的検査の信頼できる代替になり得ることを示しました。
形状、間隔、柔らかさがミエリン形成をどう導くか
プラットフォームが非常に調整可能であるため、どの物理的特徴が重要かを系統的に調べることができました。柱の幅と間隔を変えて、実際の脳組織に見られる神経線維の多様性を再現しました。太い柱ほどより頻繁かつ完全に巻き付けられ、生体の大型神経線維が優先的に絶縁される挙動を反映していました。柱が非常に細く、しかも過度に密集していると、各細胞が扱うべき標的が多すぎて巻き付き効率が低下しました。柱サイズと被覆厚の比率、いわゆる神経科学で使われるg比は健常な中枢神経系組織で見られる範囲に収まり、この人工系が自然の設計の重要な側面を再現していることを示唆しました。
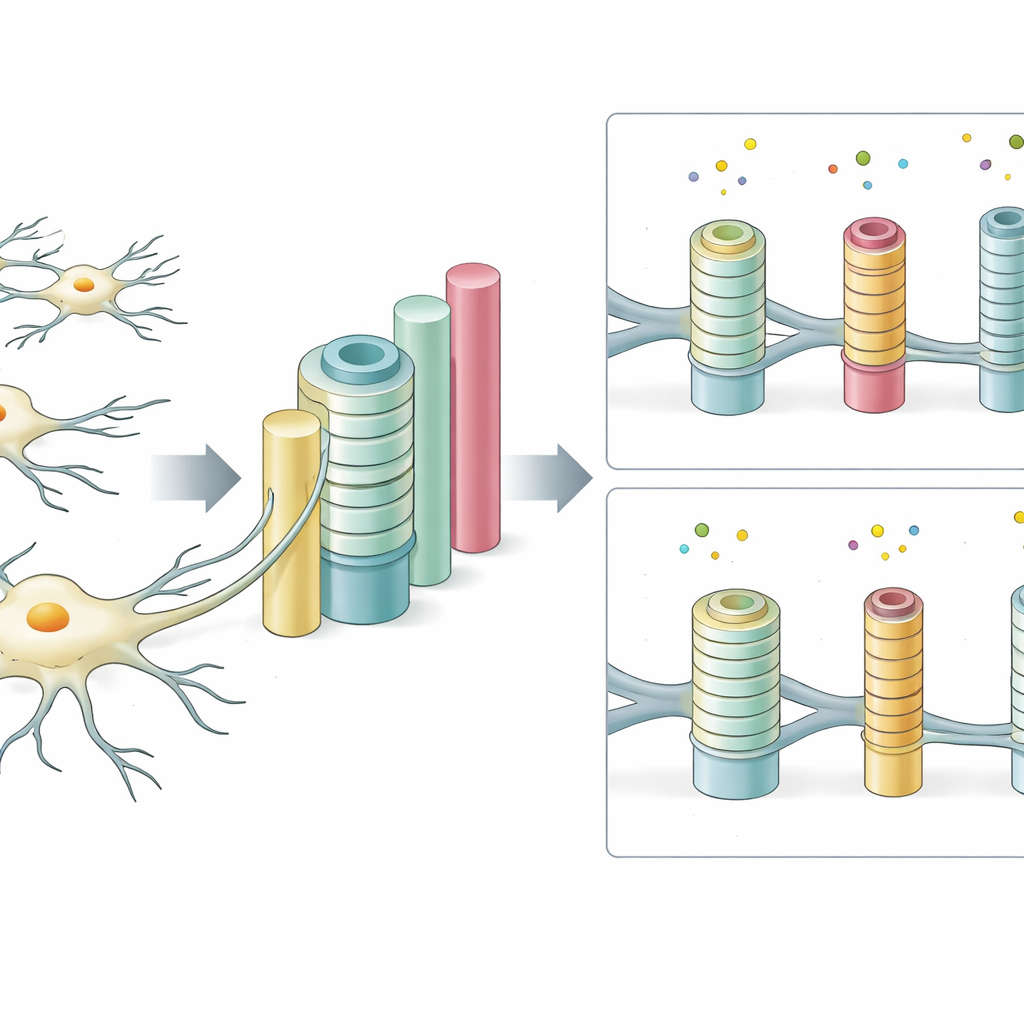
環境の“感触”と表面が細胞挙動を変える
幾何学的条件に加え、環境の「感触」も細胞の絶縁形成に強く影響しました。脳組織の柔らかさを模した非常に柔らかい柱では一部の巻き付きが見られましたが、特定の柱サイズでは低下しました。柱がより硬くなると、特に大きな柱で巻き付きは概して増加しました。また、柱表面を飾る分子も変更しました。脳の支持基質の自然成分であるラミニンでコーティングすると巻き付きが促進され、フィブロネクチンは各細胞が完全に取り囲める柱の数に変化をもたらしました。柔らかさと表面化学の変化を組み合わせると、どちらの要因も完全に絶縁された柱の数を共同で制御していることが分かり、これらの細胞が微妙な物理的・化学的手がかりに非常に敏感であることを強調しました。
薬剤の効果を明らかにする―そして誤った期待も暴く
研究チームはこの系を潜在的な薬剤の試験台に転用しました。これまでにミエリン修復を促進すると提案された複数の化合物と、過程を阻害することが知られている一種の阻害剤を適用しました。プラットフォームは候補となる「プロミエリン化」薬で明確な巻き付き増加を捉え、阻害剤では用量依存的な減少を示しました。重要なのは、いくつかの薬の見かけ上の効果が柱の硬さに依存していたことです。硬い柱上では薬はより強力に見え、柔らかく脳に近い柱上ではその利益は小さくなりました。これは、古い過度に硬い実験モデルが特定の化合物の有望さを過大評価していた可能性を示し、一部の薬が臨床試験で期待外れに終わった理由の説明に繋がります。
ヒト生物学を取り入れる
患者により関連する系にするため、研究者はこの方法がげっ歯類の細胞だけでなく、胎児組織由来のヒト細胞やヒト幹細胞由来の細胞でも機能することを示しました。これらのヒトオリゴデンドロサイトは長く複雑な突起を伸ばしてゲル柱を巻き付け、幹細胞由来の細胞では緊密な多層の絶縁も形成しました。つまり、このプラットフォームは患者特異的な系を含む現代の幹細胞技術と組み合わせることができ、ミエリンに影響を与えるヒトの疾患をモデル化し、個別化された治療法を探索するのに適しているということです。
将来の治療にとっての意義
簡単に言えば、この研究はミエリンを形成する脳細胞が実物に近い「人工神経」と相互作用できる現実的なミニチュアの遊び場を提供します。柱のサイズ、間隔、柔らかさ、表面を全て制御できるため、各特徴がミエリン修復にどのように影響するか、そして潜在的な薬剤が脳に近い環境でどのように振る舞うかを詳細に解析できます。過度に硬いまたは平坦な従来の実験系がもたらす誤解を減らし、ヒト細胞とも相性が良いため、この可変性柱プラットフォームは多発性硬化症や関連疾患に対するより信頼できる治療法の発見を加速し、損傷した神経被膜の回復という見通しを現実に近づける可能性があります。
引用: Lasli, S., Vinel, C., Agrawal, A. et al. Tunable hydrogel-based micropillar arrays for myelination studies. Nat Methods 23, 854–864 (2026). https://doi.org/10.1038/s41592-026-03048-3
キーワード: ミエリン形成, ハイドロゲル微小柱, オリゴデンドロサイト, 機械生物学, 多発性硬化症