Clear Sky Science · fr
Réseaux de micropiliers hydrogel ajustables pour l’étude de la myélinisation
Pourquoi de minuscules piliers peuvent aider à réparer les nerfs endommagés
Des maladies comme la sclérose en plaques endommagent la gaine isolante qui entoure les fibres nerveuses, ralentissant la transmission des signaux cérébraux et provoquant des troubles de la motricité, de la vision et des fonctions cognitives. L’organisme possède des cellules capables de reconstruire cette isolation, mais les chercheurs peinent encore à prédire quels médicaments les aideront réellement à accomplir ce travail. Cet article décrit un dispositif ingénieux composé de minuscules piliers souples conçus en laboratoire pour imiter les fibres nerveuses, offrant aux chercheurs une manière plus réaliste d’observer et de mesurer la reconstruction de la gaine par les cellules cérébrales — et de tester des traitements futurs de façon sûre et efficace.
Construire une forêt artificielle de poteaux semblables à des nerfs
L’équipe a créé une plateforme en gel riche en eau, un peu comme une gélatine très ferme, parsemée de milliers de micropiliers verticaux. Ces piliers représentent les fibres nerveuses du cerveau. En utilisant des techniques de microfabrication classiques, les chercheurs ont pu ajuster précisément la largeur de chaque pilier, l’espacement entre eux et leur rigidité. La plage de propriétés va d’une souplesse proche de celle du cerveau à des conditions beaucoup plus rigides, comparables à d’autres tissus du corps, tout en conservant des dimensions proches de celles des fibres nerveuses réelles. Cette grille de piliers uniformes tient dans un petit puits, si bien que seules de modestes quantités de cellules et de milieu sont nécessaires pour les expériences.
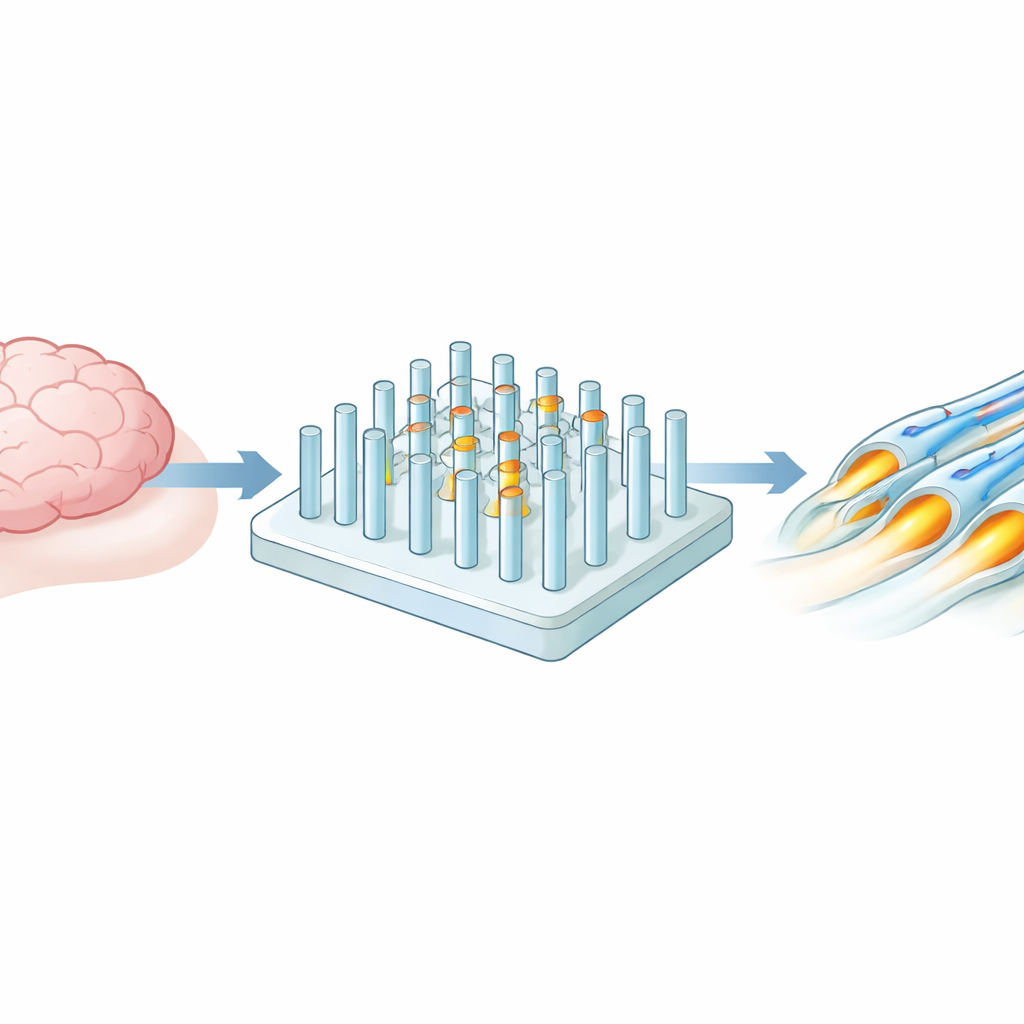
Amener les cellules cérébrales à enrouler les piliers
Ensuite, les chercheurs ont placé des oligodendrocytes — des cellules spécialisées du cerveau qui entourent normalement les fibres nerveuses de myéline — sur ces réseaux de piliers. Sur deux semaines, ils ont observé la croissance des cellules, leurs changements et l’émission de longs prolongements qui se sont enroulés autour des piliers. Grâce à des microscopes avancés, incluant l’imagerie confocale 3D et la microscopie électronique, ils ont observé la formation de multiples couches compactes d’isolation autour de nombreux poteaux en gel, très similaires à la myéline naturelle du cerveau. Plus de la moitié des piliers présentaient des enroulements multicouches, et l’épaisseur de la gaine isolante correspondait étroitement au nombre de tours effectués par la cellule, confirmant qu’une simple coloration fluorescente pouvait remplacer de manière fiable des contrôles ultrastructuraux plus laborieux.
Comment la forme, l’espacement et la souplesse orientent l’isolation
Parce que la plateforme est très modulable, l’équipe a pu sonder systématiquement quelles caractéristiques physiques comptent le plus. Ils ont fait varier la largeur et l’espacement des piliers pour refléter la diversité des tailles de fibres nerveuses dans le tissu cérébral réel. Les piliers plus épais étaient enveloppés plus souvent et de façon plus complète, reflétant la préférence d’isolation observée pour les fibres nerveuses plus larges dans les cerveaux vivants. Lorsque les piliers étaient très fins mais trop rapprochés, chaque cellule avait plus de cibles potentielles qu’elle ne pouvait en traiter, et l’efficacité de l’enroulement diminuait. Le rapport entre la taille du pilier et l’épaisseur de la gaine — le soi‑disant g‑ratio utilisé en neurosciences — se situait dans la fourchette observée dans le système nerveux central sain, suggérant que le système artificiel capture des aspects clés du design naturel.
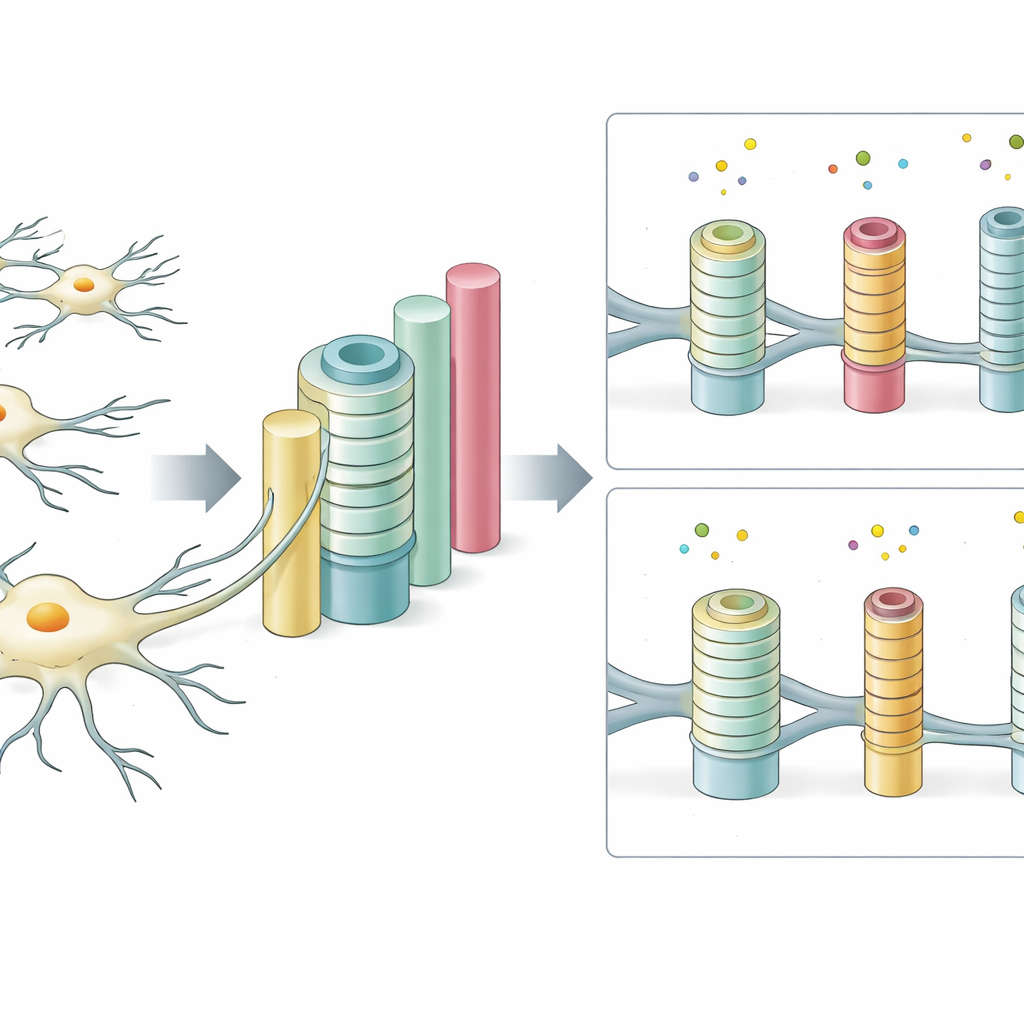
La texture et la surface du paysage changent le comportement cellulaire
Au‑delà de la géométrie, la « sensation » de l’environnement a aussi fortement influé sur la capacité des cellules à former une gaine. Sur des piliers très mous imitant le tissu cérébral mou, un certain enroulement se produisait, mais il était réduit pour certaines tailles de piliers. À mesure que les piliers devenaient plus fermes, l’enroulement augmentait généralement, en particulier sur les poteaux les plus larges. Les chercheurs ont également modifié les molécules recouvrant la surface des piliers. Un revêtement à la laminine, un composant naturel de la matrice extracellulaire cérébrale, a favorisé l’enroulement, tandis que la fibronectine a modifié le nombre de piliers que chaque cellule pouvait entourer complètement. En combinant des variations de souplesse et de chimie de surface, ils ont montré que ces deux facteurs contrôlent conjointement le nombre de piliers entièrement isolés, soulignant la sensibilité de ces cellules à des indices physiques et chimiques subtils.
Mettre au jour les effets des médicaments — et les faux espoirs
L’équipe a ensuite transformé le système en banc d’essai pour des médicaments potentiels. Ils ont appliqué plusieurs composés proposés antérieurement pour améliorer la réparation de la myéline, ainsi qu’un composé connu pour interférer avec ce processus. La plateforme a détecté des augmentations nettes d’enroulement pour des candidats « pro‑myélinisants » et des diminutions dépendantes de la dose pour l’inhibiteur. Fait crucial, la puissance apparente de certains médicaments dépendait de la rigidité des piliers. Sur des poteaux plus rigides, les médicaments semblaient plus efficaces ; sur des piliers plus mous, proches du cerveau, leurs bénéfices étaient moindres. Cela suggère que d’anciens modèles de laboratoire excessivement rigides ont pu exagérer la promesse de certains composés, ce qui aide à expliquer pourquoi certains ont échoué en essais cliniques malgré des données préliminaires encourageantes.
Intégrer la biologie humaine
Pour rendre le système plus pertinent pour les patients, les chercheurs ont montré qu’il fonctionne non seulement avec des cellules de rongeurs, mais aussi avec des cellules humaines dérivées de tissu fœtal et de cellules souches humaines. Ces oligodendrocytes humains ont étendu de longs prolongements complexes et enroulé les piliers en gel, et pour les cellules dérivées de cellules souches, ils ont même formé des gaines compactes et multicouches. Cela signifie que la plateforme peut être associée aux technologies modernes de cellules souches, y compris des lignées spécifiques aux patients, pour modéliser les maladies humaines affectant la myéline et rechercher des traitements personnalisés.
Ce que cela signifie pour les traitements futurs
En termes simples, ce travail fournit un terrain de jeu miniature et réaliste où les cellules formant l’isolation peuvent interagir avec des « faux nerfs » proches de la réalité. Parce que la taille, l’espacement, la souplesse et la surface des piliers peuvent tous être contrôlés, les scientifiques peuvent disséquer comment chaque caractéristique influence la réparation de la myéline et comment les médicaments potentiels se comportent réellement dans un environnement proche du cerveau. En réduisant les résultats trompeurs issus de systèmes de laboratoire trop rigides ou plats et en étant compatible avec des cellules humaines, cette plateforme de piliers ajustables pourrait accélérer la découverte de thérapies plus fiables pour la sclérose en plaques et les troubles apparentés, rapprochant la perspective de restaurer la gaine nerveuse endommagée de la réalité.
Citation: Lasli, S., Vinel, C., Agrawal, A. et al. Tunable hydrogel-based micropillar arrays for myelination studies. Nat Methods 23, 854–864 (2026). https://doi.org/10.1038/s41592-026-03048-3
Mots-clés: myélinisation, micropiliers en hydrogel, oligodendrocytes, mécanobiologie, sclérose en plaques