Clear Sky Science · nl
Oligosaccharide in moedermelk bemiddelt mutualisme tussen Escherichia coli en Bifidobacterium bifidum
Waarom melksuikers voor zuigelingen ertoe doen
Ouders horen vaak dat “borstvoeding goed is voor het microbioom”, maar wat dat precies betekent kan vaag blijven. Deze studie kijkt achter het gordijn en laat zien hoe specifieke suikers in moedermelk twee veelvoorkomende darmbacteriën, Escherichia coli en Bifidobacterium bifidum, helpen samenwerken in plaats van concurreren. Door baby’s en hun moeders het eerste levensjaar te volgen en vervolgens cruciale interacties in het laboratorium na te bootsen, onthullen de auteurs een verrassend verhaal: melksuikers voeden niet alleen vriendelijke microben, ze kunnen ook een fijne samenwerking choreograferen die potentiële probleemgevallen van E. coli in toom houdt.
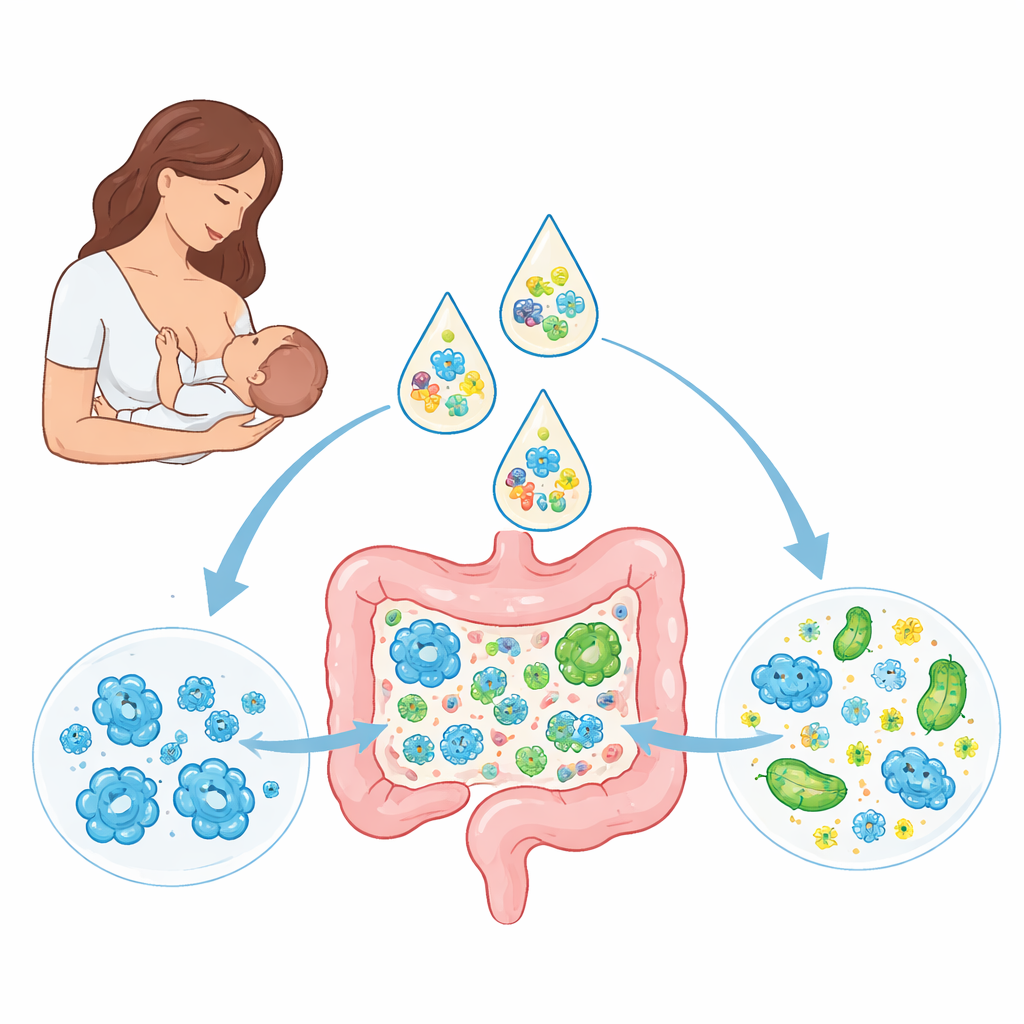
Vroege gasten in de darm van de baby
De onderzoekers volgden 41 gezonde, voldragen Nederlandse zuigelingen die aanvankelijk allemaal exclusief borstvoeding kregen, plus 30 van hun moeders. Met diepgaande DNA-sequencing van stoelmonsters op verschillende leeftijden brachten ze in kaart welke microben aanwezig waren en hoe de samenstelling in de loop van de tijd veranderde. Zoals verwacht waren soorten van Bifidobacterium dominant in veel borstgevoede zuigelingen en werden ze vaak gedeeld tussen moeders en zuigelingen, wat wijst op directe overdracht binnen gezinnen. E. coli, een lid van de Enterobacteriaceae‑familie dat bij overgroei ziekte kan veroorzaken, verscheen bij de meeste zuigelingen maar op lage niveaus. Interessant was dat de E. coli‑stammen bij baby's niet overeenkwamen met die van hun moeders, wat suggereert dat deze bacteriën meestal uit andere omgevingsbronnen komen maar maandenlang kunnen aanblijven eenmaal gevestigd.
Patronen van co‑existentie, geen oorlog
Om te testen hoe individuele soorten de bredere gemeenschap vormen, bouwde het team een nieuwe computationele pijplijn genaamd MAJIC. In plaats van alleen te kijken wie aanwezig is, vergelijkt MAJIC hele gemeenschappen wanneer een bepaalde soort aanwezig is versus wanneer deze afwezig is, en vraagt of die soort de mogelijke gemeenschapsstaten vernauwt of verruimt. Bij zeer jonge zuigelingen waren Bifidobacterium‑soorten overvloedig maar gedroegen ze zich als “achtergrondspelers”: het verliezen van één soort veranderde niet ingrijpend wie er nog kon leven, wat impliceert dat andere microben in kunnen springen en vergelijkbare rollen vervullen. Gedurende het eerste jaar vonden de auteurs geen signaal dat veelvoorkomende Bifidobacterium‑soorten E. coli onderdrukten. In plaats van een directe strijd leek hun frequente co‑voorkomen meer op vreedzaam delen van een habitat die gevormd wordt door dezelfde voedselbron—melksuikers.
Inzoomen op stammen en genen
Door honderden bacteriële genomen uit de monsters te reconstrueren, konden de onderzoekers niet alleen soorten onderscheiden maar ook individuele stammen en hun genetische variatie. Bifidobacterium longum subspecies longum werd bijvoorbeeld vaak gedeeld tussen moeders en zuigelingen en bleef in de loop van de tijd in hetzelfde kind aanwezig, wat wijst op sterke aanpassing aan de zuigelingendarm. B. bifidum toonde bijzonder strakke genetische beperkingen in sleutelgenen voor suikermetabolisme, alsof het fijn is afgestemd op zijn niche. E. coli daarentegen vertoonde hoge microdiversiteit, met meerdere stammen die binnen een zuigeling coëxisteerden en minder bewijs voor strikte gast‑specifieke afstemming. Ondanks deze verschillen droegen zowel Bifidobacterium als E. coli genensets gekoppeld aan enzymen die complexe koolhydraten afbreken, wat wijst op gedeelde selectie om melksuikers efficiënt te grijpen en te gebruiken.
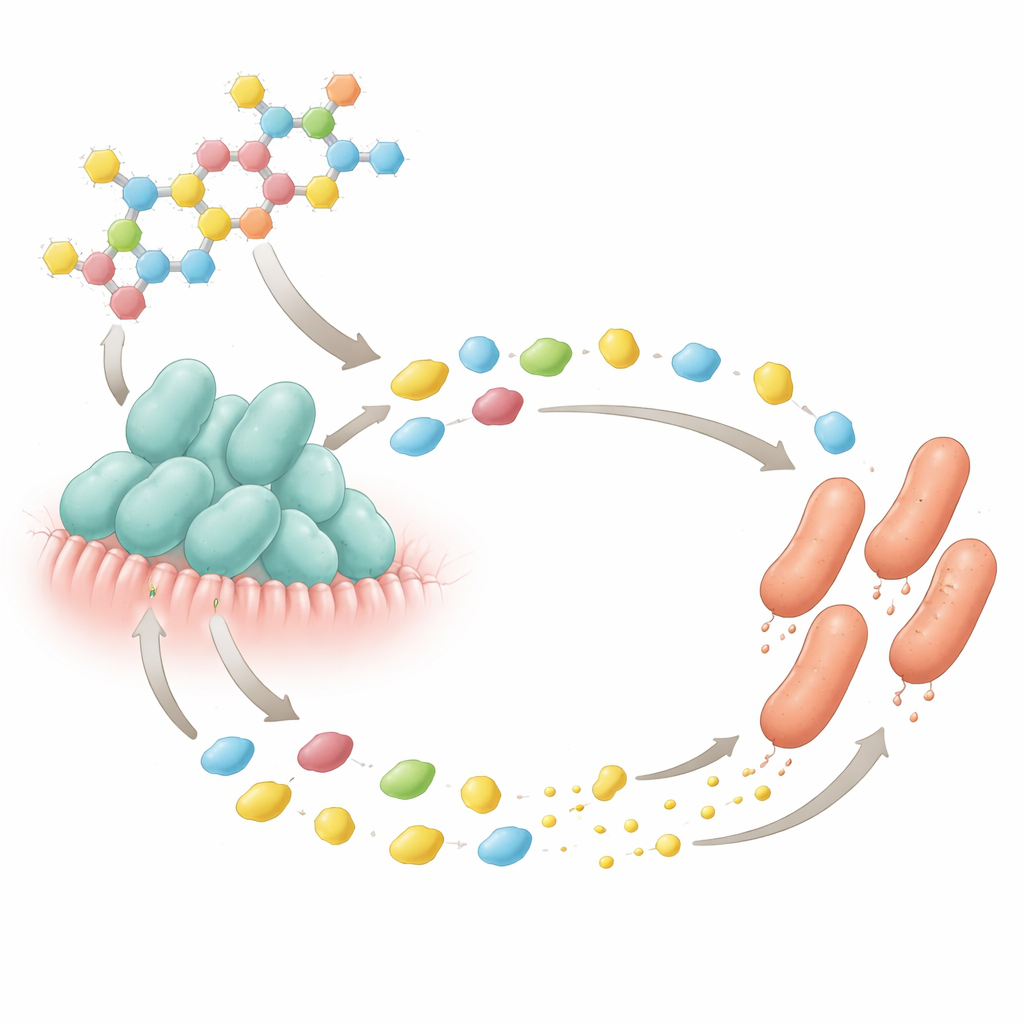
Een microscopische suiker‑voor‑nutriënt ruil
De meest opvallende resultaten kwamen uit laboratoriumexperimenten die een belangrijke melksuikerinteractie nabouwden. De auteurs concentreerden zich op 2′‑fucosyllactose, een van de meest voorkomende complexe suikers in moedermelk. B. bifidum‑isolaten uit stoelmonsters konden deze suiker in eenvoudige bouwstenen knippen, maar hadden het aminozuur cysteïne nodig om te groeien. E. coli kon de intacte suiker niet verteren maar floreerde op de vrijgekomen eenvoudige suikers. Wanneer de twee microben samen werden gekweekt in een medium met 2′‑fucosyllactose maar zonder toegevoegde cysteïne, groeiden beide goed—terwijl geen van beide onder die omstandigheden alleen kon gedijen. Verdere tests met een mutant E. coli die geen cysteïne kan maken, toonden dat normale E. coli deze ontbrekende voedingsstof aan B. bifidum leverde, terwijl B. bifidum de eenvoudige suikers verschafte die E. coli aandreven. Dit onthulde een nauwe wederzijdse uitwisseling: een mutualisme bemiddeld door een melksuiker.
Wat dit betekent voor de gezondheid van zuigelingen
Voor niet‑specialisten is de kernboodschap dat moedermelk meer doet dan “de baby voeden” of zelfs alleen “goede bacteriën voeden.” De complexe suikers kunnen samenwerkingsrelaties tussen verschillende microben tot stand brengen die hulpbronnen delen. In dit geval vormen B. bifidum en E. coli een suiker‑voor‑nutriënt‑ruil die kan helpen E. coli aanwezig maar niet dominant te houden, terwijl ze een stabiele, efficiënte gemeenschap ondersteunen die melk omzet in nuttige metabolieten voor de zuigeling. Het werk suggereert dat darmecosystemen in vroege levensfase worden gevormd door zowel concurrentie om eenvoudige door de gast geproduceerde suikers zoals lactose als door cross‑feeding op melkoligosacchariden. Begrijpen van deze onzichtbare onderhandelingen kan leiden tot betere zuigelingenvoedingen, probiotica of voedingsaanpassingen die gericht zijn op het sturen van het microbioom van zuigelingen naar een stabiele, gezondheidbevorderende staat.
Bronvermelding: Seki, D., Pollak, S., Kujawska, M. et al. Human milk oligosaccharide mediates mutualism between Escherichia coli and Bifidobacterium bifidum. Nat Commun 17, 3489 (2026). https://doi.org/10.1038/s41467-026-71764-7
Trefwoorden: microbioom van zuigelingen, oligosacchariden in moedermelk, Bifidobacterium, Escherichia coli, cross‑feeding