Clear Sky Science · fr
Les oligosaccharides du lait humain médiatisent le mutualisme entre Escherichia coli et Bifidobacterium bifidum
Pourquoi les sucres du lait infantile comptent
Les parents entendent souvent que « l’allaitement est bon pour le microbiome », mais ce que cela signifie réellement peut sembler mystérieux. Cette étude lève un coin du voile pour montrer comment des sucres spécifiques du lait humain aident deux bactéries intestinales communes, Escherichia coli et Bifidobacterium bifidum, à coopérer plutôt qu’à se concurrencer. En suivant des bébés et leurs mères pendant la première année de vie, puis en recréant des interactions clés en laboratoire, les auteurs révèlent une histoire surprenante : les sucres du lait non seulement nourrissent des microbes bénéfiques, mais ils peuvent aussi orchestrer un partenariat délicat qui maintient E. coli, potentiellement problématique, sous contrôle.
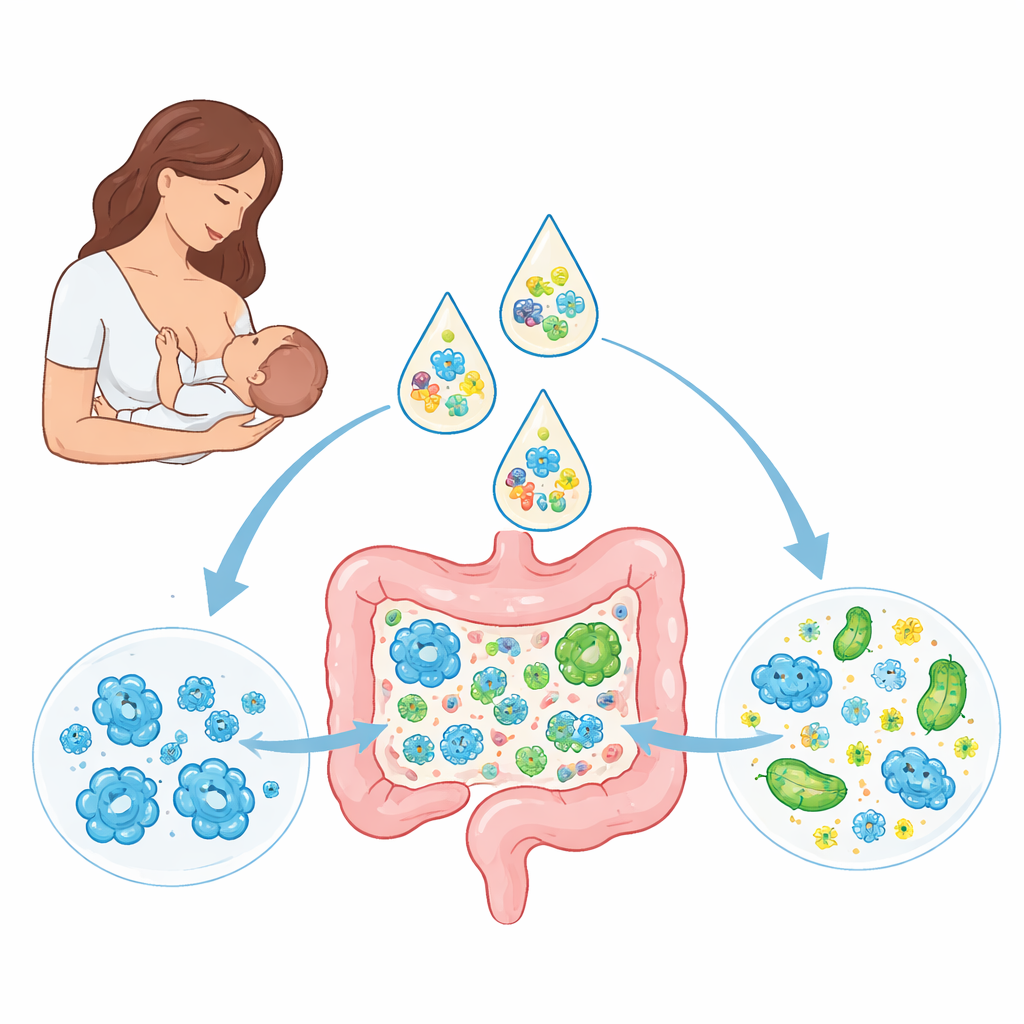
Premiers occupants de l’intestin du nourrisson
Les chercheurs ont suivi 41 nourrissons néerlandais sains et nés à terme, tous initialement exclusivement allaités, ainsi que 30 de leurs mères. Grâce à un séquençage profond de l’ADN des échantillons de selles à plusieurs âges, ils ont cartographié les microbes présents et l’évolution des communautés au fil du temps. Comme prévu, des espèces de Bifidobacterium dominaient chez de nombreux bébés allaités et étaient souvent partagées entre mères et nourrissons, ce qui suggère un transfert direct au sein des familles. E. coli, membre de la famille des Enterobacteriaceae et pouvant causer des maladies en cas de prolifération excessive, apparaissait chez la plupart des nourrissons mais à de faibles niveaux. Fait intéressant, les souches d’E. coli chez les bébés ne correspondaient pas à celles de leurs mères, ce qui indique que ces bactéries proviennent généralement d’autres sources environnementales mais peuvent persister pendant des mois une fois établies.
Des schémas de coexistence, pas de guerre
Pour tester comment des espèces individuelles façonnent la communauté globale, l’équipe a développé un nouveau pipeline computationnel nommé MAJIC. Plutôt que de ne regarder que la présence, MAJIC compare des communautés entières lorsque telle espèce est présente versus absente, pour déterminer si cette espèce tend à restreindre ou élargir les états communautaires possibles. Chez les très jeunes nourrissons, les espèces de Bifidobacterium étaient abondantes mais se comportaient comme des « joueurs de fond » : la perte d’une espèce ne modifiait pas drastiquement les autres habitants possibles, ce qui implique que d’autres microbes pouvaient remplacer leurs fonctions. Sur la première année, les auteurs n’ont trouvé aucun signal indiquant que les Bifidobacterium communes supprimaient E. coli. Plutôt qu’un affrontement direct, leur cooccurrence fréquente ressemblait davantage à un partage pacifique d’un habitat façonné par la même réserve alimentaire — les sucres du lait.
Analyse fine des souches et des gènes
En reconstituant des centaines de génomes bactériens à partir des échantillons, les chercheurs ont pu distinguer non seulement les espèces mais les souches individuelles et leur variation génétique. Bifidobacterium longum sous‑espèce longum, par exemple, était souvent partagé entre mères et nourrissons et persistait dans le même enfant, suggérant une forte adaptation à l’intestin infantile. B. bifidum présentait des contraintes génétiques particulièrement marquées sur des gènes clés de métabolisme des sucres, comme finement ajustée à sa niche. E. coli, en revanche, affichait une microdiversité élevée, avec plusieurs souches coexistant chez un même nourrisson et moins de preuves d’un ajustement strict spécifique à l’hôte. Malgré ces différences, Bifidobacterium et E. coli possédaient des ensembles de gènes associés à des enzymes capables de dégrader des glucides complexes, ce qui laisse entrevoir une pression partagée pour capturer et utiliser efficacement les sucres d’origine lactée.
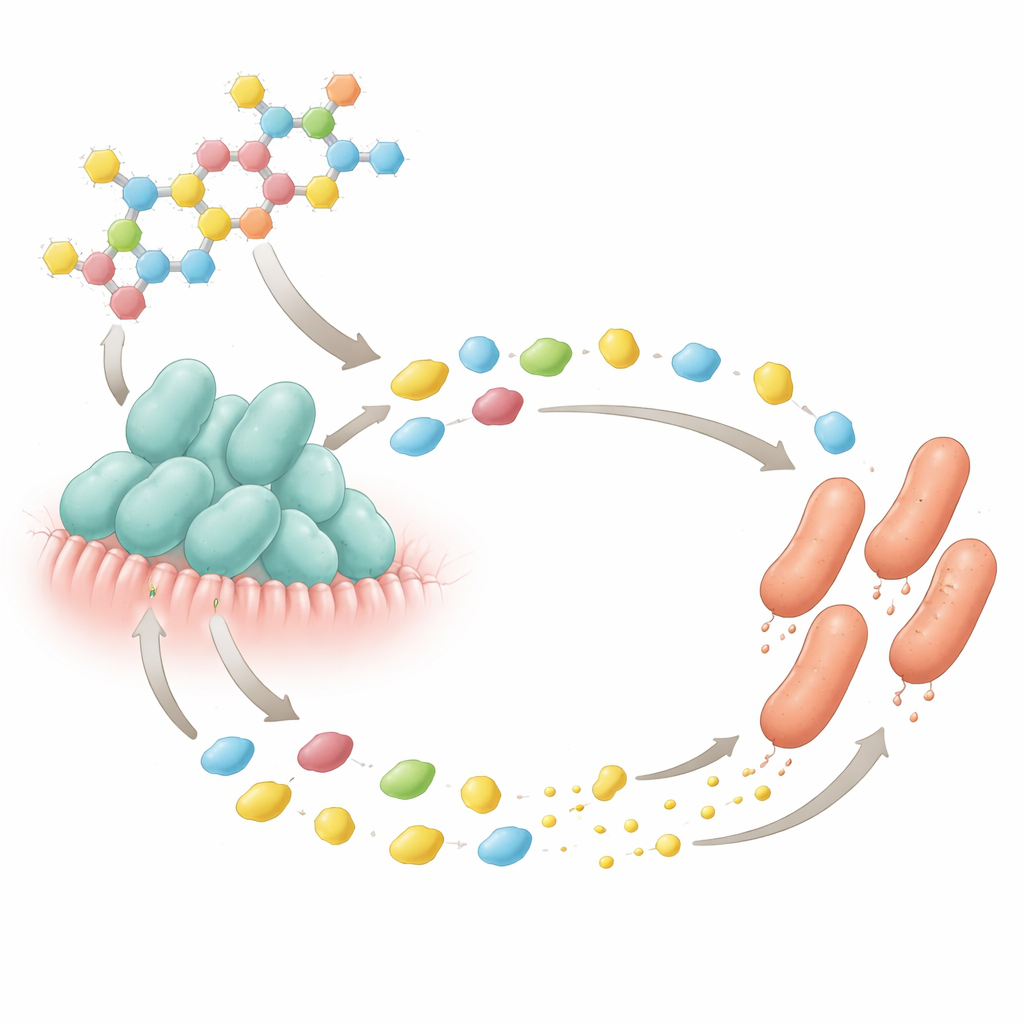
Un échange microscopique sucre‑contre‑nutriment
Les résultats les plus frappants proviennent d’expériences en laboratoire qui ont recréé une interaction clé autour d’un sucre du lait. Les auteurs se sont concentrés sur le 2′‑fucosyllactose, l’un des oligosaccharides les plus abondants du lait humain. Des isolats de B. bifidum issus de selles infantiles pouvaient cliver ce sucre en unités simples mais avaient besoin de l’acide aminé cystéine pour croître. E. coli ne pouvait pas digérer le sucre intact mais prospérait sur les sucres simples libérés. Lorsque les deux microbes ont été cultivés ensemble dans un milieu contenant du 2′‑fucosyllactose sans cystéine ajoutée, les deux ont bien crû — alors qu’aucun d’eux n’aurait pu prospérer seul dans ces conditions. Des tests supplémentaires avec une souche mutante d’E. coli incapable de synthétiser la cystéine ont montré que l’E. coli normal fournissait ce nutriment manquant à B. bifidum, tandis que B. bifidum fournissait les sucres simples qui alimentaient E. coli. Cela révèle un échange bilatéral étroit : un mutualisme médié par un sucre du lait humain.
Ce que cela signifie pour la santé infantile
Pour les non‑spécialistes, le message clé est que le lait maternel fait plus que « nourrir le bébé » ou même « nourrir les bonnes bactéries ». Ses sucres complexes peuvent instaurer des relations coopératives entre microbes différents qui se partagent les ressources. Dans ce cas, B. bifidum et E. coli forment un troc sucre‑contre‑nutriment qui peut aider à maintenir E. coli présent sans le laisser dominer, tout en soutenant une communauté stable et efficace qui transforme le lait en métabolites utiles pour le nourrisson. Les travaux suggèrent que les écosystèmes intestinaux précoces sont façonnés à la fois par la concurrence pour des sucres simples d’origine hôte comme le lactose et par le partage croisé autour des oligosaccharides du lait. Comprendre ces accords invisibles pourrait orienter de meilleurs laits infantiles, probiotiques ou ajustements alimentaires visant à diriger le microbiome infantile vers un état stable et favorable à la santé.
Citation: Seki, D., Pollak, S., Kujawska, M. et al. Human milk oligosaccharide mediates mutualism between Escherichia coli and Bifidobacterium bifidum. Nat Commun 17, 3489 (2026). https://doi.org/10.1038/s41467-026-71764-7
Mots-clés: microbiote intestinal du nourrisson, oligosaccharides du lait humain, Bifidobacterium, Escherichia coli, partage croisé