Clear Sky Science · de
Humanes Milch-Oligosaccharid vermittelt Mutualismus zwischen Escherichia coli und Bifidobacterium bifidum
Warum Säuglingsmilch‑Zucker wichtig sind
Eltern hören oft, dass „Stillen gut fürs Mikrobiom ist“, aber was genau das bedeutet, bleibt häufig unklar. Diese Studie blickt hinter den Vorhang und zeigt, wie bestimmte Zucker in menschlicher Milch zwei häufige Darmbakterien, Escherichia coli und Bifidobacterium bifidum, zur Kooperation statt zur Konkurrenz bewegen. Indem die Autoren Mütter und Babys im ersten Lebensjahr begleiteten und dann zentrale Wechselwirkungen im Labor nachstellten, zeichnen sie eine überraschende Geschichte nach: Milchzucker nähren nicht nur freundliche Mikroben, sie können auch eine feine Partnerschaft choreografieren, die potenziell problematisches E. coli in Schach hält.
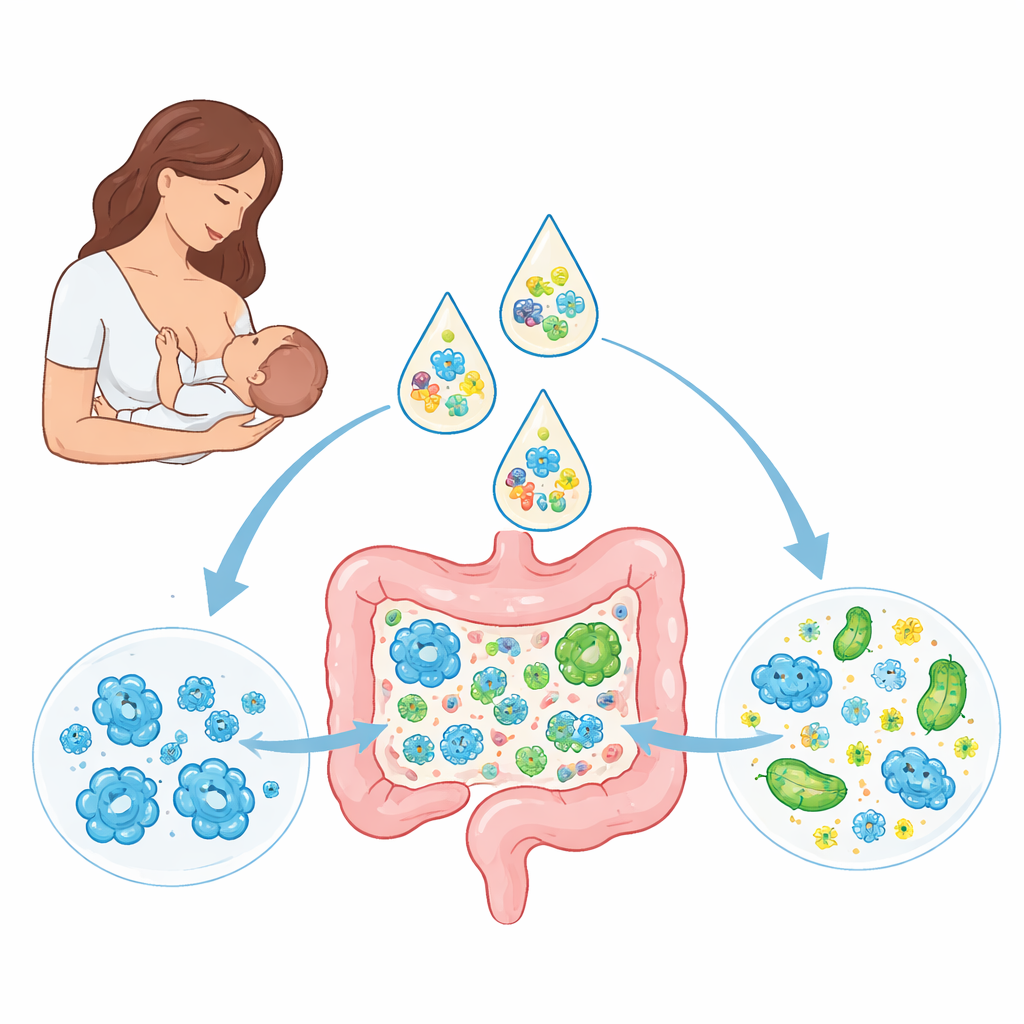
Frühe Gäste im Säuglingsdarm
Die Forschenden beobachteten 41 gesunde, termingerecht geborene niederländische Säuglinge, die anfangs alle ausschließlich gestillt wurden, sowie 30 ihrer Mütter. Mittels tiefgehender DNA-Sequenzierung von Stuhlproben zu mehreren Zeitpunkten kartierten sie, welche Mikroben vorhanden waren und wie sich die Gemeinschaften über die Zeit veränderten. Wie erwartet dominierten in vielen gestillten Babys Arten der Gattung Bifidobacterium und wurden oft zwischen Müttern und Säuglingen geteilt, was auf eine direkte Übertragung innerhalb der Familien hindeutet. E. coli, ein Mitglied der Enterobacteriaceae, das bei Überwucherung krankheitsverursachend sein kann, trat bei den meisten Säuglingen auf, jedoch in niedrigen Mengen. Interessanterweise stimmten die E.-coli-Stämme in Babys nicht mit denen ihrer Mütter überein, was nahelegt, dass diese Bakterien meist aus anderen Umweltquellen stammen, sich nach Etablierung aber über Monate halten können.
Muster des Zusammenlebens, keine Kriegsführung
Um zu prüfen, wie einzelne Arten die gesamte Gemeinschaft prägen, entwickelten die Forschenden eine neue Rechenpipeline namens MAJIC. Anstatt nur zu schauen, wer vorhanden ist, vergleicht MAJIC ganze Gemeinschaften, wenn eine bestimmte Art vorhanden ist versus wenn sie fehlt, und fragt, ob diese Art tendenziell die möglichen Gemeinschaftszustände einschränkt oder erweitert. Bei sehr jungen Säuglingen waren Bifidobacterium-Arten zwar häufig, verhielten sich aber wie „Nebenakteure“: der Verlust einer Art veränderte nicht drastisch, welche anderen Organismen dort leben konnten, was darauf hindeutet, dass andere Mikroben ähnliche Rollen übernehmen könnten. Im Verlauf des ersten Jahres fanden die Autoren keinen Hinweis darauf, dass gängige Bifidobacterium-Arten E. coli unterdrücken. Ihre häufige Koexistenz wirkte eher wie friedliches Teilen eines Lebensraums, der durch dieselbe Nahrungsquelle — Milchzucker — geformt wird, als wie ein direkter Kampf.
Genauer Blick auf Stämme und Gene
Durch die Rekonstruktion hunderter bakterieller Genome aus den Proben konnten die Forschenden nicht nur Arten, sondern einzelne Stämme und deren genetische Variation unterscheiden. Bifidobacterium longum subspecies longum etwa wurde oft zwischen Müttern und Säuglingen geteilt und blieb im selben Kind über die Zeit bestehen, was auf eine starke Anpassung an den Säuglingsdarm hindeutet. B. bifidum zeigte besonders enge genetische Einschränkungen in Schlüsselgenen zur Zuckerverarbeitung, als wäre es fein auf seine Nische abgestimmt. E. coli dagegen wies hohe Mikrodifferenzierung auf, mit mehreren koexistierenden Stämmen innerhalb eines Säuglings und weniger Hinweisen auf strikte Wirts-spezifische Anpassung. Trotz dieser Unterschiede trugen sowohl Bifidobacterium als auch E. coli Genpakete, die mit Enzymen zur Aufspaltung komplexer Kohlenhydrate verknüpft sind, was auf gemeinsamen Selektionsdruck hindeutet, milchabgeleitete Zucker effizient zu erfassen und zu nutzen.
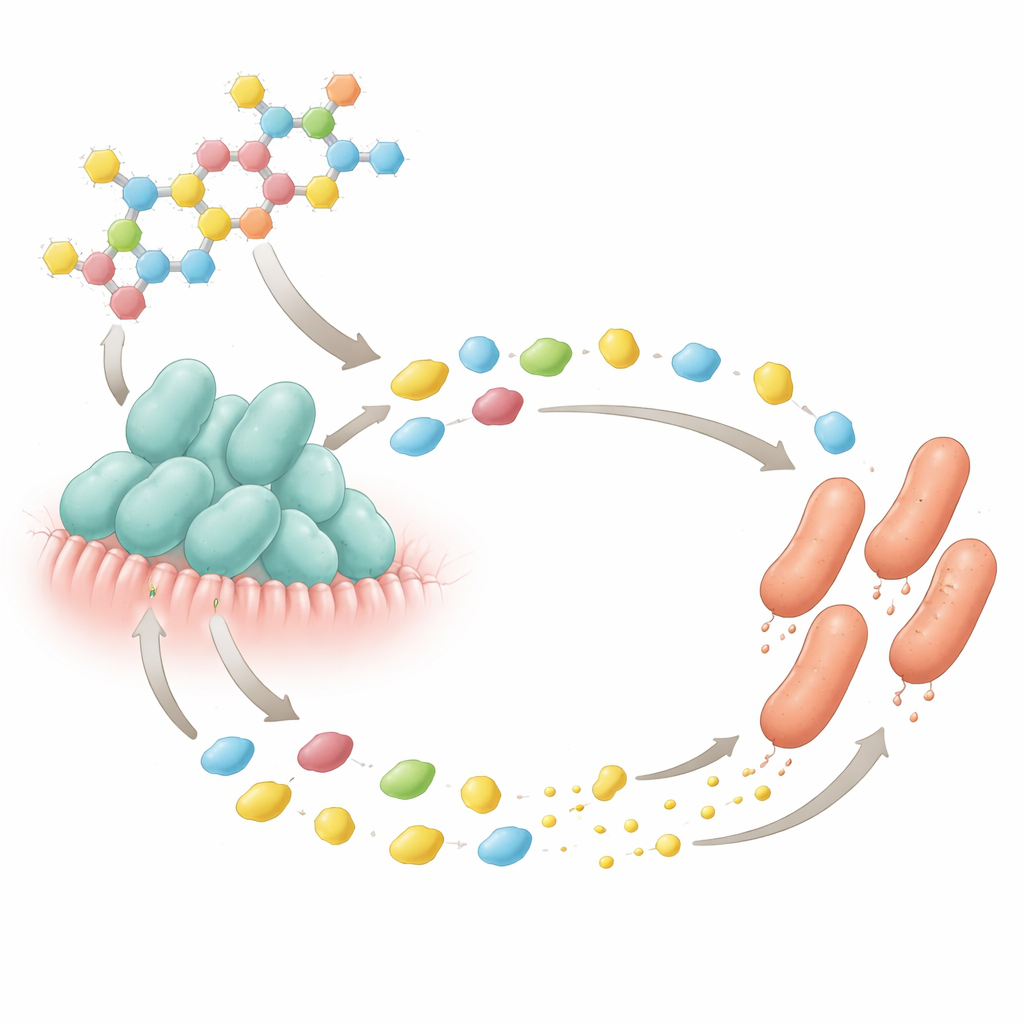
Ein mikroskopischer Zucker‑gegen‑Nährstoff‑Deal
Die auffälligsten Ergebnisse stammen aus Laborversuchen, die eine zentrale Milchzucker‑Interaktion nachstellten. Die Autoren konzentrierten sich auf 2′-Fucosyllactose, einen der häufigsten komplexen Zucker in menschlicher Milch. B. bifidum-Isolate aus Stuhlproben von Säuglingen konnten diesen Zucker in einfache Bausteine zerlegen, benötigten aber die Aminosäure Cystein zum Wachsen. E. coli konnte den intakten Zucker nicht verdauen, gedieh jedoch auf den freigesetzten Einfachzuckern. Wurden die beiden Mikroben zusammen in einem Medium mit 2′-Fucosyllactose, aber ohne zugesetztes Cystein kultiviert, wuchsen beide gut — allein unter diesen Bedingungen konnte keiner von beiden gedeihen. Weitere Tests mit einem E.-coli-Mutanten, der kein Cystein synthetisieren kann, zeigten, dass normales E. coli dieses fehlende Nährstoff lieferte, während B. bifidum die einfachen Zucker bereitstellte, die E. coli antrieben. Das offenbart einen engen zweiseitigen Austausch: einen Mutualismus, vermittelt durch einen Milchzucker.
Was das für die Säuglingsgesundheit bedeutet
Für Nichtfachleute ist die Kernaussage: Muttermilch bewirkt mehr, als nur „das Baby zu ernähren“ oder sogar nur „gute Bakterien zu füttern“. Ihre komplexen Zucker können kooperative Beziehungen zwischen verschiedenen Mikroben etablieren, die Ressourcen teilen. In diesem Fall bilden B. bifidum und E. coli einen Zucker‑gegen‑Nährstoff‑Tausch, der helfen kann, E. coli präsent, aber nicht dominant zu halten, und zugleich eine stabile, effiziente Gemeinschaft fördert, die Milch in nützliche Metabolite für das Kind umwandelt. Die Arbeit deutet darauf hin, dass frühkindliche Darmökosysteme sowohl durch Konkurrenz um einfache, vom Wirt abgeleitete Zucker wie Laktose als auch durch Cross‑Feeding auf Milch‑Oligosacchariden geprägt werden. Das Verständnis dieser unsichtbaren Abkommen könnte dabei helfen, bessere Säuglingsnahrungen, Probiotika oder Ernährungsanpassungen zu entwickeln, die das Säuglingsmikrobiom in einen stabilen, gesundheitsfördernden Zustand lenken.
Zitation: Seki, D., Pollak, S., Kujawska, M. et al. Human milk oligosaccharide mediates mutualism between Escherichia coli and Bifidobacterium bifidum. Nat Commun 17, 3489 (2026). https://doi.org/10.1038/s41467-026-71764-7
Schlüsselwörter: Säuglings-Darmmikrobiom, humanes Milch-Oligosaccharide, Bifidobacterium, Escherichia coli, Cross-Feeding