Clear Sky Science · it
Gli oligosaccaridi del latte umano mediano il mutualismo tra Escherichia coli e Bifidobacterium bifidum
Perché gli zuccheri del latte materno sono importanti
I genitori spesso sentono dire che “l’allattamento al seno fa bene al microbioma”, ma cosa significhi esattamente può rimanere un mistero. Questo studio solleva il velo per mostrare come zuccheri specifici del latte umano aiutino due batteri comuni dell’intestino, Escherichia coli e Bifidobacterium bifidum, a cooperare invece che competere. Seguendo neonati e madri nel primo anno di vita e poi ricreando in laboratorio le interazioni chiave, gli autori rivelano una storia sorprendente: gli zuccheri del latte non solo nutrono i microbi amici, ma possono anche orchestrare una partnership delicata che mantiene sotto controllo E. coli, potenzialmente problematico.
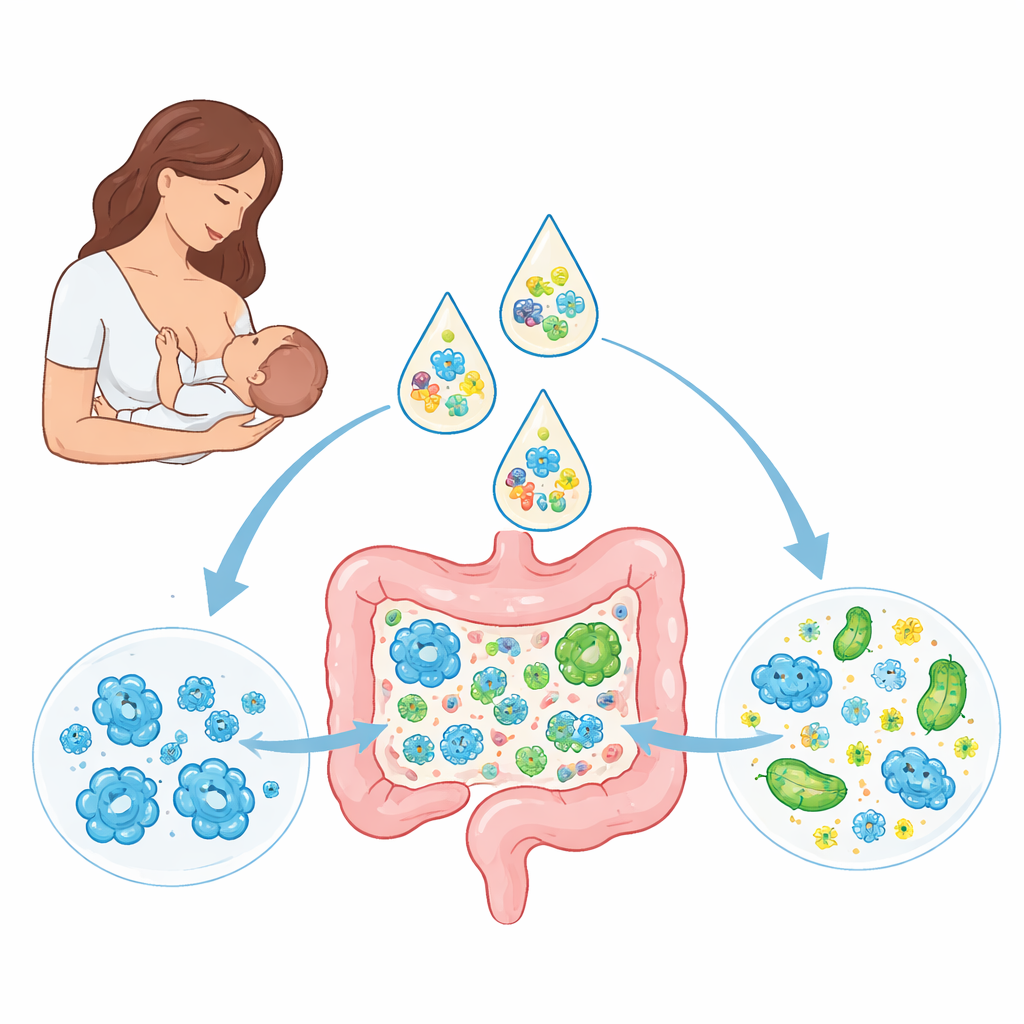
Ospiti precoci nell’intestino del neonato
I ricercatori hanno seguito 41 neonati olandesi sani e a termine, tutti inizialmente esclusivamente allattati al seno, più 30 delle loro madri. Con il sequenziamento profondo del DNA delle feci a diverse età hanno mappato quali microbi erano presenti e come le comunità cambiavano nel tempo. Come previsto, specie di Bifidobacterium dominavano in molti bambini allattati al seno ed erano spesso condivise tra madri e figli, indicando un trasferimento diretto all’interno delle famiglie. E. coli, membro della famiglia Enterobacteriaceae che può causare malattie se sovraccresce, è comparso nella maggior parte dei neonati ma a livelli bassi. Interessante, gli ceppi di E. coli nei neonati non corrispondevano a quelli delle madri, suggerendo che questi batteri arrivino solitamente da altre fonti ambientali ma possano persistere per mesi una volta stabiliti.
Modelli di coesistenza, non di guerra
Per capire come singole specie modellino la comunità più ampia, il team ha costruito una nuova pipeline computazionale chiamata MAJIC. Invece di guardare solo a chi è presente, MAJIC confronta intere comunità quando una data specie è presente rispetto a quando è assente, chiedendosi se quella specie tenda a restringere o ampliare gli stati possibili della comunità. Nei neonati molto giovani, le specie di Bifidobacterium erano abbondanti ma si comportavano come “attori di sfondo”: la perdita di una non cambiava drasticamente chi potesse vivere lì, implicando che altri microbi potessero sostituirle e svolgere ruoli simili. Nel corso del primo anno gli autori non hanno trovato segnali che le comuni specie di Bifidobacterium sopprimessero E. coli. Più che una battaglia diretta, la loro frequente co‑occorrenza sembrava piuttosto una condivisione tranquilla di un habitat plasmato dalla stessa fonte di cibo—gli zuccheri del latte.
Zoom su ceppi e geni
Ricostruendo centinaia di genomi batterici dai campioni, i ricercatori hanno potuto distinguere non solo le specie ma i singoli ceppi e la loro variazione genetica. Bifidobacterium longum subspecies longum, per esempio, era spesso condiviso tra madri e neonati e persisteva nel tempo nello stesso bambino, suggerendo una forte adattamento all’intestino infantile. B. bifidum mostrava vincoli genetici particolarmente stretti in geni chiave per la gestione degli zuccheri, come se fosse finemente sintonizzato sulla sua nicchia. E. coli, al contrario, mostrava elevata microdiversità, con più ceppi coesistenti all’interno di un neonato e meno evidenze di una sintonizzazione stretta rispetto all’ospite. Nonostante queste differenze, sia Bifidobacterium che E. coli possedevano insiemi di geni associati a enzimi che degradano carboidrati complessi, suggerendo una pressione condivisa a catturare e usare efficacemente gli zuccheri derivati dal latte.
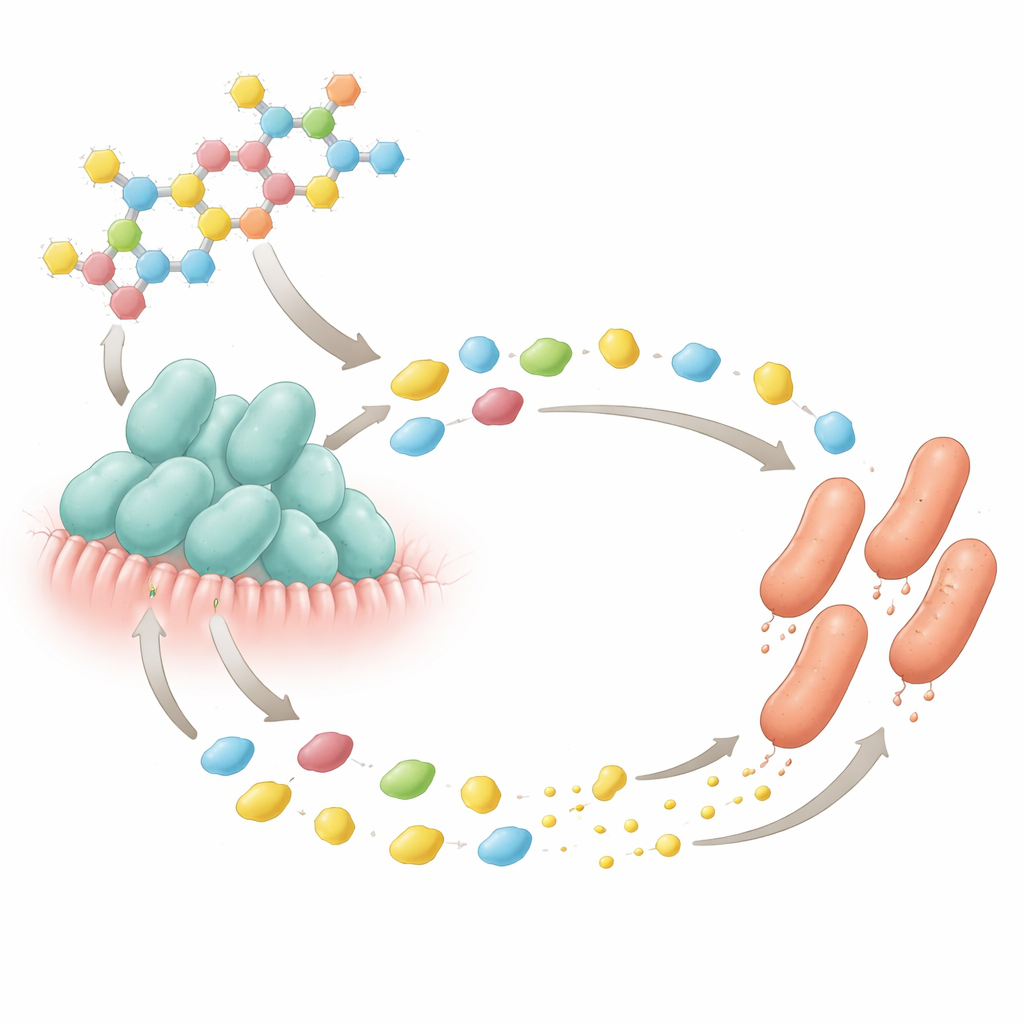
Un patto microscopico zucchero‑per‑nutriente
I risultati più sorprendenti sono venuti dagli esperimenti di laboratorio che hanno ricreato un’interazione chiave con uno zucchero del latte. Gli autori si sono concentrati sulla 2′‑fucosillattosio, uno degli oligosaccaridi più abbondanti nel latte umano. Isolati di B. bifidum da feci infantili riuscivano a tagliare questo zucchero in blocchi semplici ma avevano bisogno dell’aminoacido cisteina per crescere. E. coli non poteva digerire lo zucchero intatto ma prosperava sugli zuccheri semplici rilasciati. Quando i due microbi venivano coltivati insieme in un mezzo contenente 2′‑fucosillattosio ma senza cisteina aggiunta, entrambi crescevano bene—mentre nessuno dei due riusciva a prosperare da solo in quelle condizioni. Test successivi con un ceppo mutante di E. coli incapace di sintetizzare la cisteina hanno dimostrato che l’E. coli normale forniva questo nutriente mancante a B. bifidum, mentre B. bifidum forniva gli zuccheri semplici che alimentavano E. coli. Questo ha rivelato uno scambio bidirezionale stretto: un mutualismo mediato da uno zucchero del latte umano.
Cosa significa per la salute infantile
Per i non specialisti, il messaggio chiave è che il latte materno fa più che “nutrire il bambino” o anche solo “nutrire i batteri buoni”. I suoi zuccheri complessi possono instaurare relazioni cooperative tra diversi microbi che condividono risorse. In questo caso, B. bifidum ed E. coli formano un baratto zucchero‑per‑nutriente che può aiutare a mantenere E. coli presente ma non dominante, sostenendo nello stesso tempo una comunità stabile ed efficiente che trasforma il latte in metaboliti utili per il neonato. Il lavoro suggerisce che gli ecosistemi intestinali precoci sono plasmati sia dalla competizione per zuccheri semplici di origine ospite come il lattosio sia dal cross‑feeding sugli oligosaccaridi del latte. Comprendere questi accordi invisibili potrebbe guidare formule migliori, probiotici o modifiche dietetiche volte a orientare il microbioma infantile verso uno stato stabile e promotore di salute.
Citazione: Seki, D., Pollak, S., Kujawska, M. et al. Human milk oligosaccharide mediates mutualism between Escherichia coli and Bifidobacterium bifidum. Nat Commun 17, 3489 (2026). https://doi.org/10.1038/s41467-026-71764-7
Parole chiave: microbioma intestinale infantile, oligosaccaridi del latte umano, Bifidobacterium, Escherichia coli, cross‑feeding