Clear Sky Science · nl
Kleinste acyclische tricationische molecule met een door bis(fosfine) gestabiliseerde laag-waardige tri-antimoon-eenheid
Waarom dit kleine geladen puzzelstukje ertoe doet
Chemici zijn gefascineerd door moleculen die meerdere positieve ladingsenheden dragen, omdat het samenpersen van zoveel lading in een kleine ruimte ze meestal uit elkaar doet vliegen. Begrijpen hoe je zulke onstabiele soorten kunt temmen helpt onthullen hoe chemische bindingen werkelijk werken en kan de weg openen naar nieuwe typen materialen en katalysatoren. Deze studie beschrijft een recordklein, ketenvormig molecuul opgebouwd uit drie antimoonatomen die samen drie positieve ladingen dragen, plus een even ongebruikelijke negatief geladen partner die het systeem helpt bij elkaar te houden.
Een fragiele drie‑atomige keten bouwen
De meeste bekende sterk geladen moleculen op basis van hoofd-groepelementen vormen ringen of grotere clusters, die hun lading spreiden en intense interne afstoting vermijden. De auteurs wilden iets extremer maken: de kleinst mogelijke open keten van drie gebonden zware atomen die toch meer dan één positieve lading draagt. Ze kozen voor antimoon, een zwaardere verwant van arseen en fosfor, omdat de grotere atomen extra lading beter kunnen verdragen. Door een voorgevormd antimoonfragment zorgvuldig te combineren met een sterk aantrekkend antimoonzout bij zeer lage temperatuur, en de uiteinden van de keten te omsluiten met een lompe “bis(fosfine)” greep, slaagden ze erin een felrood verbinding te isoleren met een rechte-maar-gebogen drievoudige antimooneenheid met een totale lading van plus drie.
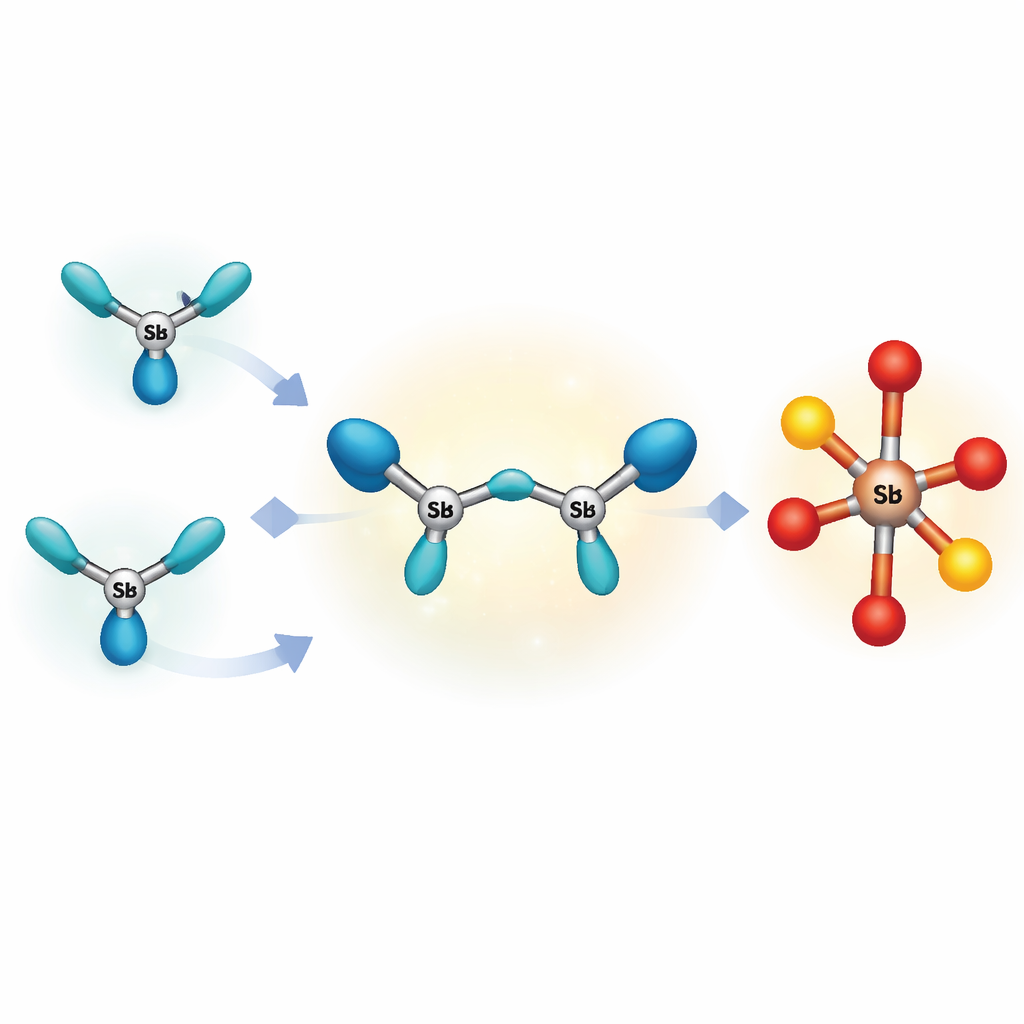
Een vreemde partner aan de negatieve kant
Om drie positieve ladingen te balanceren bevat het kristal ook een zelden gezien anion, of negatief geladen eenheid, gebaseerd op antimoon gebonden aan zuurstof en vier triflaatgroepen. Röntgenmetingen tonen een O–Sb–O ruggegraat met vier extra zuurstofrijke armen, die zeer polaire antimoonzuurstofverbindingen creëren die sterk reactief zijn. Omdat noch de positief geladen keten noch deze ongebruikelijke negatieve partner goed beschermd zijn door lompe omhulling, is het gehele zout thermisch fragiel: zelfs milde verwarming veroorzaakt ontleding, precipitatie van metaalantimoon en het verschijnen van een stabieler product. Dit gedrag betekent dat de oorspronkelijke tri-antimoonketen slechts als een vluchtige momentopname langs het pad naar andere verbindingen bestaat.
Inzicht in de bindingen
Het team gebruikte kwantumchemische berekeningen om in de elektronische structuur van de tri‑antimoonketen te kijken. Ze vonden dat de drie antimoonatomen een gebogen "W"-opstelling vormen, ondersteund door een zwakke driezijdige, vierelektronenbinding langs de keten. Het centrale antimoonatoom draagt twee ongebruikte elektronenparen, terwijl elk buitenste atoom er één draagt. Ladanalyse onthult een opvallende polariteit: de uiteinden van de keten en de fosforatomen van de ondersteunende grepen zijn relatief positief, terwijl het centrale antimoonatoom enigszins negatief is. Deze ongelijkmatige verdeling, samen met de grote omvang van antimoon en de zwakke metaal–metaalbinding, helpt verklaren waarom de keten zo gemakkelijk breekt en zo reactiebereid is.
Van vluchtige keten naar nieuwe antimoonchemie
Omdat de rode tri‑antimoonsoort snel uiteenvalt, produceerden de onderzoekers deze ter plaatse voor elke test en onderzochten daarna hoe hij reageert. Kleine wijzigingen in de omstandigheden leidden tot een reeks nieuwe antimoonverbindingen: vervanging van zuurstof in het tegenion door zwavel gaf een zwavel-gekoppelde di-antimoonsoort, terwijl toevoeging van eenvoudige chalcogeen–chalcogeenmoleculen (gebaseerd op zwavel of seleen) antimoon–chalcogeenfragmenten opleverde door het verbreken van die chalcogeen–chalcogeënbindingen. Jodiumhoudende reagentia resulteerden in een jodidecomplex, en reactie van het tri‑antimoonsysteem met een cobaltcarbonyldonor gaf een opvallend cluster waarin antimoonatomen in het hart van een driehoek van cobaltcentra zitten die aan koolmonoxide-liganden gebonden zijn. Vergelijking van deze uitkomsten met reacties van een eenvoudiger antimoonfragment toonde aan dat de sterk geladen keten en zijn reactieve anion verschillende chemische paden volgen.
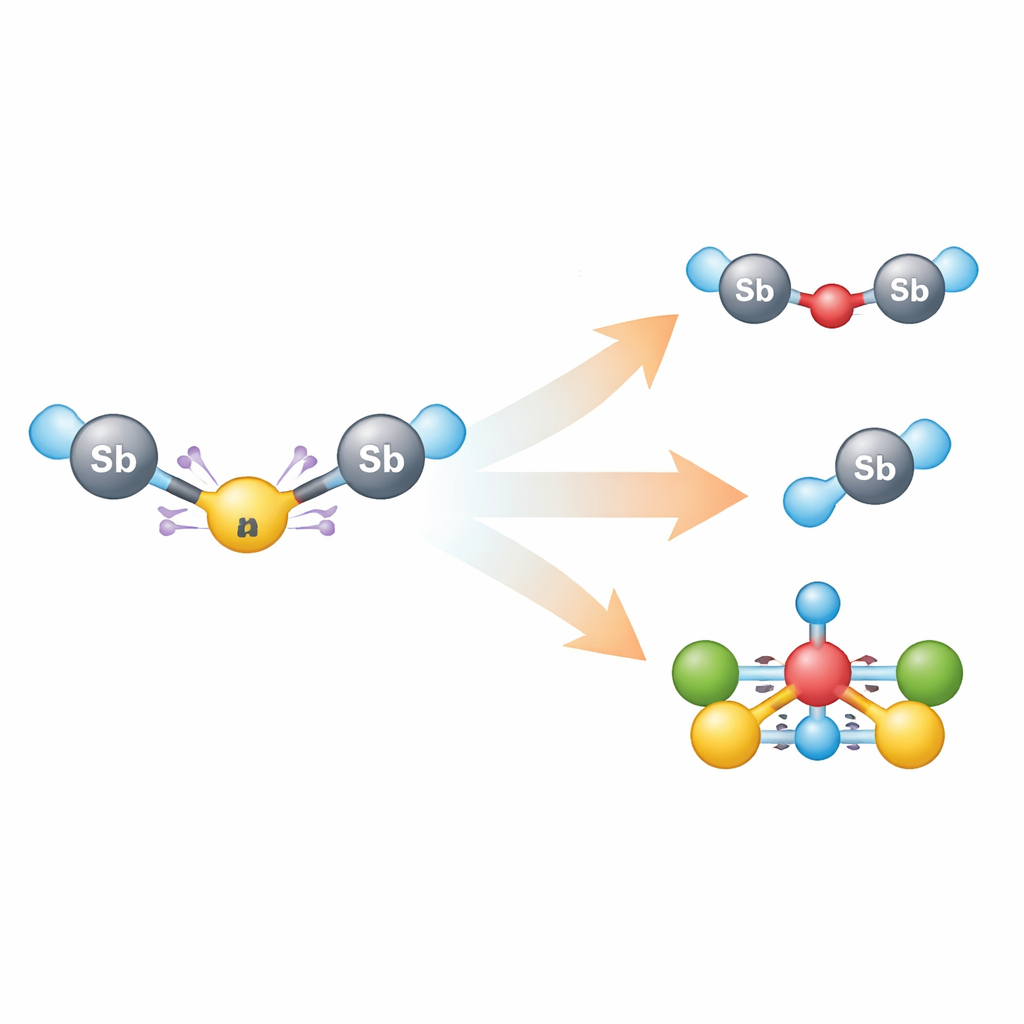
Wat de studie in eenvoudige bewoordingen toont
In wezen zijn de auteurs erin geslaagd een uitzonderlijk kleine en sterk geladen moleculaire keten te vangen en te karakteriseren die normaal te onstabiel zou zijn om te bestuderen. Door een delicate tri‑antimoonkation te koppelen aan een reactief zuurstofrijk anion en het net genoeg te stabiliseren met fosfinegrepen, laten ze zien hoe zware atomen op ongebruikelijke manieren elektronen kunnen delen, hoe lading en zwakke bindingen hand in hand gaan, en hoe dergelijke soorten een familie van nieuwe verbindingen kunnen voortbrengen, inclusief gemengde antimoon–cobaltclusters. Voor niet‑specialisten benadrukt dit werk hoe het opzoeken van de grenzen van moleculen — hier het samenpersen van drie positieve ladingen in een lijn van drie atomen — nieuwe bindingspatronen onthult die uiteindelijk tot nieuwe strategieën in hoofd‑groepelementchemie en materiaalontwerp kunnen inspireren.
Bronvermelding: Mukherjee, N., Peerless, B., Nadurata, V.L. et al. Smallest acyclic tricationic molecule containing a Bis(phosphine)-stabilized low-valent triantimony-based Unit. Nat Commun 17, 2697 (2026). https://doi.org/10.1038/s41467-026-70910-5
Trefwoorden: antimoonchemie, multicationische moleculen, metaal–metaal bindingen, hoofd-groepelementclusters, reactieve tussenproducten