Clear Sky Science · es
La molécula tricatiónica acíclica más pequeña que contiene una unidad triantimonio de bajo estado de oxidación estabilizada por bis(fosfina)
Por qué importa este diminuto rompecabezas cargado
Los químicos sienten fascinación por las moléculas que llevan varias unidades de carga positiva, porque concentrar tanta carga en un espacio pequeño suele hacer que se desintegren. Entender cómo domar estas especies inestables ayuda a revelar cómo funcionan realmente los enlaces químicos y puede abrir puertas a nuevos tipos de materiales y catalizadores. Este estudio presenta una molécula en cadena de récord, formada por tres átomos de antimonio que en conjunto llevan tres cargas positivas, junto con una pareja igualmente inusual con carga negativa que contribuye a mantener el sistema unido.
Construyendo una frágil cadena de tres átomos
La mayoría de las moléculas muy cargadas conocidas basadas en elementos del grupo principal forman anillos o aglomerados mayores, que reparten la carga y evitan una repulsión interna intensa. Los autores se propusieron crear algo más extremo: la cadena abierta más pequeña posible de tres átomos pesados enlazados que aún lleve más de una carga positiva. Eligieron el antimonio, un hermano más pesado del arsénico y el fósforo, porque sus átomos grandes pueden acomodar mejor carga adicional. Combinando con cuidado un fragmento de antimonio preformado con una sal de antimonio fuertemente atractora a muy baja temperatura, y envolviendo los extremos de la cadena con un agarre voluminoso de «bis(fosfina)», lograron aislar un compuesto rojo intenso que contiene una unidad de tres átomos de antimonio recta pero doblada con una carga total de +3.
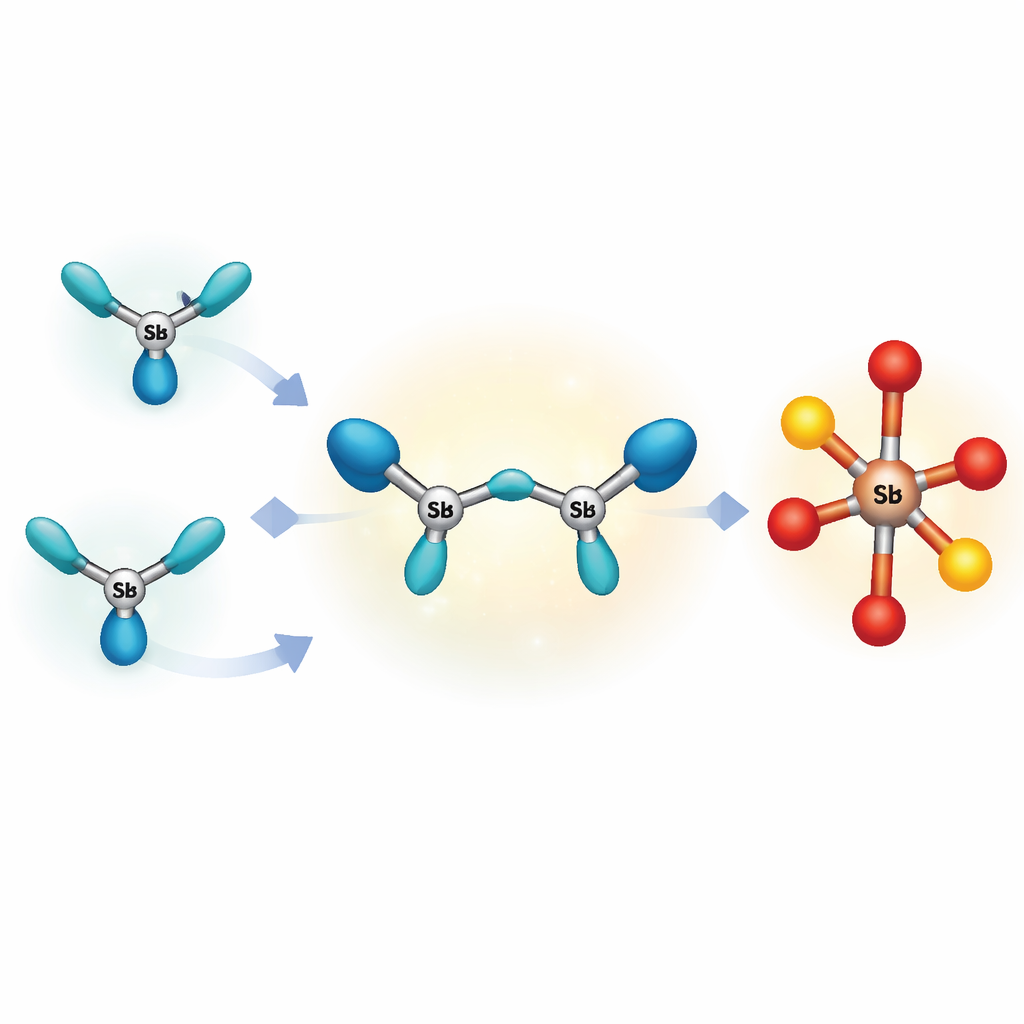
Un extraño compañero en el lado negativo
Para equilibrar las tres cargas positivas, el cristal también contiene un anión poco frecuente, o unidad con carga negativa, basado en antimonio enlazado a oxígeno y a cuatro grupos triflado. Las medidas por rayos X muestran una columna O–Sb–O con cuatro brazos adicionales ricos en oxígeno, creando enlaces antimonio–oxígeno muy polares que son altamente reactivos. Dado que ni la cadena cargada positivamente ni este inusual compañero negativo están bien protegidos por entornos voluminosos, la sal completa es térmicamente frágil: incluso un calentamiento suave la descompone, precipita antimonio metálico y aparece un producto más estable. Este comportamiento significa que la cadena triantimonio original existe sólo como una instantánea fugaz en la ruta hacia otros compuestos.
Escudriñando el enlace
El equipo usó cálculos cuántico‑químicos para mirar en la estructura electrónica de la cadena triantimonio. Encontraron que los tres átomos de antimonio forman una disposición doblada en forma de «W» sostenida por un enlace débil de tres centros y cuatro electrones a lo largo de la cadena. El átomo central de antimonio porta dos pares de electrones no utilizados, mientras que cada átomo exterior porta uno. El análisis de carga revela una polaridad llamativa: los extremos de la cadena y los átomos de fósforo de los agarres de soporte son relativamente positivos, mientras que el átomo central de antimonio es algo negativo. Esta distribución desigual, junto con el gran tamaño del antimonio y el enlace metal–metal débil, ayuda a explicar por qué la cadena es tan fácil de romper y tan proclive a reaccionar.
De una cadena efímera a nueva química del antimonio
Como la especie triantimonio roja se descompone con rapidez, los investigadores la generaron en el lugar para cada prueba y luego examinaron cómo reacciona. Pequeños cambios en las condiciones dieron lugar a una variedad de nuevos compuestos de antimonio: sustituir el oxígeno del contra‑anión por azufre produjo una especie de diantimonio puenteada por azufre, mientras que añadir moléculas simples de calcógeno–calcógeno (basadas en azufre o selenio) generó fragmentos antimonio–calcógeno al romperse esos enlaces calcógeno–calcógeno. Reactivos que contienen yodo dieron lugar a un complejo yoduro, y al reaccionar el sistema triantimonio con una fuente de carbonilo de cobalto se obtuvo un aglomerado llamativo en el que átomos de antimonio ocupan el núcleo de un triángulo de centros de cobalto unidos a ligandos de monóxido de carbono. Comparar estos resultados con reacciones de un fragmento de antimonio más simple mostró que la cadena altamente cargada y su anión reactivo siguen vías químicas distintas.
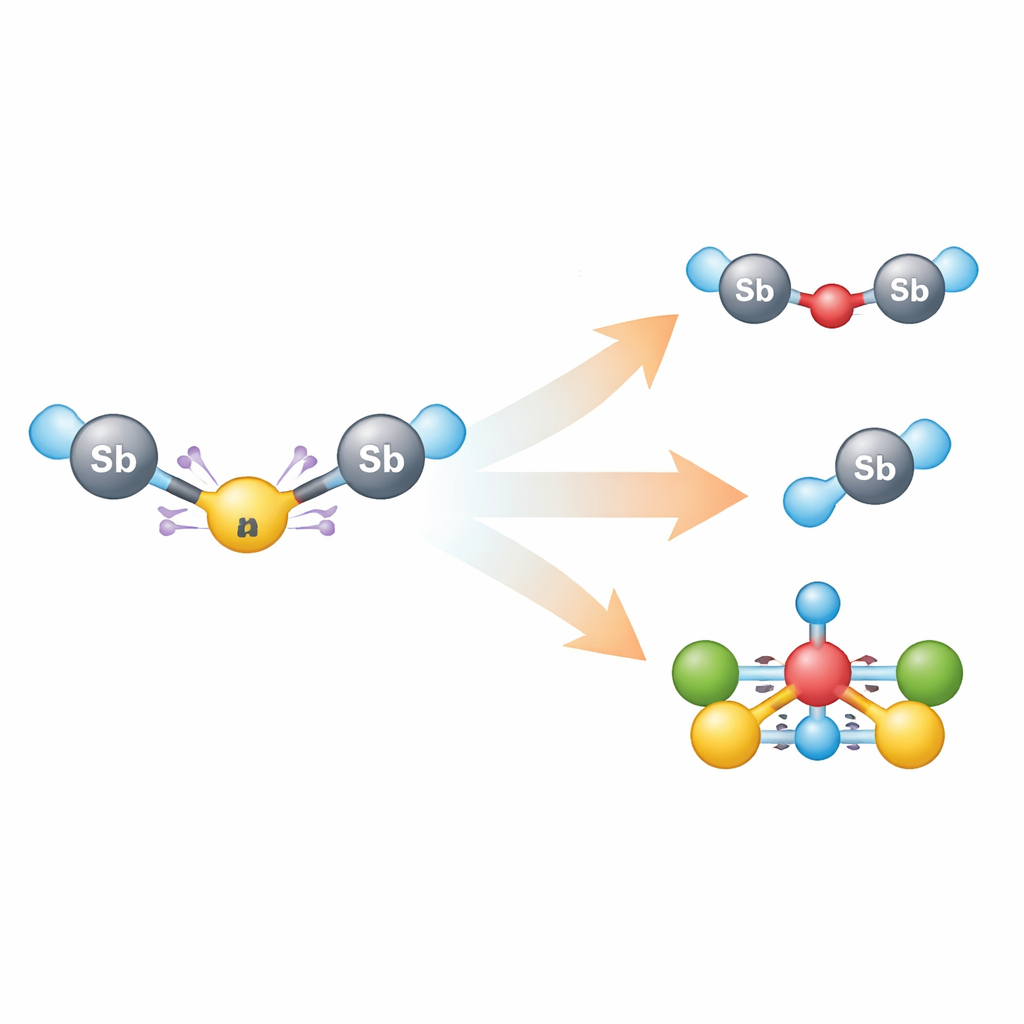
Lo que muestra el estudio en términos simples
En esencia, los autores han logrado capturar y caracterizar una cadena molecular excepcionalmente pequeña y altamente cargada que normalmente sería demasiado inestable para estudiar. Al emparejar un catión triantimonio delicado con un anión rico en oxígeno y reactivo y estabilizarlo lo justo con agarres de fosfina, revelan cómo los átomos pesados pueden compartir electrones de formas inusuales, cómo la carga y la debilidad del enlace van de la mano, y cómo tales especies pueden sembrar una familia de nuevos compuestos, incluidos aglomerados mixtos de antimonio–cobalto. Para el público no especializado, este trabajo destaca cómo llevar las moléculas a sus límites —aquí, empaquetar tres cargas positivas en una línea de tres átomos— descubre nuevos patrones de enlace que pueden inspirar en última instancia estrategias novedosas en la química de elementos principales y el diseño de materiales.
Cita: Mukherjee, N., Peerless, B., Nadurata, V.L. et al. Smallest acyclic tricationic molecule containing a Bis(phosphine)-stabilized low-valent triantimony-based Unit. Nat Commun 17, 2697 (2026). https://doi.org/10.1038/s41467-026-70910-5
Palabras clave: química del antimonio, moléculas multicatiónicas, enlaces metal–metal, aglomerados de elementos principales, intermedios reactivos