Clear Sky Science · de
Kleinste azyklische trikationische Molekül mit einer bis(phosphin)-stabilisierten niedrigvalenten triantimon‑Einheit
Warum dieses winzige geladene Rätsel wichtig ist
Chemiker sind fasziniert von Molekülen, die mehrere positive Ladungseinheiten tragen, weil so viel Ladung auf engem Raum normalerweise zu gewaltiger Abstoßung und Zerfall führt. Zu verstehen, wie man solche instabilen Arten zähmt, hilft zu enthüllen, wie chemische Bindungen tatsächlich funktionieren, und kann neue Wege zu Materialien und Katalysatoren eröffnen. Diese Studie berichtet über ein rekordkleines, kettenförmiges Molekül aus drei Antimon‑Atomen, das zusammen drei positive Ladungen trägt, zusammen mit einem ebenso ungewöhnlichen negativ geladenen Partner, der das System mithält.
Aufbau einer fragilen Drei‑Atome‑Kette
Die meisten bekannten hochgeladenen Moleküle auf Basis der Hauptgruppenelemente bilden Ringe oder größere Cluster, die ihre Ladung verteilen und starke innere Abstoßungen vermeiden. Die Autoren wollten etwas Extremeres schaffen: die kleinstmögliche offene Kette aus drei gebundenen schweren Atomen, die dennoch mehr als eine positive Ladung trägt. Sie wählten Antimon, einen schwereren Verwandten von Arsen und Phosphor, weil seine großen Atome zusätzliche Ladung besser aufnehmen können. Durch die gezielte Kombination eines vorgefertigten Antimon‑Fragments mit einem stark elektronenziehenden Antimon‑Salz bei sehr niedrigen Temperaturen und dem Ummanteln der Kettenenden mit einem sperrigen „bis(phosphin)“‑Haltegriff gelang es ihnen, eine leuchtend rote Verbindung zu isolieren, die eine gerade‑bis‑gebogene Drei‑Antimon‑Einheit mit einer Gesamtladung von plus drei enthält.
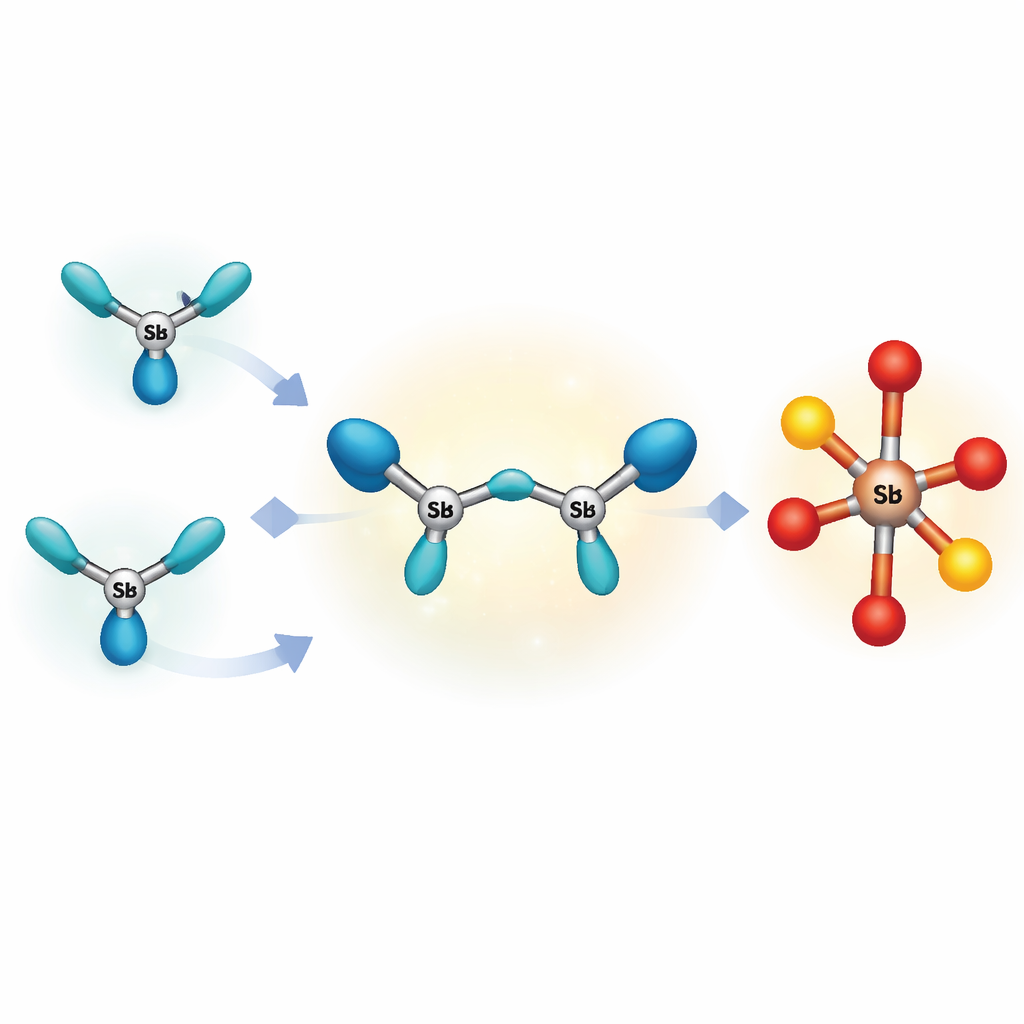
Ein seltsamer negativer Partner
Um drei positive Ladungen auszugleichen, enthält das Kristallgitter außerdem ein seltenes Anion, eine negativ geladene Einheit, bestehend aus Antimon, das an Sauerstoff und vier Triflat‑Gruppen gebunden ist. Röntgenmessungen zeigen eine O–Sb–O‑Achse mit vier zusätzlichen sauerstoffreichen Armen, die sehr polare Antimon‑Sauerstoff‑Bindungen bilden, die stark reaktiv sind. Da weder die positiv geladene Kette noch dieser ungewöhnliche negative Partner durch sperrige Umgebungen hinreichend geschützt sind, ist das gesamte Salz thermisch fragil: selbst sanftes Erwärmen führt zu Zerfall, Ausfällung metallischen Antimons und Bildung eines stabileren Produktes. Dieses Verhalten bedeutet, dass die ursprüngliche Triantimon‑Kette nur als flüchtiger Schnappschuss auf dem Weg zu anderen Verbindungen existiert.
Ein Blick in die Bindungsverhältnisse
Das Team nutzte quantenchemische Rechnungen, um in die elektronische Struktur der Triantimon‑Kette zu blicken. Sie fanden, dass die drei Antimon‑Atome eine gebogene „W“-Anordnung bilden, gestützt durch eine schwache Drei‑Zentren‑Vier‑Elektronen‑Bindung entlang der Kette. Das zentrale Antimon‑Atom trägt zwei ungenutzte Elektronenpaare, während jedes Außenelement jeweils eines trägt. Die Ladungsanalyse zeigt eine auffällige Polarität: die Enden der Kette und die Phosphoratome der Stützgriffe sind relativ positiv, während das mittlere Antimon‑Atom etwas negativ geladen ist. Diese ungleichmäßige Verteilung, zusammen mit der großen Größe des Antimons und der schwachen Metall–Metall‑Bindung, erklärt, warum die Kette so leicht zu brechen und so reaktionsfreudig ist.
Von der flüchtigen Kette zur neuen Antimon‑Chemie
Weil die rote Triantimon‑Spezies schnell zerfällt, erzeugten die Forscher sie jeweils in situ für jeden Versuch und untersuchten dann ihr Reaktionsverhalten. Kleine Änderungen der Bedingungen führten zu einer Reihe neuer Antimon‑Verbindungen: der Austausch des Sauerstoffs im Gegenanion gegen Schwefel ergab eine schwefel‑verbrückte Diantimon‑Spezie, während die Zugabe einfacher Chalkogen‑Chalkogen‑Moleküle (auf Schwefel‑ oder Selen‑Basis) durch Aufbrechen dieser Chalkogen–Chalkogen‑Bindungen Antimon‑Chalkogen‑Fragmente erzeugte. Jodhaltige Reagenzien führten zu einem Iodidkomplex, und die Reaktion des Triantimon‑Systems mit einer Cobalt‑carbonyl‑Quelle ergab einen auffälligen Cluster, in dessen Kern Antimon‑Atome sitzen, umgeben von einem Dreieck aus Cobalt‑Zentren, die an Kohlenmonoxid‑Liganden gebunden sind. Der Vergleich dieser Ergebnisse mit Reaktionen eines einfacheren Antimon‑Fragments zeigte, dass die hochgeladene Kette und ihr reaktives Anion unterschiedliche Reaktionswege einschlagen.
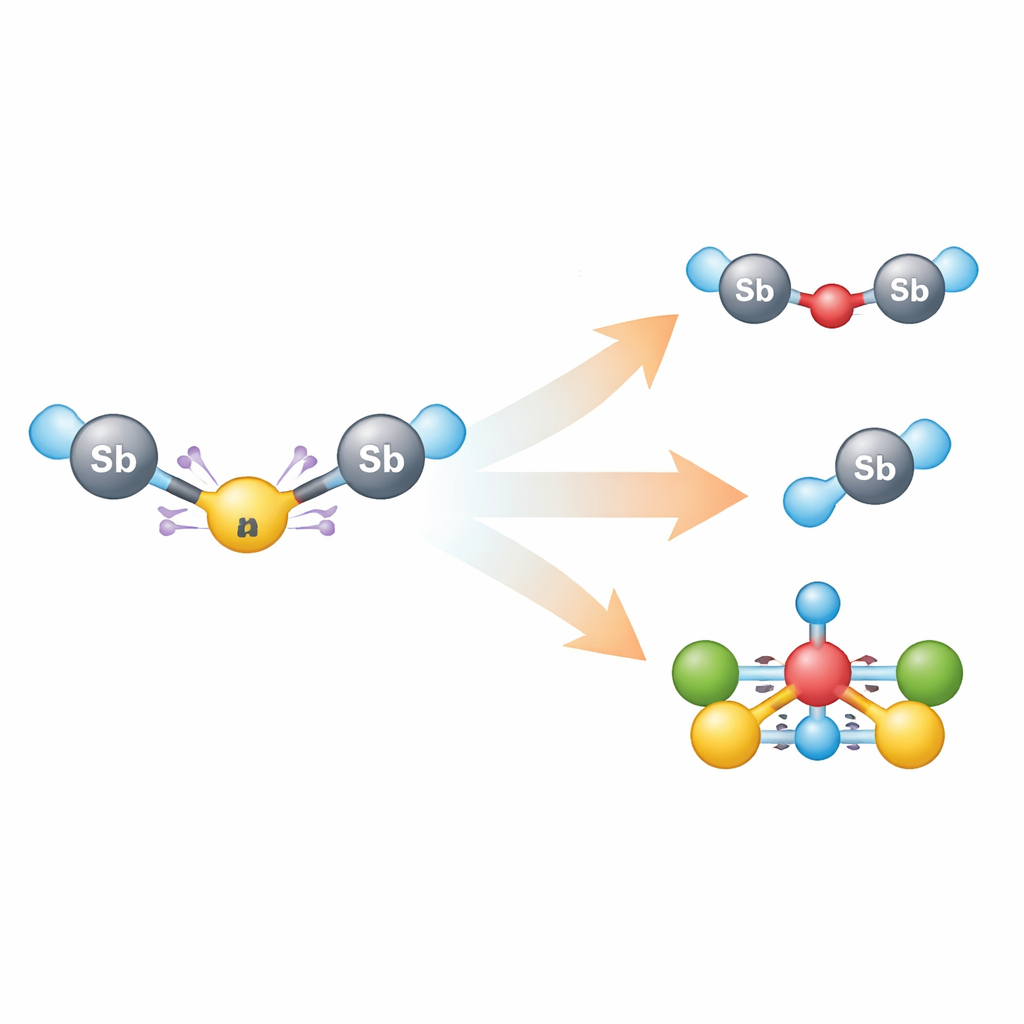
Was die Studie einfach ausgedrückt zeigt
Im Kern ist es den Autoren gelungen, eine außergewöhnlich kleine und stark geladene Molekülkette einzufangen und zu charakterisieren, die normalerweise zu instabil wäre, um sie zu untersuchen. Durch das Paaren eines empfindlichen Triantimon‑Kations mit einem reaktiven, sauerstoffreichen Anion und die gerade ausreichende Stabilisierung durch Phosphin‑Griffe zeigen sie, wie schwere Atome Elektronen auf ungewöhnliche Weise teilen, wie Ladung und Bindungsschwäche Hand in Hand gehen und wie solche Arten den Grundstein für eine Familie neuer Verbindungen legen können, einschließlich gemischter Antimon–Cobalt‑Cluster. Für Nicht‑Spezialisten macht diese Arbeit deutlich, dass das Ausreizen molekularer Grenzen — hier das Unterbringen von drei positiven Ladungen in einer Dreierlinie — neue Bindungsmuster aufdeckt, die letztlich frische Strategien in der Hauptgruppenchemie und im Materialdesign inspirieren könnten.
Zitation: Mukherjee, N., Peerless, B., Nadurata, V.L. et al. Smallest acyclic tricationic molecule containing a Bis(phosphine)-stabilized low-valent triantimony-based Unit. Nat Commun 17, 2697 (2026). https://doi.org/10.1038/s41467-026-70910-5
Schlüsselwörter: Antimon‑Chemie, multikationische Moleküle, Metall–Metall‑Bindung, Hauptgruppenkügelchen, reaktive Zwischenprodukte