Clear Sky Science · it
La più piccola molecola tricationica aciclica contenente un’unità tri-antimonio a basso stato di ossidazione stabilizzata da Bis(fosfina)
Perché questo piccolo rompicapo carico conta
I chimici sono affascinati dalle molecole che portano più unità di carica positiva, perché concentrare così tanta carica in uno spazio ridotto di solito le fa disgregare. Capire come domare specie così instabili aiuta a rivelare come funzionano davvero i legami chimici e può aprire la strada a nuovi tipi di materiali e catalizzatori. Questo studio descrive una molecola a catena di dimensioni record, costruita da tre atomi di antimonio che insieme portano tre cariche positive, affiancata da un partner negativo altrettanto insolito che contribuisce a tenere insieme il sistema.
Costruire una fragile catena a tre atomi
La maggior parte delle molecole altamente cariche note basate su elementi del gruppo principale forma anelli o cluster più grandi, che distribuiscono la carica e evitano forti repulsioni interne. Gli autori si sono posti l’obiettivo di creare qualcosa di più estremo: la più piccola catena aperta possibile di tre atomi pesanti legati tra loro che porti ancora più di una singola carica positiva. Hanno scelto l’antimonio, cugino più pesante di arsenico e fosforo, perché i suoi atomi grandi possono meglio accomodare carica in eccesso. Combinando con cura un frammento di antimonio preformato con un sale di antimonio fortemente attrattivo a temperature molto basse, e avvolgendo le estremità della catena con una presa ingombrante di tipo “bis(fosfina)”, sono riusciti a isolare un composto rosso brillante contenente un’unità triantimonio lineare‑ma‑piegata con carica totale di +3.
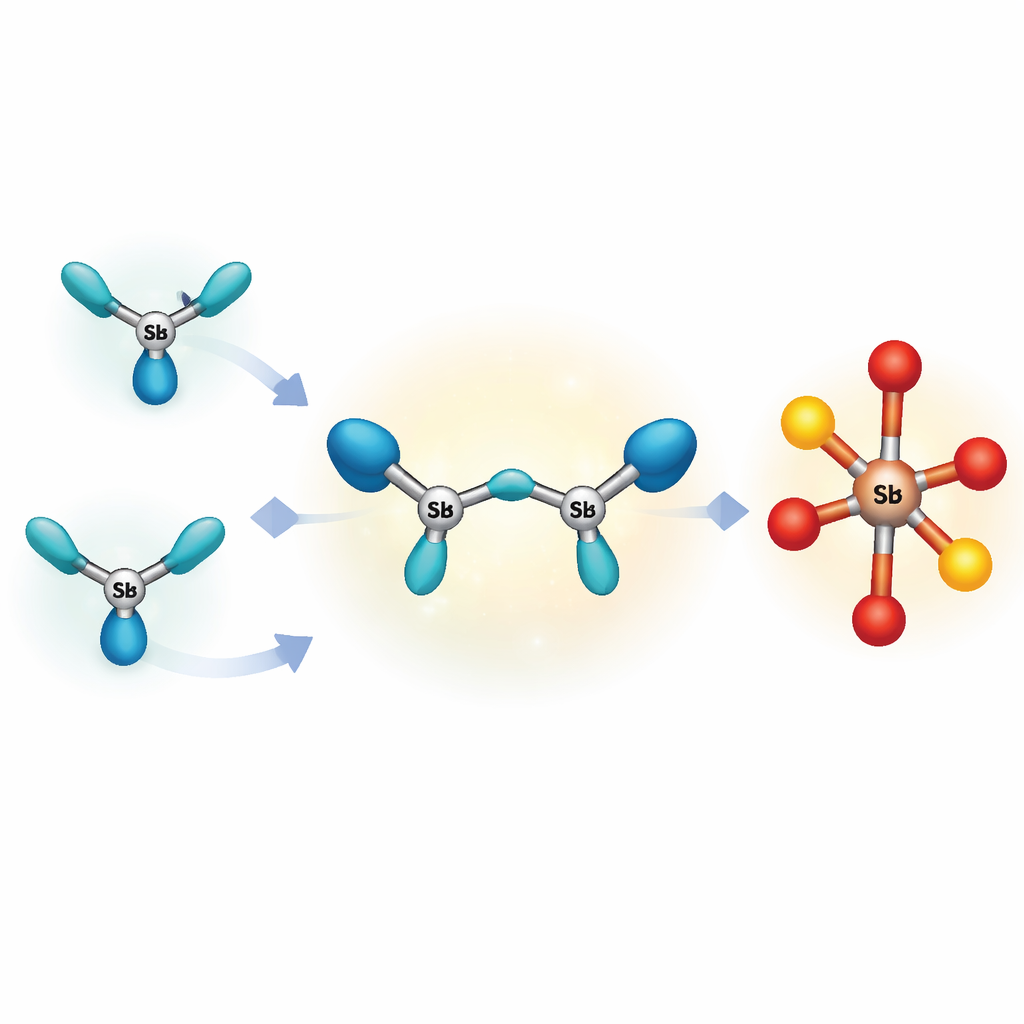
Un partner negativo strano
Per bilanciare tre cariche positive, il cristallo contiene anche un anione raramente osservato, cioè un’unità caricata negativamente basata su antimonio legato a ossigeno e a quattro gruppi triflate. Misure a raggi X mostrano una spina O–Sb–O con quattro bracci aggiuntivi ricchi di ossigeno, creando legami antimonio–ossigeno molto polari e altamente reattivi. Poiché né la catena carica positivamente né questo insolito partner negativo sono ben protetti da ingombri sterici, il sale è termicamente fragile: anche un leggero riscaldamento ne provoca la decomposizione, la precipitazione di antimonio metallico e la comparsa di un prodotto più stabile. Questo comportamento indica che la catena triantimonio originale esiste solo come un’istantanea effimera lungo il percorso verso altri composti.
Uno sguardo all’interno del legame
Il team ha utilizzato calcoli quantistico‑chimici per scrutare la struttura elettronica della catena triantimonio. Hanno scoperto che i tre atomi di antimonio formano una disposizione piegata a “W” sostenuta da un debole legame a tre centri e quattro elettroni lungo la catena. L’atomo centrale di antimonio porta due coppie di elettroni non coinvolte, mentre ciascun atomo esterno ne porta una. L’analisi della carica rivela una polarità marcata: le estremità della catena e gli atomi di fosforo delle impugnature di supporto sono relativamente positivi, mentre l’atomo centrale di antimonio è leggermente negativo. Questa distribuzione irregolare, insieme alla grandezza dell’antimonio e alla debolezza del legame metallico‑metallico, aiuta a spiegare perché la catena si rompe così facilmente ed è così propensa a reagire.
Dalla catena effimera a nuova chimica dell’antimonio
Poiché la specie triantimonio rossa si disintegra rapidamente, i ricercatori l’hanno generata in situ per ogni prova e poi hanno indagato come reagisce. Piccole modifiche nelle condizioni hanno portato a una serie di nuovi composti di antimonio: sostituire l’ossigeno nell’anione contropartita con zolfo ha dato una specie diantimonio ponte‑zolfo, mentre l’aggiunta di semplici molecole calcogen‑calcogen (a base di zolfo o selenio) ha prodotto frammenti antimonio‑calcogeno rompendo quei legami calcogeno–calcogeno. Reagenti contenenti iodio hanno portato a un complesso ioduro, e la reazione del sistema triantimonio con una sorgente di carbonile di cobalto ha generato un cluster sorprendente in cui gli atomi di antimonio occupano il nucleo di un triangolo di centri di cobalto legati a leganti monossido di carbonio. Il confronto di questi esiti con le reazioni di un frammento di antimonio più semplice ha mostrato che la catena altamente caricata e il suo anione reattivo seguono vie chimiche distinte.
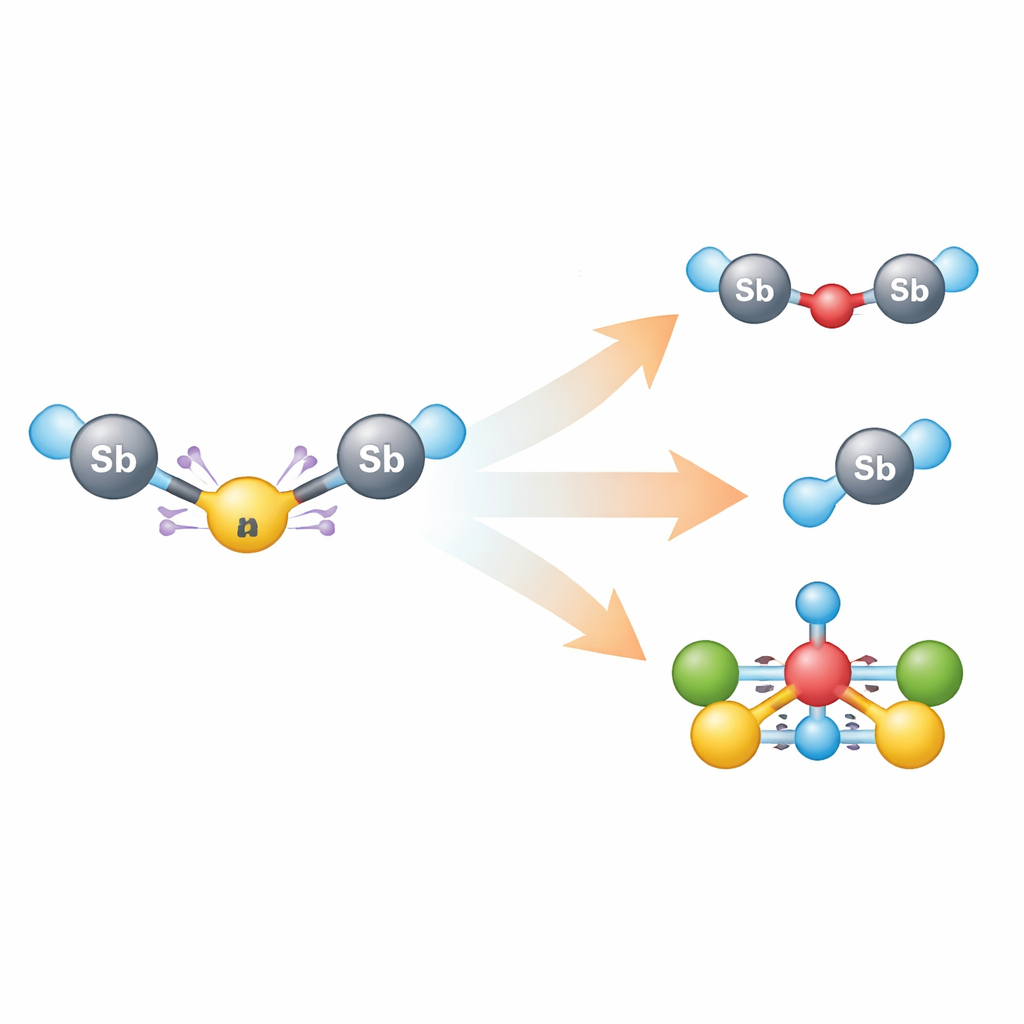
Cosa mostra lo studio in termini semplici
In sostanza, gli autori sono riusciti a catturare e caratterizzare una catena molecolare eccezionalmente piccola e altamente caricata che normalmente sarebbe troppo instabile per essere studiata. Abbinando un catione triantimonio delicato con un anione ricco di ossigeno e reattivo e stabilizzandolo appena quanto basta con impugnature fosfine, rivelano come atomi pesanti possano condividere elettroni in modi insoliti, come carica e debolezza del legame vadano di pari passo e come tali specie possano dare origine a una famiglia di nuovi composti, inclusi cluster misti antimonio‑cobalto. Per i non specialisti, questo lavoro mette in luce come spingere le molecole ai loro limiti — qui, concentrare tre cariche positive in una linea di tre atomi — scoperchi nuovi schemi di legame che possono infine ispirare strategie innovative nella chimica del gruppo principale e nel design dei materiali.
Citazione: Mukherjee, N., Peerless, B., Nadurata, V.L. et al. Smallest acyclic tricationic molecule containing a Bis(phosphine)-stabilized low-valent triantimony-based Unit. Nat Commun 17, 2697 (2026). https://doi.org/10.1038/s41467-026-70910-5
Parole chiave: chimica dell’antimonio, molecole multicationiche, legame metallico‑metallico, cluster del gruppo principale, intermedi reattivi