Clear Sky Science · nl
Voorspelling van sterke Cu(I)–He-interactie bij open metaalplaatsen maakt isotopen-selectieve heliumadsorptie mogelijk
Een nieuwe manier om het meest onaantastbare gas te temmen
Helium staat bekend als nagenoeg onreactief, maar is cruciaal voor MRI‑scanners, geavanceerde elektronica en baanbrekende natuurkunde. Eén zeldzame vorm, helium‑3, is zo schaars en waardevol dat men wereldwijd zoekt naar betere methoden om het van gewoon helium‑4 te scheiden. Dit artikel laat zien dat bepaalde koperhoudende materialen helium veel sterker kunnen aantrekken dan verwacht, en opent daarmee een route naar praktischer terugwinning van helium‑3 bij temperaturen waar de huidige technologie moeite mee heeft.
Waarom helium‑3 zo belangrijk is
Helium‑3 vormt slechts een paar delen per miljoen van natuurlijk helium, maar door zijn bijzondere kwantumgedrag bij extreem lage temperaturen heeft het unieke toepassingen. Het helpt bij het koelen van krachtige magneten in medische scanners, maakt gevoelige lekdetectie in de industrie mogelijk en is een werkpaard in laagtemperatuurexperimenten in de fysica. Ook wordt het beschouwd als mogelijke brandstof voor geavanceerde fusie‑reactoren, die schonere energie zouden kunnen leveren door geladen deeltjes te produceren in plaats van gevaarlijke neutronen. Tegenwoordig komt het meeste helium‑3 nog indirect uit de vervalproducten van tritium in nucleaire voorraden, en het scheiden van helium‑3 van helium‑4 vereist doorgaans temperaturen van slechts enkele graden boven het absolute nulpunt. Die combinatie van schaarste, vraag en kostbare verwerking maakt elke nieuwe scheidingsmethode aantrekkelijk.
Het ontdekken van een onverwachte binding
De conventionele opvatting is dat helium nauwelijks aan iets blijft plakken omdat de elektronen zeer sterk gebonden en moeilijk vervormbaar zijn. De auteurs dagen dit beeld uit door eenvoudige clusters te bestuderen waarin een koperion in de oxidatietoestand +1, Cu(I), omgeven is door verschillende tegenhangers en vervolgens door een heliumatoom wordt benaderd. Met behulp van geavanceerde kwantumchemie vinden ze dat wanneer koper gepaard gaat met geschikte negatief geladen partners zoals fluoride of hydroxide, een heliumatoom verrassend sterk kan binden—tot ongeveer 19 kilojoule per mol, veel meer dan de zwakke aantrekking tussen typische edelgasparen. Analyse van de elektrondichtheid toont dat helium gepolariseerd raakt en zelfs een klein deel van een elektron aan koper kan doneren, waardoor een binding ontstaat die deels elektrostatistisch en licht covalent van karakter is. 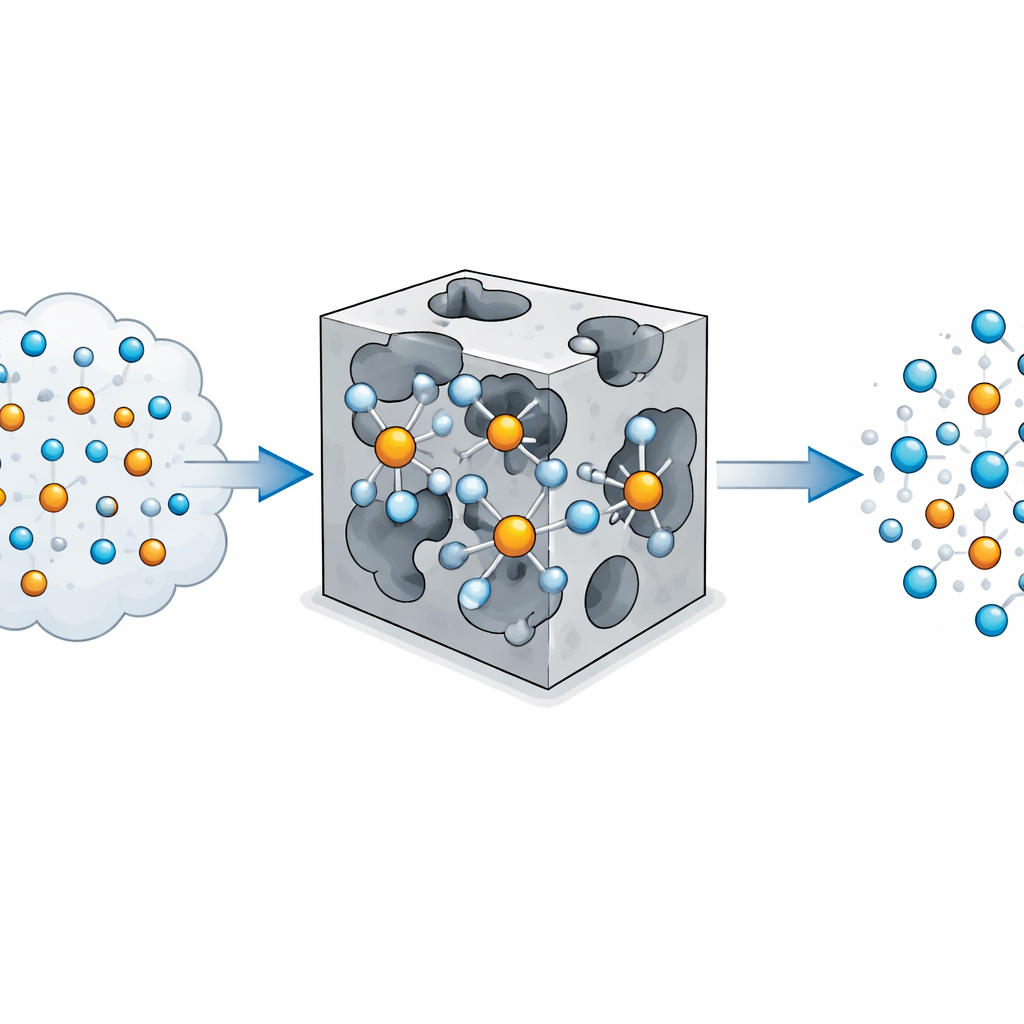
Van simpele clusters naar echte materialen
Met deze inzichten zoekt het team naar realistische materialen die ondergecoordineerde Cu(I)-plaatsen herbergen—koperatomen die slechts aan twee of drie buren gebonden zijn en daardoor relatief blootliggen. Ze bestuderen moleculaire "kroonether"-ringen, fragmenten van zeolieten (poruze aluminosilicaten) en metaal‑organische raamwerken (MOFs), kristallijne netwerken van metaalknopen en organische linkerers. Door een efficiënte maar nauwkeurige kwantummethode te combineren met een op maat gemaakte behandeling van de kwantumbeweging van helionuclei, schatten ze hoe sterk helium in elke omgeving bindt en hoe die binding verschilt tussen helium‑3 en helium‑4. In veel gevallen blijft helium veel sterker plakken dan verwacht, vooral wanneer het kopercentrum tweevoudig gecoördineerd is en in een gebogen geometrie staat die ruimte laat voor een nauwe nadering van helium.
Benutten van subtiele kwantumverschillen
De sleutel tot isotopenscheiding ligt niet alleen in hoe sterk helium bindt, maar in hoe de kwantum nulpuntsbeweging verschilt tussen het lichtere helium‑3 en het zwaardere helium‑4. Zelfs bij lage temperaturen trilt elk atoom in zijn bindingsput. Omdat helium‑3 lichter is, heeft het een hogere nulpuntsenergie en verkent het een iets groter ruimtelijk gebied, wat de binding effectief verzwakt in vergelijking met helium‑4. De auteurs berekenen deze kwantumeffecten nauwkeurig door het energielandschap langs de koper–helium‑binding in kaart te brengen en de corresponderende Schrödinger‑vergelijking numeriek op te lossen. Ze tonen aan dat sterke Cu–He‑interacties het verschil in nulpuntsenergieën versterken genoeg om aanzienlijke voorkeuren voor de ene isotoop boven de andere te creëren, gekwantificeerd als scheidingsfactoren die ver boven die van de huidige technologieën bij dezelfde temperatuur liggen.
Veelbelovende koperen raamwerken voor koeler maar praktisch gebruik
Onder de vele geteste materialen springen bepaalde zeolietmodellen en vooral een MOF gebaseerd op een koper‑chloride bouwblok (bekend uit het kristal WOLRIZ) eruit. In deze MOF binden tweevoudig gecoördineerde Cu(I)-plaatsen met een gebogen opstelling helium met ongeveer 4 tot 6 kilojoule per mol—sterk voor helium maar niet zo sterk dat het gas niet weer kan worden losgelaten. Bij het kookpunt van vloeibaar waterstof, 20 kelvin, nadert de berekende scheidingsfactor voor helium‑4 ten opzichte van helium‑3 drie, wat duidelijk de huidige benaderingen overstijgt die zelfs lagere temperaturen vereisen om vergelijkbare of kleinere effecten te bereiken. De studie suggereert dat verdere afstemming van de koperomgeving, of het verkennen van andere metalen met vergelijkbaar gedrag, nog betere kandidaten kan opleveren. 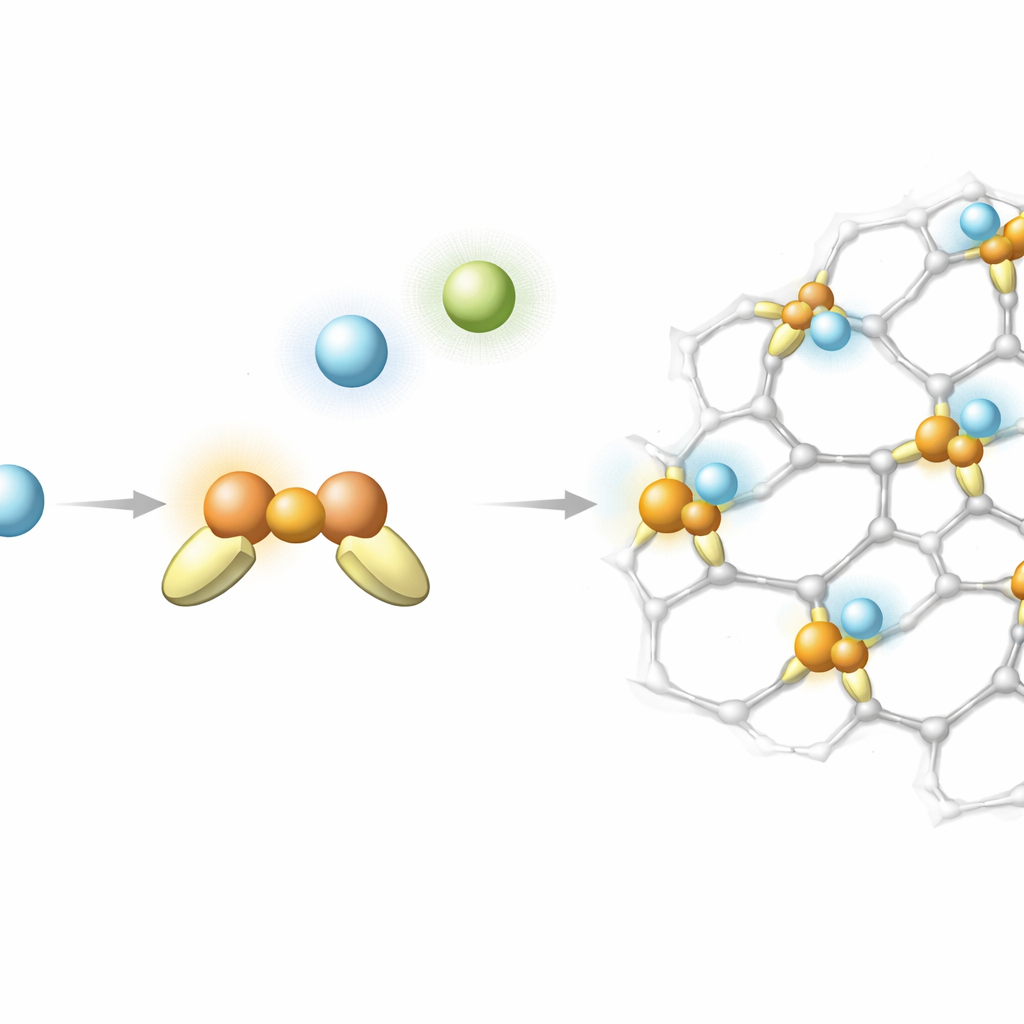
Wat dit betekent voor helium en daarbuiten
Simpel gezegd laten de auteurs zien dat het "edelste" gas niet zo ongenaakbaar is als gedacht: wanneer het het juiste soort blootliggende koperplaats tegenkomt, kan helium een verrassend intieme band vormen. Deze sterker‑dan‑verwachte aantrekking bevoordeelt vanzelfsprekend de ene isotoop boven de andere vanwege hun subtiele kwantumverschillen, en kan mogelijk efficiëntere terugwinning van helium‑3 mogelijk maken bij technologisch behapbare lage temperaturen. Naast praktische implicaties zet dit werk diepgewortelde aannames over heliums passiviteit opzij en nodigt het chemici uit om creatief na te denken over het doen van "chemie" met een gas dat eerder als vrijwel onaantastbaar werd beschouwd.
Bronvermelding: Dongmo, E.G., Das, S., Moncada, F. et al. Prediction of strong Cu(I)–He interaction at open metal sites enables isotope-selective helium adsorption. Nat Commun 17, 2952 (2026). https://doi.org/10.1038/s41467-026-70901-6
Trefwoorden: heliumisotoop scheiding, koper adsorptieplaatsen, metaal‑organische raamwerken, nucleaire kwantumeffecten, poruze materialen