Clear Sky Science · ar
التنبؤ بتفاعل قوي بين Cu(I) وHe في المواقع المعدنية المكشوفة يتيح امتصاص الهيليوم الانتقائي حسب النظير
طريقة جديدة لترويض الغاز الأكثر صعوبة في التعاطي
يشتهر الهيليوم بأنه شبه مستحيل أن يتفاعل مع أي مادة، ومع ذلك فهو ضروري لأجهزة الرنين المغناطيسي والتقنيات الإلكترونية المتقدمة وفيزياء الحافة. أحد أشكاله النادرة، الهيليوم‑3، نادر وثمين للغاية لدرجة أن العالم يبحث بنشاط عن طرق أفضل لفصله عن الهيليوم‑4 العادي. تكشف هذه الورقة أن مواد معينة قائمة على النحاس يمكنها أن تجذب الهيليوم بقوة أكبر مما كان متوقعاً، ما يفتح طريقًا نحو استرداد عملي أكثر للهيليوم‑3 عند درجات حرارة تعجز عنها التقنيات الحالية.
لماذا أهمية الهيليوم‑3 كبيرة للغاية
يشكل الهيليوم‑3 أجزاءً قليلة فقط في المليون من الهيليوم الطبيعي، لكن سلوكه الكمّي غير الاعتيادي عند درجات الحرارة القصوى يُكسبه استخدامات فريدة. يساعد في تبريد المغناطيسات القوية في أجهزة المسح الطبية، ويُمكن من كشف التسربات بدقة في الصناعة، ويستخدم على نطاق واسع في تجارب الفيزياء منخفضة الحرارة. كما أنه مرشح كوقود لاندماج متقدم قد يوفر طاقة أنظف بإنتاجه جسيمات مشحونة بدلاً من إشعاع نيوتروني خطير. اليوم، يأتي معظم الهيليوم‑3 بشكل غير مباشر من تحلل التريتيوم في المخزونات النووية، وفصله عن الهيليوم‑4 يتطلب عادة درجات حرارة قريبة جداً من الصفر المطلق. تخلق هذه التركيبة من الندرة والطلب وتكاليف المعالجة أهمية كبيرة لأي طريقة فصل جديدة.
اكتشاف رابطة غير متوقعة
تقول الحكمة التقليدية إن الهيليوم نادراً ما يلتصق بأي شيء لأن إلكتروناته مرتبطة بقوة ومن الصعب تشويهها. يتحدى المؤلفون هذا الرأي بدراسة مجموعات بسيطة حيث أيون النحاس في حالة التأكسد +1، Cu(I)، محاط بذرات أو جزيئات مرافقَة ثم يقترب منه ذرة هيليوم. باستخدام كيمياء كمية عالية المستوى، يجدون أنه عندما يقترن النحاس بشركاء سالبين مناسبين مثل الفلوريد أو الهيدروكسيد، يمكن لذرة الهيليوم أن ترتبط بقوة مفاجئة — تصل إلى نحو 19 كيلو جول لكل مول، أي أكثر بكثير من جذبات الغازات النبيلة الاعتيادية الضعيفة. يُظهر تحليل كثافة الإلكترون أن الهيليوم يصبح مستقطباً ويمنح حتى جزءًا صغيرًا من إلكترون إلى النحاس، مكوناً رابطة ذات طابع كهربائي جزئي وبضع قوة تساهمية. 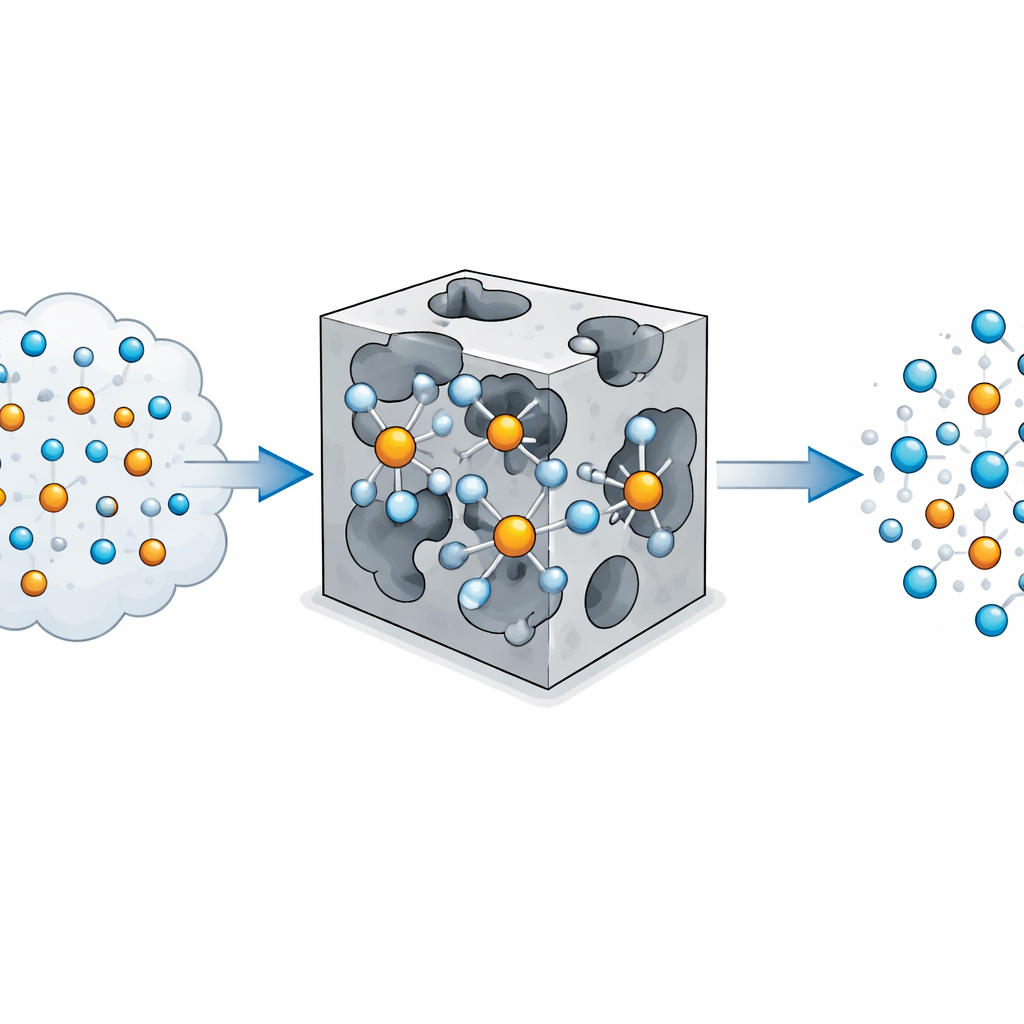
من المجموعات البسيطة إلى المواد الواقعية
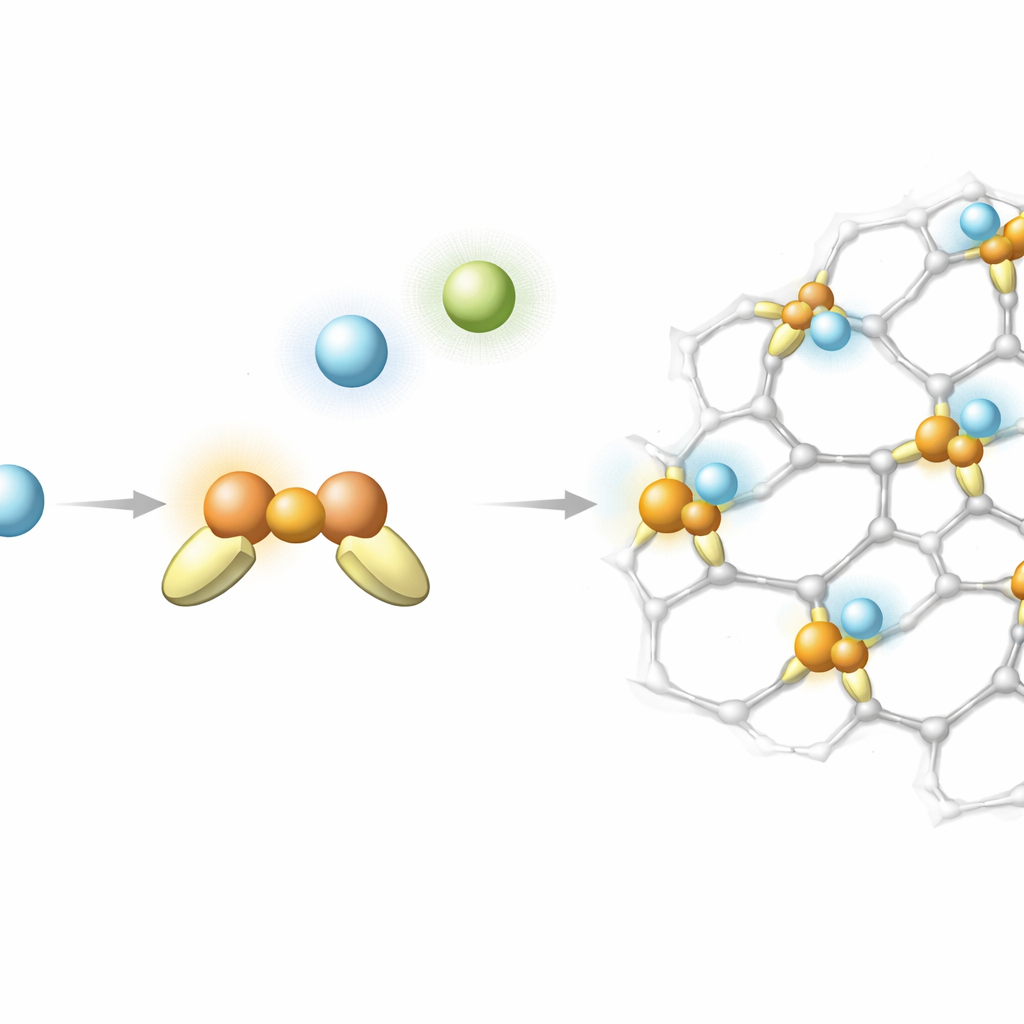
مسلحين بهذه الرؤية، يبحث الفريق عن مواد واقعية تستضيف مواقع Cu(I) ناقصة الإحاطة — ذرات نحاس مرتبطة بجارَين أو ثلاث جيران فقط وبالتالي تظل مكشوفة نسبياً. يدرسون حلقات جزيئية من نوع «إيثر التاج»، وشظايا من الزئوليتات (معادن ألومينوسيليكات مسامية)، وهياكل عضوية‑معدنية (MOFs)، وهي شبكات بلورية من عقد معدنية وروابط عضوية. من خلال دمج طريقة كمية فعّالة لكنها دقيقة مع طريقة مصممة لمعالجة الحركة الكمّية لنوى الهيليوم، يقدّرون مدى قوة ارتباط الهيليوم في كل بيئة وكيف يختلف هذا الارتباط بين الهيليوم‑3 والهيليوم‑4. في كثير من الحالات، يظل الهيليوم ملتصقاً أكثر مما كان متوقعاً، خاصة عندما تكون مركزات النحاس ثنائية التنسيق ومصوّبة بحيث تترك مجالاً لاقتراب الهيليوم عن قرب.
استغلال الفروق الكمّية الطفيفة
المفتاح لفصل النظائر لا يكمن فقط في مدى قوة ارتباط الهيليوم، بل في كيفية اختلاف حركة النقطة الصفرية الكمّية بين الهيليوم‑3 الأخف والهيليوم‑4 الأثقل. حتى عند درجات حرارة منخفضة، تهتز كل ذرة في جيب ارتباطها. وبما أن الهيليوم‑3 أخف وزناً، فله طاقة نقطة صفرية أعلى ويستكشف منطقة فراغية أوسع قليلاً، مما يضعف ارتباطه نسبياً بالمقارنة مع الهيليوم‑4. يحسب المؤلفون هذه التأثيرات الكمّية بعناية عبر رسم منحنى الطاقة على طول رابطة النحاس‑الهيليوم وحل معادلة شرودنغر المقابلة رقمياً. يبينون أن تفاعلات Cu–He القوية تضخم الفرق في طاقات النقطة الصفرية بما يكفي لخلق تفضيلات ملحوظة لأحد النظائر على الآخر، مقاسة كعوامل فصل تتجاوز بكثير ما تحققه تقنيات اليوم عند نفس درجة الحرارة.
هياكل نحاسية واعدة للتشغيل عند برودة عملية
من بين المواد العديدة المختبرة، يبرزت نماذج زئوليتية وخصوصاً هيكل MOF مبني على وحدة بناء نحاسية‑كلوريدية (معروفة من البلورة WOLRIZ). في هذا الـMOF، تربط مواقع Cu(I) ثنائية التنسيق ذات ترتيب منحنٍ الهيليوم بحوالي 4 إلى 6 كيلو جول لكل مول — قوة كبيرة للهيليوم لكنها ليست بحيث تمنع إطلاق الغاز لاحقاً. عند نقطة غليان الهيدروجين السائل، 20 كلفن، يقترب عامل الفصل المحسوب للهيليوم‑4 مقابل الهيليوم‑3 من ثلاثة، متجاوزاً بوضوح النهج الحالية التي تتطلب درجات حرارة أقل لتحقيق تأثيرات مماثلة أو أصغر. وتقترح الدراسة أن تعديل بيئة النحاس أكثر، أو استكشاف معادن أخرى ذات سلوك مشابه، قد يوفر مرشحين أفضل.
ماذا يعني هذا بالنسبة للهيليوم وما بعده
بعبارات بسيطة، يُظهر المؤلفون أن «أنبل» الغازات ليس بعُزلة كما يبدو: عندما يواجه الموقع النحاسي المكشوف المناسب، يمكن للهيليوم أن يشكل شراكة مفاجئة القُرب. هذا الجذب الأقوى من المتوقع يفضّل بشكل طبيعي أحد النظائر على الآخر بسبب اختلافاتهما الكمّية الدقيقة، ما قد يمكّن من حصاد الهيليوم‑3 بكفاءة أكبر عند درجات حرارة باردة لكنها قابلة للتطبيق تقنياً. إلى جانب دلالاته العملية، تطيح هذه الدراسة بأفكار راسخة عن خمول الهيليوم وتدعو الكيميائيين للتفكير بإبداع في إجراء «كيمياء» مع غاز كان يُعتبر سابقاً شبه غير قابل للمس.
الاستشهاد: Dongmo, E.G., Das, S., Moncada, F. et al. Prediction of strong Cu(I)–He interaction at open metal sites enables isotope-selective helium adsorption. Nat Commun 17, 2952 (2026). https://doi.org/10.1038/s41467-026-70901-6
الكلمات المفتاحية: فصل نظائر الهيليوم, مواضع امتصاص النحاس, هياكل عضوية-معدنية, التأثيرات الكمّية النووية, مواد مسامية