Clear Sky Science · fr
Prédiction d’une interaction Cu(I)–He forte sur des sites métalliques ouverts permettant l’adsorption hétéro-isotopique de l’hélium
Une nouvelle façon de dompter le gaz le plus intouchable
L’hélium est célèbre pour sa quasi‑absence de réactivité, et pourtant il est indispensable aux appareils d’IRM, à l’électronique avancée et aux expériences de physique de pointe. Une forme rare, l’hélium‑3, est si peu abondante et si précieuse que le monde cherche activement de meilleures méthodes pour le séparer de l’hélium‑4 courant. Cet article révèle que certains matériaux à base de cuivre peuvent attirer l’hélium bien plus fortement qu’attendu, ouvrant la voie à une récupération plus pratique de l’hélium‑3 à des températures où les technologies actuelles échouent.
Pourquoi l’hélium‑3 est si important
L’hélium‑3 ne représente que quelques parties par million de l’hélium naturel, mais son comportement quantique inhabituel à très basse température lui confère des usages uniques. Il sert à refroidir des aimants puissants dans les appareils médicaux, permet la détection de fuites sensibles en industrie et est un pilier des expériences de physique à basse température. C’est aussi un candidat comme carburant pour des réacteurs de fusion avancés, qui pourraient fournir une énergie plus propre en produisant des particules chargées plutôt que des neutrons dangereux. Aujourd’hui, la majeure partie de l’hélium‑3 provient encore indirectement de la désintégration du tritium dans des stocks nucléaires, et sa séparation de l’hélium‑4 nécessite généralement des températures proches du zéro absolu. Cette combinaison de rareté, de demande et de coûts de traitement rend toute nouvelle méthode de séparation extrêmement attrayante.
La découverte d’une liaison inattendue
La sagesse conventionnelle veut que l’hélium adhère très peu aux autres espèces, ses électrons étant fortement liés et difficiles à polariser. Les auteurs remettent en question cette idée en examinant de petits agrégats où un ion cuivre à l’état d’oxydation +1, Cu(I), est entouré de différents partenaires puis approché par un atome d’hélium. Grâce à une chimie quantique de haut niveau, ils montrent que lorsque le cuivre est associé à des partenaires suffisamment électronégatifs comme le fluorure ou l’hydroxyde, un atome d’hélium peut se lier de manière étonnamment forte — jusqu’à environ 19 kilojoules par mole, bien plus que les forces ténues entre gaz nobles typiques. L’analyse de la densité électronique révèle que l’hélium se polarise et cède même une petite fraction d’électron au cuivre, créant une liaison à la fois en grande partie électrostatique et légèrement covalente. 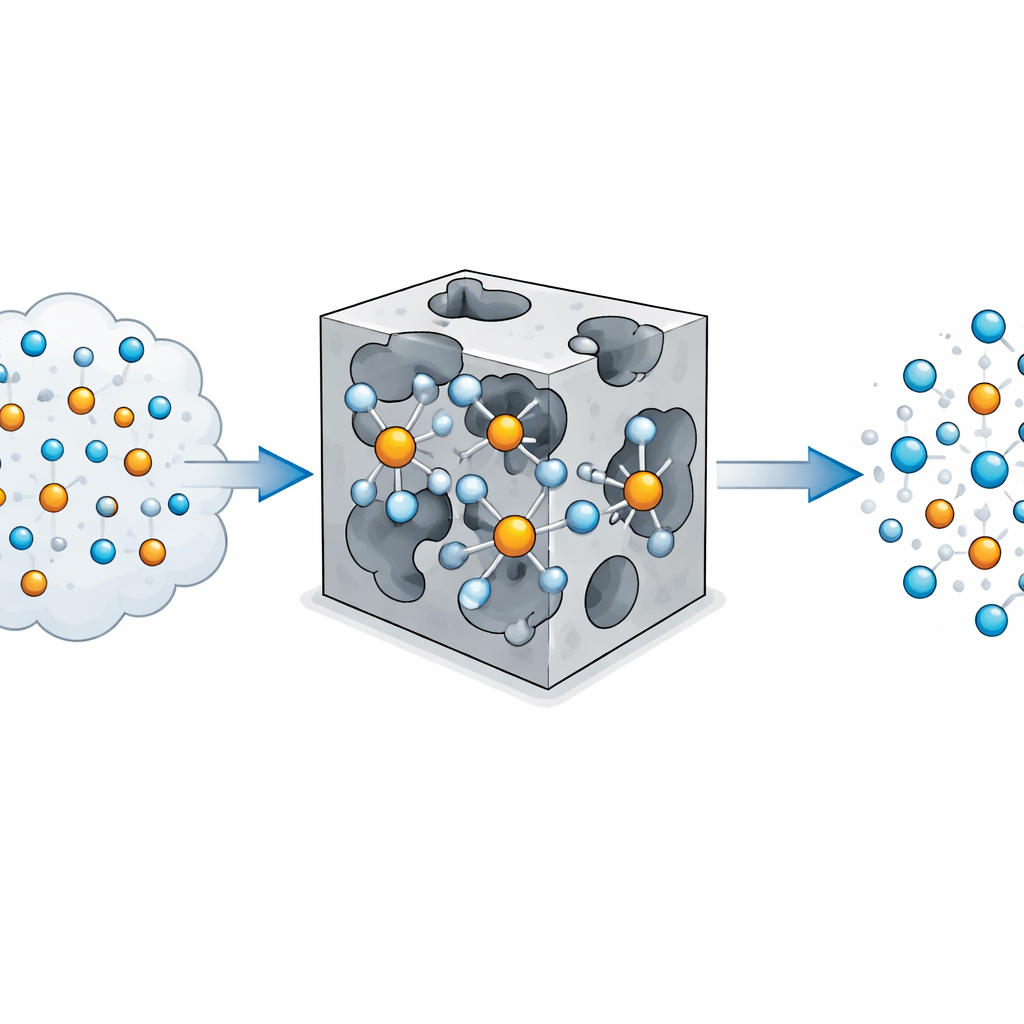
Des agrégats simples aux matériaux réels
Fort de cette compréhension, l’équipe recherche des matériaux réalistes hébergeant des sites Cu(I) sous‑coordonnés — des atomes de cuivre liés à seulement deux ou trois voisins et donc relativement exposés. Ils étudient des anneaux moléculaires de type « couronne », des fragments de zéolites (minéraux aluminosilicatés poreux) et des cadres métal‑organiques (MOF), réseaux cristallins de nœuds métalliques et de liaisons organiques. En combinant une méthode quantique efficace mais précise avec un traitement adapté du mouvement quantique des noyaux d’hélium, ils estiment la force d’adsorption de l’hélium dans chaque environnement et comment cette adhésion diffère entre l’hélium‑3 et l’hélium‑4. Dans de nombreux cas, l’hélium s’accroche bien davantage que prévu, en particulier lorsque le centre de cuivre est à coordination binaire et dispose d’une géométrie coudée laissant de l’espace pour un fort rapprochement de l’hélium.
Exploiter de subtiles différences quantiques
La clé de la séparation isotopique réside non seulement dans la force de liaison de l’hélium, mais aussi dans la différence de mouvement zéro‑point entre l’hélium‑3, plus léger, et l’hélium‑4, plus lourd. Même à basse température, chaque atome vibre dans son site d’adsorption. Parce que l’hélium‑3 est plus léger, il a une énergie zéro‑point plus élevée et explore une région d’espace légèrement plus large, ce qui affaiblit effectivement sa liaison par rapport à l’hélium‑4. Les auteurs calculent soigneusement ces effets quantiques en cartographiant le paysage énergétique le long de la liaison cuivre–hélium et en résolvant numériquement l’équation de Schrödinger correspondante. Ils montrent que des interactions Cu–He fortes amplifient la différence d’énergies zéro‑point suffisamment pour créer des préférences isotopiques significatives, quantifiées par des facteurs de séparation bien supérieurs à ceux des technologies actuelles à la même température.
Des cadres cuivreux prometteurs pour une opération plus froide mais pratique
Parmi les nombreux matériaux testés, certains modèles de zéolites et en particulier un MOF basé sur un motif cuivre–chlorure (connu à partir du cristal WOLRIZ) se distinguent. Dans ce MOF, des sites Cu(I) à coordination deux avec une disposition coudée lient l’hélium à hauteur d’environ 4 à 6 kilojoules par mole — fort pour l’hélium mais pas au point d’empêcher le relargage du gaz. Au point d’ébullition de l’hydrogène liquide, 20 kelvin, le facteur de séparation calculé en faveur de l’hélium‑4 par rapport à l’hélium‑3 approche trois, dépassant nettement les approches actuelles qui exigent encore des températures plus basses pour obtenir des effets similaires ou moindres. L’étude suggère qu’un réglage fin de l’environnement du cuivre, ou l’exploration d’autres métaux présentant un comportement analogue, pourrait produire des candidats encore meilleurs. 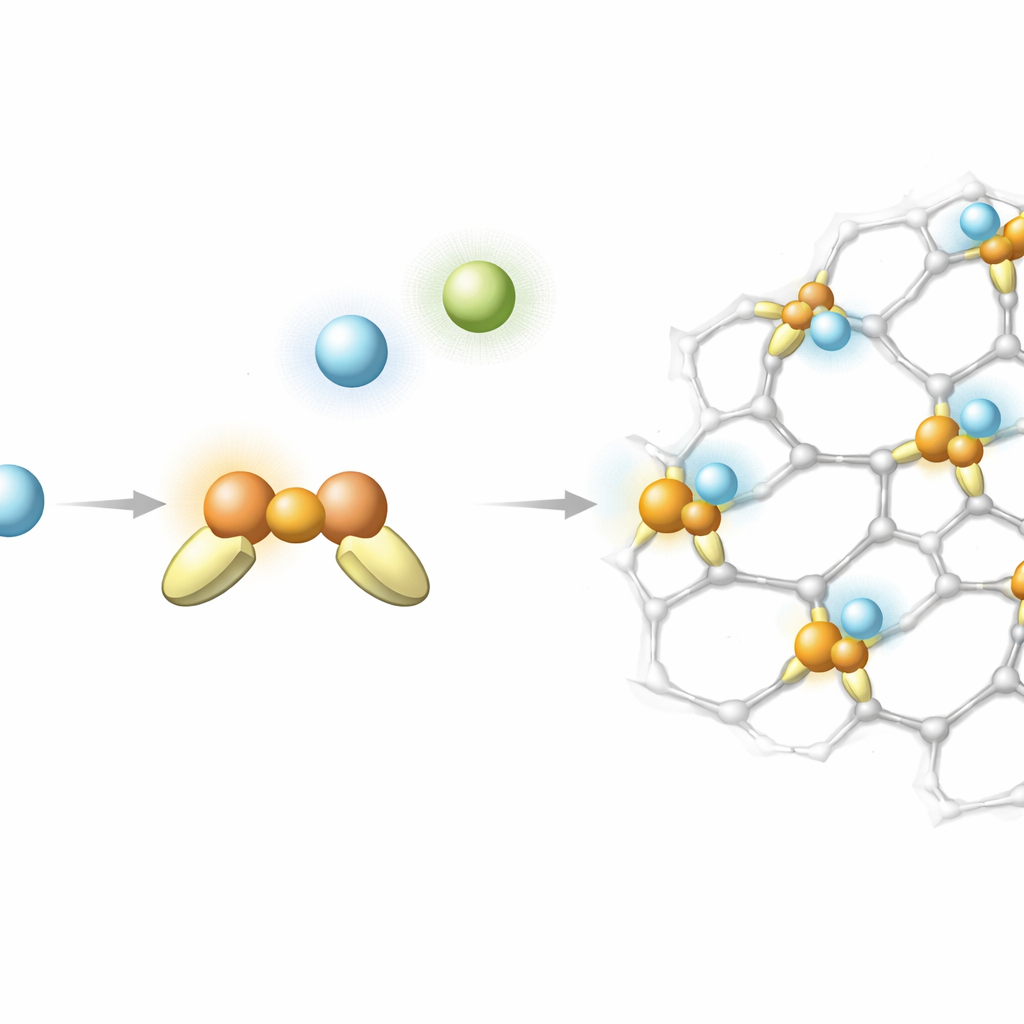
Ce que cela signifie pour l’hélium et au‑delà
En termes concrets, les auteurs montrent que le gaz « le plus noble » n’est pas aussi distant qu’il paraît : lorsqu’il rencontre le bon type de site cuivrique exposé, l’hélium peut établir un partenariat étonnamment intime. Cette attraction plus forte que prévu favorise naturellement un isotope par rapport à l’autre en raison de leurs fines différences quantiques, offrant potentiellement une collecte de l’hélium‑3 plus efficace à des températures froides mais techniquement accessibles. Outre ses implications pratiques, le travail remet en cause des idées reçues sur la passivité de l’hélium et invite les chimistes à imaginer de la « chimie » avec un gaz jusqu’alors considéré comme presque totalement intouchable.
Citation: Dongmo, E.G., Das, S., Moncada, F. et al. Prediction of strong Cu(I)–He interaction at open metal sites enables isotope-selective helium adsorption. Nat Commun 17, 2952 (2026). https://doi.org/10.1038/s41467-026-70901-6
Mots-clés: séparation des isotopes de l’hélium, sites d’adsorption au cuivre, cadres métal‑organique, effets quantiques nucléaires, matériaux poreux