Clear Sky Science · nl
Een cyanidevrije route naar de elektrosynthese van nitrilen
Een verborgen hoek van de chemie opruimen
Nitrilen zijn onopvallende werkpaarden van het moderne leven: ze zitten in geneesmiddelen, kunststoffen, kleurstoffen en landbouwchemicaliën. Toch levert hun industriële productie vaak kooldioxide, stikstofoxiden en zelfs toxisch cyanide op. Deze studie presenteert een manier om nitrilen te maken met elektriciteit en een bescheiden katalysator in plaats van harde hitte of giftige reagentia, en wijst zo de weg naar schonere fabrieken die mogelijk hun eigen afvalgassen kunnen hergebruiken.

Waarom de huidige routes problemen geven
Industrie maakt nitrilen doorgaans door eenvoudige chemicaliën met ammoniak en zuurstof tot enkele honderden graden Celsius te verhitten. Die vurige omstandigheden zijn moeilijk te beheersen, waardoor een deel van de grondstoffen volledig verbrandt tot kooldioxide en stikstofoxiden. Alternatieve routes ruilen hitte in voor chemie die grote hoeveelheden cyaanzouten gebruikt, die zeer toxisch en lastig veilig op schaal te hanteren zijn. Met miljoenen tonnen cyaan die jaarlijks worden gebruikt, laten zelfs kleine inefficiënties gevaarlijk afval achter. Een duurzamere aanpak zou bij kamertemperatuur werken, op hernieuwbare elektriciteit kunnen worden aangesloten en cyanide volledig vermijden, terwijl dezelfde waardevolle producten worden voortgebracht.
Elektriciteit gebruiken als chemisch gereedschap
De auteurs ontwierpen een elektrochemisch systeem dat precies dat doet: het zet elektrische energie in om de reactie aan te drijven die een aldehyde (hier benzaldehyde) en ammoniak omzet in het nitril benzonitril. Het hart van het systeem is een zorgvuldig gestructureerde katalysator gegroeid op koperspons. Kleine clusters kobaltoxide zitten op de topjes van koperoxide-nanorodjes en creëren een groot, actief oppervlak. Wanneer een bescheiden positieve spanning wordt aangelegd in een vloeibare mengeling van benzaldehyde, ammoniak, water en acetonitril, zet de elektrode bijna elke elektron om in het gewenste nitril, met een faradaïsche efficiëntie dicht bij 99% en vrijwel perfecte selectiviteit. De katalysator blijft minstens 100 uur werken met weinig prestatieverlies, wat suggereert dat hij robuust genoeg kan zijn voor industrieel gebruik.
De atomen volgen tijdens de reactie
Om te begrijpen hoe deze schone conversie werkt, volgde het team de reactie realtime met meerdere spectroscopische technieken. Ze ontdekten dat benzaldehyde en ammoniak eerst combineren tot een kortlevend intermediair dat op een imine lijkt—in wezen wordt de koolstof-zuurstof dubbele binding vervangen door een koolstof-stikstof dubbele binding. Deze soort hecht zich aan koperplaatsen op het katalysatoroppervlak, waar onder de aangelegde spanning geleidelijk waterstofatomen worden onttrokken, waardoor de koolstof–stikstof driedubbele binding achterblijft die kenmerkend is voor nitrilen. Computersimulaties ondersteunen dit beeld en tonen dat koper in een hogere oxidatietoestand bijzonder goed is in het wegtrekken van elektronen uit het intermediair, terwijl nabijgelegen kobaltoxide-clusters het aantal actieve sites verhogen en de elektronische eigenschappen van koper subtiel afstemmen om deze dehydrogenatiestap te bevorderen.
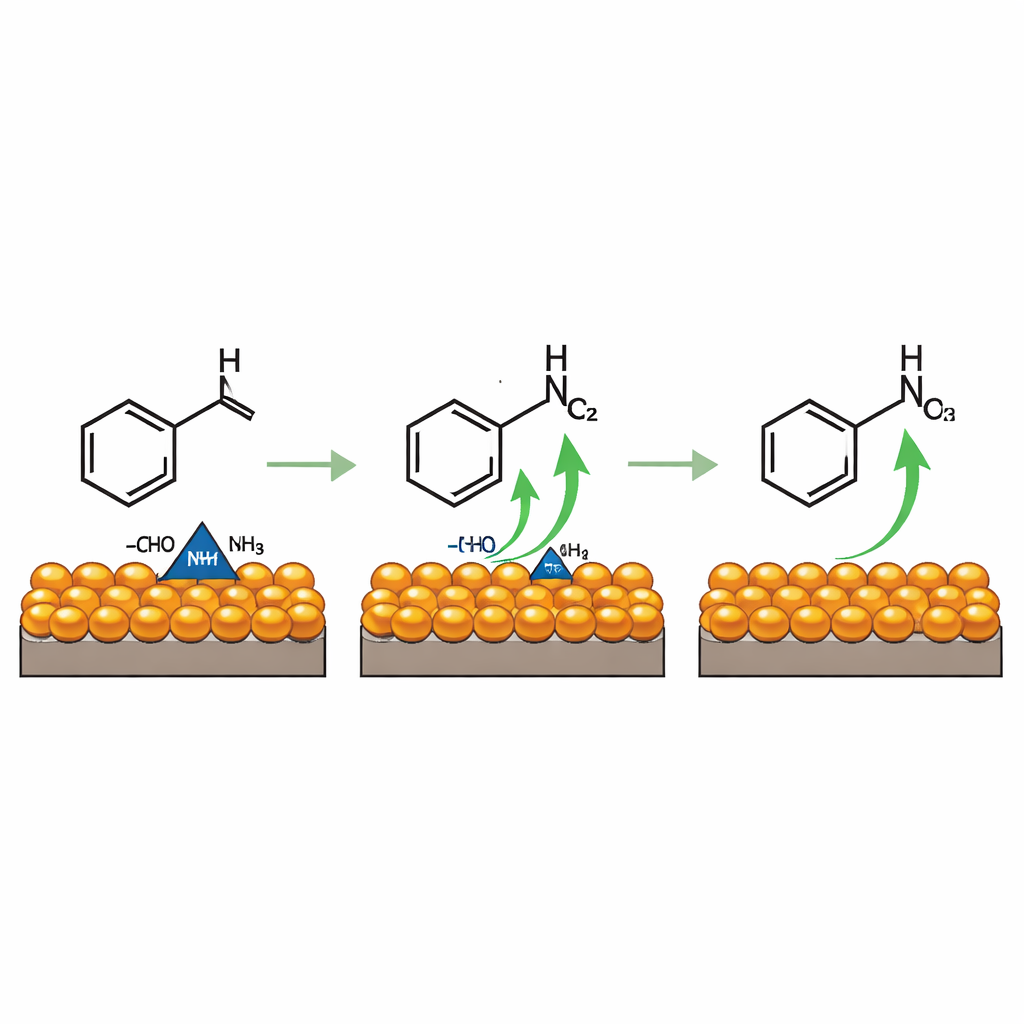
Van eenvoudige aromaten naar producten voor de praktijk
Eenmaal bewezen voor benzaldehyde bleek dezelfde aanpak veelzijdig te zijn. Een reeks aromatische en alifatische aldehyden, waaronder typen met chloor-, broom- of cyano-groepen, werden soepel omgezet in hun nitrilen met efficiënties tussen ongeveer 78% en 97%. Het systeem kan zelfs worden ingezet in meerstapsroutes die beginnen bij alcoholen of eenvoudige koolwaterstoffen zoals tolueen, door die eerst te oxideren naar aldehyden en vervolgens door te zetten naar het nitril. Opmerkelijk is dat sommige van deze uitgangsmaterialen zelf gemaakt kunnen worden uit gevangen kooldioxide, wat wijst op een volledig elektrificeerbare keten van afvalgas naar hoogwaardige chemicaliën.
Vervuilde lucht recyclen tot nuttige producten
Een bijzonder aantrekkelijk aspect is dat de voor de reactie benodigde ammoniak niet per se uit het traditionele, energie-intensieve Haber–Bosch-proces hoeft te komen. De auteurs tonen aan dat de anodische productie van nitrilen gecombineerd kan worden met een katodisch proces dat stikstofoxiden—belangrijke luchtverontreinigers—omzet in ammoniak in dezelfde algehele opstelling. Bij stroomdichtheden tot 200 milliampère per vierkante centimeter komt de hoeveelheid ammoniak die aan de kathode wordt gevormd goed overeen met de hoeveelheid die aan de anode verbruikt wordt. In principe kan een fabriek dus haar eigen stikstofoxide-emissies omzetten in de stikstofbron voor schonere nitrilproductie.
Een veiligere route voor alledaagse moleculen
In eenvoudige bewoordingen vervangt dit werk hete, vuile en soms giftige chemie door een koelere, elektrisch aangedreven methode die dezelfde nuttige nitrilen maakt met veel minder ongewenste bijproducten. Door een slim ontworpen katalysator te combineren met zorgvuldige controle van de reactievormen behalen de auteurs hoge opbrengsten en lange levensduur, terwijl ze de deur openen naar het gebruik van afvalgassen als grondstoffen. Als deze aanpak wordt opgeschaald, kunnen dergelijke elektrochemische routes helpen een deel van de chemische industrie te decarboniseren en de milieuvoetafdruk van veel alledaagse producten te verkleinen zonder de producten zelf te veranderen.
Bronvermelding: Xian, J., Wang, L., Mi, Z. et al. A cyanide-free route towards the electrosynthesis of nitriles. Nat Commun 17, 4095 (2026). https://doi.org/10.1038/s41467-026-70732-5
Trefwoorden: elektrosynthese, groene chemie, nitrilen, ammoniak, gebruik van afvalgassen